
【题目】石灰石高温煅烧获得的生石灰是炼钢生产中的主要碱性造渣材料,其活性度好坏对冶炼过程有重要影响。
(提出问题)哪些因素可能影响生石灰的活性度?
(查阅资料)生石灰活性度体现了生石灰与其他物质的反应能力,是表征生石灰水化反应速度的一个指标。生产中常用的检测标准定义为:在足够时间内,用中和生石灰消化时产生的Ca(OH)2所消耗的盐酸的体积数(单位为mL)表示。
(进行实验)
实验1:相同条件下,煅烧不同石灰石,测生石灰的活性度。
产地 | 石灰石 | 生石灰 | |
外观 | CaO含量/% | 活性度/mL | |
A地 | 灰白色 | 94.89 | 391 |
B地 | 灰白色带少量红棕色 | 89.97 | 375 |
实验2:取某石灰石试样,在电炉内进行煅烧,烧成后测定生石灰的活性度。
时间/min | 各煅烧温度下的生石灰活性度/mL | |||||
1050℃ | 1100℃ | 1150℃ | 1200℃ | 1250℃ | 1300℃ | |
12 | 790 | 836 | 868 | 808 | 454 | 412 |
16 | 793 | 856 | 871 | 845 | 556 | 530 |
20 | 795 | 863 | 873 | 864 | 617 | 623 |
实验3:煅烧温度1050℃时,加NaCl和不加NaCl,比较煅烧石灰石的分解率(分解率影响生石灰活性度)。
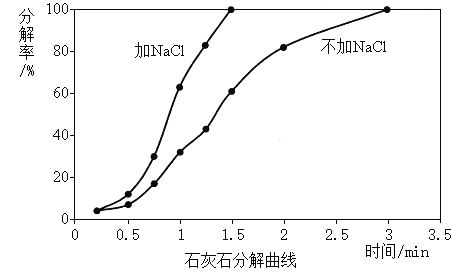
(解释与结论)
(1)实验1的目的是___________。
(2)能证明最佳煅烧温度为1100~1200℃的证据是__________。
(3)实验3的结论是_________。
(反思与评价)
(4)写出石灰石高温分解生成生石灰和另一种氧化物的化学方程式_________。
(5)除以上研究的可能影响生石灰活性度的因素外,你认为还可以研究的其他因素有_______(写出一条即可)。
【答案】探究石灰石种类对生石灰活性度的影响 12min时,煅烧温度在1100~1200℃时的生石灰活性度都大于800mL,而其他温度时都较小 加入NaCl提高石灰石分解速率,影响生石灰活性度 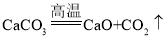 原料粒度(其他答案如:保温时间、杂质成分等合理给分)
原料粒度(其他答案如:保温时间、杂质成分等合理给分)
【解析】
(1)实验1是相同条件下,煅烧不同石灰石,测生石灰的活性度,故实验1的目的是探究石灰石种类对生石灰活性度的影响。
(2)某个相同时间段时,煅烧温度为1100℃、1150℃和1200℃的生石灰活性度比其他温度时的大,说明为最佳煅烧温度,故能证明最佳煅烧温度为1100~1200℃的证据是12min时,煅烧温度在1100~1200℃时的生石灰活性度都大于800mL,而其他温度时都较小。
(3)由实验3图像可知,相同时间,加NaCl时煅烧石灰石的分解率较大,故实验3的结论是加入NaCl提高石灰石分解速率,影响生石灰活性度。
(4)石灰石高温分解生成生石灰和另一种氧化物是二氧化碳,反应的化学方程式为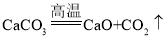 。
。
(5)除以上研究的可能影响生石灰活性度的因素外,还可以研究的其他因素有原料粒度(保温时间、杂质成分等)。


科目:初中化学 来源: 题型:
【题目】某工厂排放的工业废水中含有硫酸亚铁和少量硫酸铜。下图是从该废水中回收金属铜和硫酸亚铁晶体的主要流程,请回答下列问题:

(1)工业废水中加入铁粉后发生反应的化学方程式为______________。
(2)操作I名称为______________。
(3)进行操作I前加入稀硫酸的目的是___,能否用稀盐酸代替?_______(填“能”或“不能”),原因是______________。
(4)实验室稀释浓硫酸的具体操作为______________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】A﹣J是初中化学常见的物质,它们的相互转化关系如图所示。其中A是烘焙糕点所用发酵粉的主要成分之一;H和D的组成元素相同;I是红棕色固体。

请回答下列问题:
(1)写出下列物质的化学式:B______D_____。
(2)反应④的化学方程式_____,其实际应用为___。
(3)J制品在沙漠地区锈蚀缓慢的原因是_____;合金中_____含有非金属(填“一定”、“可能”或“不”)。
查看答案和解析>>
科目:初中化学 来源: 题型:
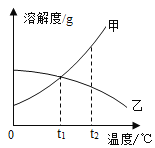
【题目】甲、乙两种物质的溶解度曲线如下图所示。t1℃时,将等质量的水分别加入到各盛有等质量甲、乙的试管中,充分振荡后,试管底部均有未溶解的固体,再将其温度都升高到t2℃。
0
(1)t1℃时,等质量甲、乙分别配成饱和溶液,所需水的质量甲____乙(填“>”“<”或“=”);
(2)若不考虑水分的蒸发,由t1℃升温到t2℃的过程中,下列说法正确的是_____(填序号,下同);
A 甲乙两种物质的溶解度都增大 B 甲物质的溶解度小于乙物质的溶解度
C 甲溶液的质量减小 D 装有乙物质的试管中剩余固体增多
(3)通常情况下,在实验室用甲和水配制一定溶质质量分数的甲溶液,需用到的仪器有:托盘天平、烧杯和___。
A 酒精灯 B 药匙 C 玻璃棒 D 漏斗 E 铁架台 F 量筒 G 胶头滴管
(4)现有t2℃甲的饱和溶液,其中含少量乙。为得到纯净的甲物质,下列设计方案正确的是__。
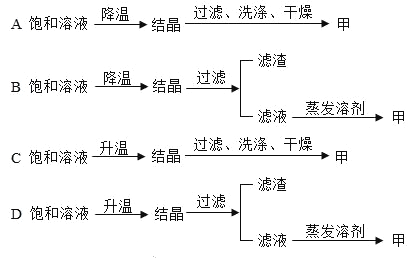
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】如图所示,在白色点滴板1-6的孔穴中,分别滴加适量稀盐酸,研究物质的性质。
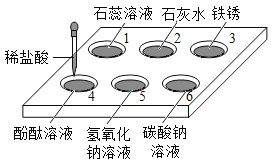
(1)没有明显现象变化的孔穴有___________(填孔穴序号)。
(2)孔穴3中发生反应的化学方程式为___________。
(3)孔穴6反应后的溶液中溶质是(写出所有可能)_________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】根据如图中a、b、c三种物质的溶解度曲线,回答下列问题:

(1)P点表示在t1℃时b和c两物质的溶解度相等,还可以表示______________。
(2)现有等质量的a、b、c三种物质,配成t2℃时的饱和溶液,所得饱和溶液质量的大小关系为_________。
(3)t2℃时,50 g b物质加入到50 g水中充分溶解后,所得溶液的质量为_______。
(4)b中含有少量的a,若要提纯b,可采用________结晶的方法。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】25℃时,探究某固体物质的溶解性,实验记录如下表。下列实验结论正确的是( )
编号 | ① | ② | ③ | ④ |
水的质量/g | 50 | 50 | 50 | 50 |
加入固体质量/g | 5 | 10 | 15 | 20 |
现象 | 固体完全溶解 | 固体完全溶解 | 剩余少量固体 | 剩余较多固体 |
A.实验①所得溶液的溶质质量分数是实验②的一半
B.在实验④中再加入50g 水后,溶液的溶质质量分数为15%
C.由表格中的数据可以确定 25℃时该物质的溶解度大小的范围是:20 g≤S<30g
D.实验②中温度由25℃冷却到10℃时,一定有固体析出
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】已知 A~G 是初中化学常见的物质,A 通常为黑色粉末,C 为无色气体,E 常用于制肥皂,G 为目前世界上年产量最高的金属,若用 “—”表示两种物质能发生反应,用“![]() ”表示一种物质能转化为另一种物质,
”表示一种物质能转化为另一种物质,![]() 表示相互转化,且有些反应需在溶液中进行。请回答下列问题:
表示相互转化,且有些反应需在溶液中进行。请回答下列问题:
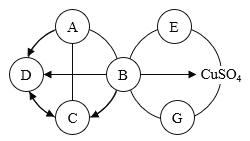
(1)请写出物质(溶质)的化学式:B__________________;D______________;E________________;G___________________;
(2)硫酸铜溶液与片状固体 G 反应的现象是___________________;
(3)A 与 C 反应的化学方程式为______________。
查看答案和解析>>
科目:初中化学 来源: 题型:
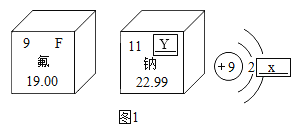
【题目】“宏观--微观--符号”三重表征是化学视角认识物质及其变化的方法。
(1)如图1是两种元素在元素周期表中的信息以及氟原子的原子结构示意图,Y是______,![]() ______,氟原子在化学反应中容易形成______
______,氟原子在化学反应中容易形成______![]() 写离子符号
写离子符号![]() 。
。
(2)如图2是某密闭容器中氢气在氧气中燃烧的微观示意图,根据图示回答下列问题。
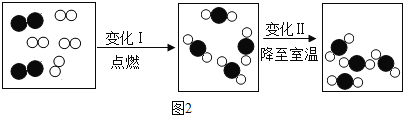
①变化前后,没有发生改变的粒子是______![]() 填粒子名称
填粒子名称![]() ,变化Ⅰ和变化Ⅱ的本质区别是______。
,变化Ⅰ和变化Ⅱ的本质区别是______。
②上述变化过程中共有______种元素,共有______种物质。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com