
分析 (1)甲烷属于碳氢化合物,完全燃烧能生成水和二氧化碳.
(2)二氧化硫、氮氧化物溶于雨水时,能和水反应生成酸,当溶有酸的雨水的酸性达到一定程度时,就形成酸雨,酸雨能够腐蚀建筑物,毁坏森林树木,酸化水体、土壤等.
煤燃烧时,含有的硫能和氧气反应生成二氧化硫,二氧化硫能和氧化钙反应生成亚硫酸钙,亚硫酸钙能和氧气反应生成硫酸钙.
解答 解:
(1)甲烷燃烧能生成水和二氧化碳,反应的化学方程式为:CH4+2O2 $\frac{\underline{\;点燃\;}}{\;}$ CO2+2H2O.
故填:CH4+2O2 $\frac{\underline{\;点燃\;}}{\;}$ CO2+2H2O.
(2)二氧化硫能和水反应生成亚硫酸,亚硫酸能和氧气反应生成硫酸,含有亚硫酸或硫酸的雨水,当
pH<5.6时就形成酸雨,酸雨能够影响植物生长,腐蚀金属制品,破坏大理石建筑物等.
故填:酸雨能够影响植物生长,腐蚀金属制品,破坏大理石建筑物等.
在煤中加入生石灰或石灰石时,煤燃烧产生的高温能使石灰石分解成生石灰和二氧化碳,生石灰能和硫燃烧生成的二氧化硫反应生成亚硫酸钙,亚硫酸钙能和氧气反应生成硫酸钙,从而防止二氧化硫进入空气中.
故填:生石灰(或石灰石).
答案:
(1)CH4+2O2 $\frac{\underline{\;点燃\;}}{\;}$ CO2+2H2O.
(2)酸雨能够影响植物生长,腐蚀金属制品,破坏大理石建筑物等;生石灰(或石灰石).
点评 解题时的关键抓住沼气的主要成分甲烷及其性质并结合生活实际来分析.


 华东师大版一课一练系列答案
华东师大版一课一练系列答案科目:初中化学 来源: 题型:解答题
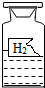 某化学课外小组的同学,在实验室实验时发现一瓶标签破损的无色溶液(如图).这瓶溶液是什么物质?在老师的指导下,同学们首先对该溶液成分提出假设并进行了如下的探究活动.请在空白处完成相应内容.
某化学课外小组的同学,在实验室实验时发现一瓶标签破损的无色溶液(如图).这瓶溶液是什么物质?在老师的指导下,同学们首先对该溶液成分提出假设并进行了如下的探究活动.请在空白处完成相应内容.查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 化合反应 | B. | 分解反应 | C. | 置换反应 | D. | 复分解反应 |
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
| 试剂1 | 试剂2 | 混合前温度/℃ | 混合后温度/℃ | |
| 35毫升稀盐酸 | 25毫升NaOH溶液 | 20.0 | 第1次 | 24.2 |
| 第2次 | 24.0 | |||
| 第3次 | 24.4 | |||
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com