
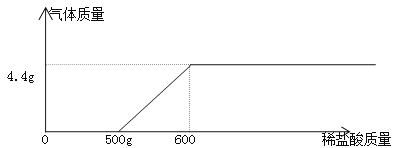
【题目】现有NaOH、NaCl和Na2CO3固体混合物109.1g。在烧杯中加入水溶解,向烧杯中加入稀盐酸,加入稀盐酸的质量与产生气体的关系如图:
求:
(1) 完全反应后,产生二氧化碳气体的体积是多少L?,保留一位小数。(已知二氧化碳气体密度为1.9g/L)
⑵加入稀盐酸的的质量分数?
⑶计算原混合物中NaCl的质量分数,保留一位小数。
【答案】(1)2.3L;(2)7.3%;⑶53.6%
【解析】
NaOH、NaCl和Na2CO3固体混合物中的Na2CO3固体能与稀盐酸反应生成二氧化碳气体,根据图像可知,与Na2CO3固体反应的稀盐酸的质量为:600g-500g=100g。(1)因为ρ=![]() ,所以v=
,所以v=![]() =
=![]() =2.3L。
=2.3L。
⑵设加入稀盐酸的的质量分数为x,则100g稀盐酸所含溶质的质量为:100g×x
Na2CO3 + 2HCl == 2NaCl + H2O + CO2↑
73 44
100g×x 4.4g
![]() =
=![]() ,解得x=7.3%
,解得x=7.3%
⑶根据图像可知,与NaOH反应的稀盐酸的质量为500g,500g稀盐酸中所含溶质的质量为:500g×7.3%=36.5g
设固体混合物中NaOH的质量为y
NaOH + HCl == NaCl + H2O
40 36.5
y 36.5g
![]() =
=![]() ,解得y=40g
,解得y=40g
设固体混合物中Na2CO3的质量为z
Na2CO3 + 2HCl == 2NaCl + H2O + CO2↑
106 44
z 4.4g
![]() =
=![]() ,解得z=10.6g
,解得z=10.6g
原混合物中NaCl的质量为:109.1g-10.6g-40g=58.5g
则原混合物中NaCl的质量分数为:![]() ×100%=53.6%
×100%=53.6%


 阅读快车系列答案
阅读快车系列答案科目:初中化学 来源: 题型:
【题目】小金为了探究温度对H2O2分解反应速率的影响,借助如图所示实验装置(夹持装置略去),进行了两次实验,两次实验的部分设计如表所示:

(1)写出实验中发生的化学反应的化学式表达式:_____________,二氧化锰在反应中的作用是__________。取用二氧化锰可以用________(填“药匙”或“镊子”)。
(2)MnO2中锰元素的化合价为___________;
(3)实验2中应加入5%H2O2_____________毫升;
(4)在两次实验中,可通过_______________来比较H2O2分解反应速率的大小;
(5)实验2中水浴温度控制在80℃时,测定的反应速率会比真实值偏大,其原因除锥形瓶内气体受热膨胀外,还有______________;
(6)实验结束后若要将MnO2从混合物中分离回收,可采取的方法是_____________。该方法用到的玻璃仪器有玻璃棒、___________、____________。玻璃棒的作用是______,将本实验中的二氧化锰经分离、干燥后称量,其质量为________g。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】化学是一门以实验为基础的科学,请回答问题:

(1)写出实验室用A装置制氧气的化学方程式_________。
(2)实验室现用B装置制取二氧化碳气体,多孔塑料片上面放置石灰石,打开止水夹M,取下左侧的橡胶塞,向U型管内加入稀盐酸,U型管内发生反应的化学方程式为___________________,一段时间后,关闭M后,呈现的现象是______________,该装置的优点是____________。若用C装置收集该气体,气体应从 _________(填“a”或“b”)端通入。
(3)有人提出工业生产上回收利用空气中CO2的构想:把空气吹入饱和碳酸钠溶液中,溶液可吸收CO2生成碳酸氢钠(NaHCO3);加热碳酸氢钠分解放出CO2并生成碳酸钠等;CO2在合成塔内与氢气反应生成甲醇。
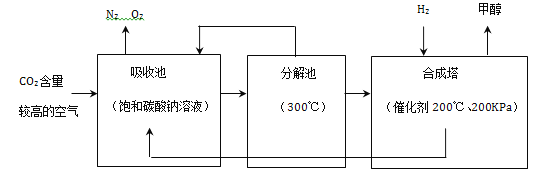
①分解池中发生的化学方程式为_________。
②合成塔中参加反应的氢气、二氧化碳与生成的甲醇和水的分子个数比为3︰1︰1︰1,则甲醇分子中碳、氢、氧原子的个数比为_________。
③该流程中能循环利用的物质是水和_________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】用化学用语填空:(1)2个氧分子_________(2)3个铁离子___________________
(3)标出过氧化氢中氧元素的化合价_________(4)2个镁原子_______(5)硫酸铜中的阴离子:__________
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】甲、乙、丙三种物质的溶解度曲线如图所示.根据下图中信息回答下列问题:
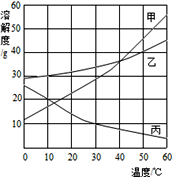
(1)50℃时,乙物质的溶解度是_______g。
(2)40℃时,甲、乙、丙三种物质的饱和溶液各1195克,则在甲、乙、丙三种物质饱和溶液中含有水的质量大小顺序为_____________。(用甲、乙、丙表示)
(3)甲、乙、丙三种饱和溶液,温度由50℃逐渐降低到20℃时,____________溶质的质量分数没有改变。(用甲、乙、丙表示)
(4)50℃时,将等质量的甲、乙、丙三种物质的饱和溶液同时升温至60℃,所得溶液中溶质质量分数最小的是_____。
(5)要配制140g溶质质量分数为28.5%的乙物质溶液,配制时溶液的温度需要控制的范围是_______。(填“≥50℃”或“≥40℃”或“≥30℃”或“≥20℃”)
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】某同学设计下图所示的实验装置进行一氧化碳还原氧化铜的实验。试回答:
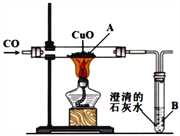
(1)实验开始时,为什么要先通一会一氧化碳,再给 A处的氧化铜加热?_________________;A处看到的现象__________,A处发生反应的化学方程式是___________________。B处发生反应的化学方程式是________________________;
(2)该装置存在的一个主要问题是___________________;
(3)加热一段时间后,如果要对A处残留固体的组成进行探究,试猜想残留固体的组成为__________________________________________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】下图为某反应的微观示意图,下列说法错误的是
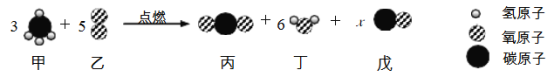
A. x=2
B. 该反应中有4种氧化物
C. 反应前后原子的种类、个数、质量都不变
D. 若反应中甲、乙的分子个数比为1∶2时,则无物质戊生成
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】化学式在分子、原子水平上研究物质的组成、结构、性质及其应用的一门基础自然科学.
(1)现有H、O、S、K四种元素,从中选择合适的元素,根据下面物质分类的要求,组成相应类别物质的化学式,填在如图所示的横线上.
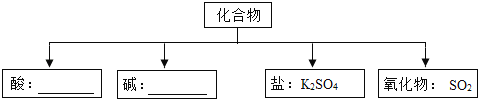
(2)下表列出了部分元素的原子结构示意图.请回答下列问题:
O | Mg | S | Cl |
|
|
|
|
氧原子的核电荷数为 ,硫原子在化学反应中易 (填“得到”或“失去”)电子,由镁元素和氯元素组成化合物的化学式为 ,氧元素和硫元素化学性质具有相似性的原因是它们的原子 相同.
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】化学兴趣小组同学在实验室发现一瓶标签残缺的无色液体(如图)
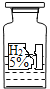
(温馨提示:标签上的5%表示该混合物中主要成分所占的质量分数)。他们对此瓶无
色液体是什么产生了兴趣,于是进行了如下探究。
(猜想)猜想一:水﹔猜想二:稀硫酸(H2SO4)﹔猜想三:过氧化氢溶液
小组同学对标签又进行了仔细的观察、分析,他们一致认为猜想一不合理。理由是____________。
(设计方案)同学们结合所学知识设计出如下探究方案:向盛有少量二氧化锰的试管中加入适量的该液体,并将带火星的木条放在试管口。
(实验)按上述方案进行实验.发现有大量气泡产生,带火星的木条复燃。
(结论与解释)(1)以上事实证明猜想__________是正确的;
(2)产生气体的化学反应文字表达式为 ______________________________
(反思与评价)(1)在实验中,某同学提出应该先将气体收集。然后用带火星的木条检验,你认为____________(填“有”或“没有”)必要。
(2)为避免在今后的实验中出现标签残缺的情况,在倾倒液体时应注意____________
(拓展与迁移)根据探究结果,重新贴好标签。标签上化学式中氧元素的化合价为________ (已知氢元素显+l价)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com