
分析 (1)根据河水中有水、可溶性物质、溶解在水中的气体等分析;
(2)煮沸能使硬水软化;
(3)要测定水样的酸碱度,常使用pH试纸或pH计;
(4)根据溶液的定义分析判断;
(5)用肥皂水可区分软水和硬水.
解答 解:(1)流溪河水中含有水、溶解进去的气体,可溶性杂质等物质,属于混合物;
(2)生活中使硬水软化的一种最常用方法是煮沸;
(3)要测定某工业水样的酸碱度,最适宜的是使用pH试纸或pH计,酸碱指示剂只能测定溶液酸碱性,不能测定酸碱性的强弱,故选B;
(4)蔗糖加入蒸馏水中,用玻璃棒不断搅拌,能形成无色溶液,无水硫酸铜加入水中形成是蓝色溶液,泥沙和花生油加入水中,用玻璃棒不断搅拌,不能形成均一稳定的混合物.故选C.;
(5)皂水可区分软水和硬水,加肥皂水后生成泡沫多的是软水,生成泡沫少的是硬水.
故答案为:(1)纯净物;
(2)煮沸;
(3)B;
(4)C;
(5)泡沫.
点评 本题考查了有关水的知识,根据所学内容细心分析即可,有利于学生通过题目对水的有关知识归纳总结.


 孟建平名校考卷系列答案
孟建平名校考卷系列答案科目:初中化学 来源: 题型:选择题
| A. | 滤液中一定含有硝酸亚铁和硝酸银,可能含有硝酸铜 | |
| B. | 滤液中一定含有硝酸亚铁、硝酸银、硝酸铜 | |
| C. | 滤渣中一定含有铁、银、铜 | |
| D. | 滤渣中一定含有银,可能含有铜 |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题

查看答案和解析>>
科目:初中化学 来源: 题型:解答题
 | 商品名 | 固体管道疏通剂 |
| 主要成分 | 氢氧化钠60% 碳酸钠15% | |
| 注意事项 | 不要与皮肤接触 | |
| 含量 | 600g |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
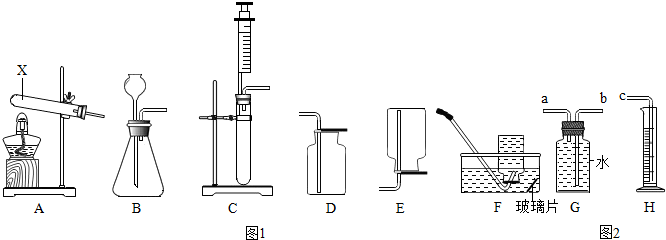
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
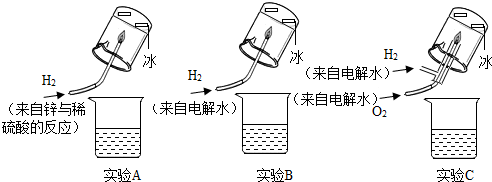
| 实验序号 | 加入液体 | 实验现象 |
| ① | 实验A 的收集液4.0mL | 褪色 |
| ② | 实验B 的收集液5.5mL | 褪色 |
| ③ | 实验C的收集液10.0mL | 不褪色 |
| ④ | 蒸馏水10.0mL | 不褪色 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
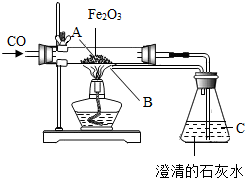 某课外活动小组的同学们在老师的帮助下,探究用赤铁矿(主要成分是Fe2O3)炼铁的主要反映原理.他们设计的实验装置如图所示,回答下列问题:
某课外活动小组的同学们在老师的帮助下,探究用赤铁矿(主要成分是Fe2O3)炼铁的主要反映原理.他们设计的实验装置如图所示,回答下列问题:查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com