
【题目】某同学进行如图实验,充分反应后,将试管①②内的物质倒入同一烧杯中混合再充分反应后过滤,结果得到滤渣A和无色滤液B。
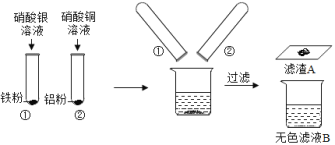
(1)试管①中反应的化学方程式为:_____;试管②中观察到的现象是:有红色固体出现,溶液_____。
(2)过滤操作中需要的玻璃仪器有:烧杯、玻璃棒和_____;无色滤液B中含有的物质是H2O和_____ (填化学式 )。
(3)设计实验探究滤渣A的成分
(提出问题)滤渣A的成分是什么?
(查阅资料)银、铜、铁、铝四种金属中,只有铝可以和氢氧化钠溶液反应,化学方程式为:2Al+2NaOH+2H2O═2NaAlO2+3H2↑。
(作出猜想)滤渣A的成分为:
猜想Ⅰ:银、铜;猜想Ⅱ:银、铜、铁;猜想Ⅲ:_____。
(分析思考)猜想Ⅰ一定不正确,原因是_____。
(进行实验)取两份滤渣样品进行实验,请填写下列空白:
样品 | 加入试剂 | 现象 |
第一份样品 | 足量稀盐酸 | 产生气泡,固体部分溶解,溶液变_____色 |
第二份样品 | 足量氢氧化钠溶液 | 现象b |
(作出判断)如果现象为b为“产生气泡,固体部分溶解”,则猜想_____成立;
如果现象b为_____,则猜想_____成立。
【答案】Fe+2AgNO3![]() Fe(NO3)2+2Ag 由蓝色变成无色 漏斗 Al(NO3)3 银、铜、铁、铝 滤渣A中一定含有铁 浅绿 Ⅲ 不产生气泡,固体不溶解 Ⅱ
Fe(NO3)2+2Ag 由蓝色变成无色 漏斗 Al(NO3)3 银、铜、铁、铝 滤渣A中一定含有铁 浅绿 Ⅲ 不产生气泡,固体不溶解 Ⅱ
【解析】
(1)金属活动性顺序中,排在前面的金属能将排在后面的金属从其化合物的水溶液中置换出来,Fe+2AgNO3![]() Fe(NO3)2+2Ag。铝能将硝酸铜溶液中的铜置换出来,2Al+3Cu(NO3)2== 2Al(NO3)3 +3Cu,Cu(NO3)2溶液是蓝色,Al(NO3)3溶液是无色的,所以溶液由蓝色变为无色。
Fe(NO3)2+2Ag。铝能将硝酸铜溶液中的铜置换出来,2Al+3Cu(NO3)2== 2Al(NO3)3 +3Cu,Cu(NO3)2溶液是蓝色,Al(NO3)3溶液是无色的,所以溶液由蓝色变为无色。
(2)过滤操作中需要的玻璃仪器有:烧杯、玻璃棒和漏斗。Fe(NO3)2溶液是浅绿色,所以无色滤液B中含有生成的Al(NO3)3 和溶剂水。
(3)因为铝比铁金属活动性强,无色滤液B中含有Al(NO3)3,无Fe(NO3)2,则是铝将Fe(NO3)2反应完了,2Al+3Fe(NO3)2 ==2Al(NO3)3+3Fe,滤渣中一定含有生成的Fe,很可能含有铝,所以A的成分可能是银、铜、铁、铝。分析思考:猜想Ⅰ一定不正确,原因是滤液是无色溶液,说明硝酸亚铁和铝完全反应生成硝酸铝和铁,因此滤渣A中一定含有生成的铁。进行实验:Fe +2HCl== FeCl2+H2↑,稀盐酸是无色溶液,FeCl2溶液是浅绿色,所以实验现象是溶液由无色变为浅绿色。作出判断:银、铜、铁、铝四种金属中,只有铝可以和氢氧化钠溶液反应,生成氢气,如果现象b为“产生气泡,固体部分溶解”,则说明固体中有铝,猜想Ⅲ成立;如果现象b为不产生气泡,固体不溶解,说明滤渣中不含有铝,则猜想Ⅱ成立。


科目:初中化学 来源: 题型:
【题目】(一) 实验室使用过氧化溶液与二氧化锰制取氧气并回收二氧化锰,可供选择的实验仪器和用品如下。
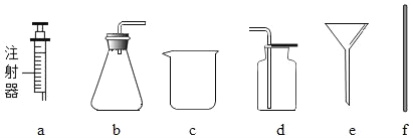
(1)仪器C的名称为_______________________。
(2)上述方法制取氧气的化学方程式_____________________________。
(3)制取氧气时,用a仪器加入过氧化氢溶液不能达到的目的是_______(填序号)。
A. 便于控制反应快慢B.定量添加药品更方便C.生成氧气质量更大
(4)回收二氧化锰时,将固液分离的操作是_______,该过程中玻璃棒的作用是______________;除图中仪器以外,过滤还需要的仪器名称是_______________。
(5)回收的二氧化锰,还可以在上述反应中反复使用。其原因是___________________________。
(二)某同学要探究燃烧的条件和空气中氧气的含量,进行了如下实验。(已知:白磷的着火点为![]() )
)

(1)对比步骤II和IV的现象可知,可燃物燃烧的条件之一是____________________。
(2)待装置冷却一段时间后,打开K2,如果观察到_________________________________,说明空气中氧气的体积约占1/5。若实验测得空气中氧气的体积分数小于1/5,原因可能是_______________________。(答一条即可)
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】已知硝酸钾在不同温度下的溶解度如表:
温度(℃) | 20 | 30 | 40 | 50 | 60 | 70 | 80 |
溶解度(g/100g 水) | 32 | 46 | 64 | 85.5 | 110 | 138 | 170 |
甲是 80℃含有 100g 水的 KNO3 溶液,操作过程如图所示。以下分析错误的是( )
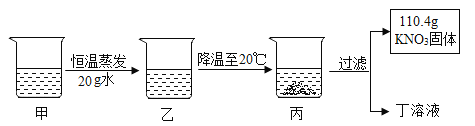
A. 甲一定是不饱和溶液,乙可能饱和溶液
B. 甲乙丙丁溶液中溶质的质量分数关系式乙>甲>丙=丁
C. 甲溶液中,溶剂与溶质的质量比为 25:34
D. 甲溶液冷却时,开始析出固体的温度在 60℃~70℃之间
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】含碳元素的物质在自然界中普遍存在.请回答下列问题:
(1)已知碳元素的原子结构示意图为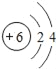 ,其最外层电子数为_____.
,其最外层电子数为_____.
(2)请根据下图提供的信息,在相应的位置上写出不同单质的名称或化学式:
名称:_____ | 化学式:_____ | 名称:_____ |
可用于制铅笔芯 |
分子结构 |
单质图片 |
(3)近几十年来,大气中CO2的含量不断上升,使全球变暖.导致大气中CO2含量不断上升的主要因素是(填写序号)_____.
①人和动物的呼吸 ②植物的光合作用 ③化石燃料的大量使用和森林遭到破坏.
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】如图是某化学反应的微观模型,“![]() ”和“
”和“![]() ”分别表示不同元素的原子,下列对图示模型的理解正确的是 ( )
”分别表示不同元素的原子,下列对图示模型的理解正确的是 ( )
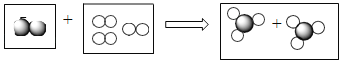
A. 该反应属于分解反应
B. 参加反应的两种物质的分子个数比为 2:3
C. 只有一种单质参与该反应
D. 共有两种元素参与反应
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】甲、乙、丙、丁四种物质在反应前后的质量关系如图所示,下列有关说法错误的是
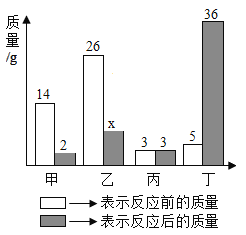
A. 参加反应的甲和乙质量比为2:7 B. 丙可能是该反应的催化剂
C. 丁一定是化合物 D. x的值是7
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】初中化学课本中的部分实验如下图。请你回答下列问题。
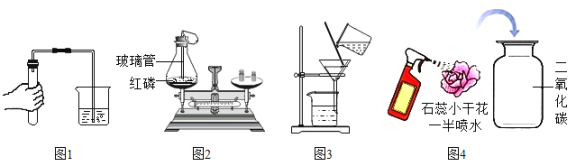
(1)图1是检查装置气密性的实验。将导管放入水中的目的是_____,证明装置不漏气的现象是_____。
(2)图2是验证质量守恒定律的实验装置。在锥形瓶瓶塞上的玻璃管外端套一个瘪气球,瘪气球的作用是_____。
(3)图3是过滤液体的实验。倒入液体时漏斗内液面要低于滤纸边缘,主要是为了防止_____。
(4)图4是验证二氧化碳与水反应的实验。其中的花朵是用石蕊溶液染成的紫色干燥纸花。把石蕊小干花一半喷水后放入盛满二氧化碳的集气瓶中,观察到的现象是_____,石蕊小干花喷一半水的目的是_____。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】结合右表(元素周期表的一部分)中原子结构示意图,回答有关问题。
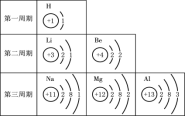
(1)铍(Be)属于“金属”或“非金属”中的 ________元素;H2 是由________构成的物质(填“分子”、“原子”或“离子”)。
(2)一个锂(Li)原子容易失去_______个电子,形成的离子用符号可以表示为_______;Mg原子中的质子数为 _______;Al具有 很好的抗腐蚀性,是因为________。
(3)从原子结构上看,同一周期的元素具有相同的_______数。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】煤化工是以煤为原料,经过化学加工使煤转化为气体、液体、固体燃料以及各种化工产品的工业过程。请回答下列问题:
(1)下列说法正确的是_______。
A.煤是复杂的混合物,主要含碳元素
B.由煤加工成焦炭发生的是物理变化
C.家用“液化石油气”就是煤隔绝空气加热得到的产品
D.煤燃烧排放的二氧化硫、二氧化氮是形成酸雨的主要物质
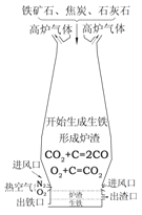
(2)煤的加工产品有很多用途,其中焦炭广泛应用于炼铁。如图是高炉炼铁的示意图。请根据图例回答:
①炼铁过程中焦炭的作用是__________________________;
②高炉炼铁会产生大量的高炉气体,其主要成分是高浓度的CO和氧化铁尘粒。请你对高炉气体的处理提出合理化的建议___________________。
(3)化肥厂生产合成氨的原料是煤、空气、水。生产简要流程如下:
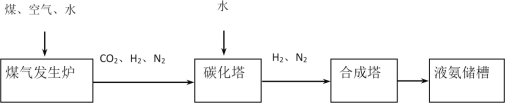
煤气发生炉中主要反应:①C+O2=CO2;②C+H2O=CO+H2。两个反应必须进行调控才能保持一定的炉温。判断:反应②________(填“放出”或“吸收”)热量。将合成的氨气部分通入碳化塔,既除去了二氧化碳又得到了化肥NH4HCO3,试写出该反应的化学方程式_____________________________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com