
【题目】化学是一门以实验为基础的科学。
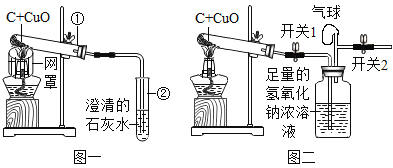
(1)化学课堂上,老师做了如图一的实验(网罩的作用是_____)。随着不断加热,试管①里逐渐有红色固体产生,化学方程式为_____,该反应的基本反应类型属于_____。同时试管②里的现象是_____。
(2)小明发现通入试管②里的气体有逸出液面的现象,怀疑试管①里还有其它气体生成,比如一氧化碳。老师首先赞扬小明有科学的质疑精神,建议在化学兴趣小组的活动中展开探究。请你也参与其中,一起探究。
(提出问题)碳还原氧化铜的反应还有一氧化碳生成吗?
(猜想与假设)猜想一:没有一氧化碳生成;猜想二:还有一氧化碳生成
(设计方案)在老师的帮助下,小明设计出如图二实验。为了提高实验效果,小明加大了反应物的用量。老师提示:实验前应先验纯,再将两个开关都打开,再加热,反复挤压气球,将其中的气体排尽,老师这样提示的目的是_____。
(进行实验)
实验操作 | 实验现象 | 实验结论 |
先按老师的提示操作,加热一会儿后,关闭开关2.待充分反应,关闭开关1,停止加热。 | 黑色粉末变成红色_____ | 逸出液面的气体不是二氧化碳 |
_____ | 气体被点燃 | 逸出液面的气体是一氧化碳。猜想二成立。 |
(交流与提高)同学们通过对以上实验的讨论与分析,认为一氧化碳的产生至少源自两个反应:
一是试管内反应物直接反应生成;二是生成物又发生反应而生成。请你写出其中一个化学方程式_____。
实验中生成的二氧化碳被氢氧化钠浓溶液吸收没有明显现象,同学们想进一步检验该反应的生成物,可选用的药品有_____(填序号)。
①酚酞溶液 ②氢氧化钙溶液 ③稀盐酸 ④锌粒 ⑤氯化钙溶液
某同学在做碳还原氧化铜的实验时,碳粉将8g氧化铜完全还原后收集到的气体质量总和为2.4g,则此时生成的气体为_____。
(评价与反思)经过本次活动,同学们感到,正是因为小明具有质疑精神,我们这次活动才有了更多、更新的收获。同时也认为图一装置不够完善,为了防止尾气对空气的污染,应该把上图装置中的右部分装置换成下列_____装置(填字母序号)。

【答案】聚拢火焰,提高温度 2CuO+C![]() 2Cu+CO2↑ 置换反应 澄清的石灰水变浑浊 排出装置内的空气,防止加热时产生爆炸 一段时间后气球变小,但是没有完全变瘪 打开开关2,点燃气体 CO2+C
2Cu+CO2↑ 置换反应 澄清的石灰水变浑浊 排出装置内的空气,防止加热时产生爆炸 一段时间后气球变小,但是没有完全变瘪 打开开关2,点燃气体 CO2+C![]() 2CO ②③⑤ CO和CO2 A(或B或D)
2CO ②③⑤ CO和CO2 A(或B或D)
【解析】
(1)图一实验中,酒精灯上网罩的作用是聚拢火焰提高温度;试管①中,碳与氧化铜在高温的条件下反应生成铜和二氧化碳,该反应是由单质与化合物反应生成另一种单质与另一种化合物,属于置换反应;生成了二氧化碳,能使澄清的石灰水变浑浊,故填:聚拢火焰,提高温度;2CuO+C![]() 2Cu+CO2↑;置换反应;澄清的石灰水变浑浊;
2Cu+CO2↑;置换反应;澄清的石灰水变浑浊;
(2)[设计方案]先将两个开关都打开,再加热,反复挤压气球一会儿。是为了排出装置内的空气,防止加热时产生爆炸,故填:排出装置内的空气,防止加热时产生爆炸;
[进行实验]
实验操作 | 实验现象 | 实验结论 |
先按老师的提示操作,加热一会儿后,关闭开关2.待充分反应,关闭开关1,停止加热。 | 黑色粉末变成红色,一段时间后气球变小,但是没有完全变瘪。 | 逸出液面的气体不是二氧化碳 |
打开开关2,点燃气体 | 气体被点燃 | 逸出液面的气体是一氧化碳。猜想二成立。 |
故填:一段时间后气球变小,但是没有完全变瘪;打开开关2,点燃气体。
[交流与提高]一氧化碳的产生至少源自两个反应:一是试管内反应物直接反应生成,即碳和氧化铜反应生成铜和一氧化碳,二是生成物又发生反应而生成,即是二氧化碳和碳高温反应生成一氧化碳,故填:CO2+C![]() 2CO。
2CO。
实验中生成的二氧化碳被氢氧化钠浓溶液吸收没有明显现象,生成的是碳酸钠,要进一步检验该反应的生成物,可选用的药品有②氢氧化钙溶液、③稀盐酸、⑤氯化钙溶液,故填:②③⑤;
若碳与氧化铜反应生成二氧化碳,设碳与氧化铜反应生成二氧化碳的质量为x,则:
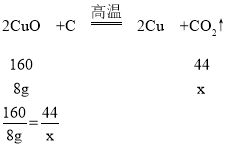
x=2.2g
若碳与氧化铜反应生成一氧化碳,设碳与氧化铜反应生成一氧化碳的质量为y,则:
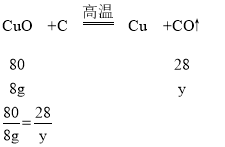
y=2.8g
而实验中生成气体的质量为2.4g,2.2g<2.4g<2.8g,所以生成的气体是二氧化碳与一氧化碳的混合物;故填:CO和CO2;
[评价与反思]为了防止尾气对空气的污染,应该把上图装置中的b部分装置换成如图2中的A、B、D都可以,这是因为A、B、D装置都能够防止一氧化碳进入空气中。故填:A(或B或D);


科目:初中化学 来源: 题型:
【题目】实验室部分仪器或装置如下图所示,请回答下列问题。
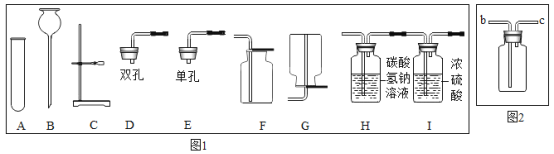
(1)写出仪器B的名称____________。
(2)实验室以氯酸钾为原料制取并收集氧气,完成这个实验图1中还缺少的仪器是_______,反应的化学方程式为____________。若用图2的装置收集氧气,氧气从_______导管口通入(填“b”或“c”),验满的方法__________。
(3)在实验室制取并收集一瓶纯净干燥的二氧化碳,请从图1中选择合适的仪器组装,装置组合为____和H(填编号),反应的化学方程式为________________ , 该反应的基本反应类型_________。其中H装置中碳酸氢钠溶液的作用是__________________。
(4)为了证明氢氧化钙溶液与稀盐酸能发生反应,氢氧化钠溶液与二氧化碳也能发生反应。如图所示进行实验(装置气密性良好,实验前活塞和弹簧夹K处于关闭状态)。

实验一:氢氧化钙溶液与稀盐酸发生反应
打开分液漏斗的活塞,使稀盐酸逐滴滴加入A中锥形瓶,观察到___________的现象时,关闭活塞,证明氢氧化钙溶液与稀盐酸发生反应;
实验二:氢氧化钠与二氧化碳反应
将注射器中的氢氧化钠溶液推入B中锥形瓶,过一段时间后,打开弹簧夹K,观察到_________的现象并且溶液呈红色,证明氢氧化钠溶液与二氧化碳确实发生了反应。请写出二氧化碳与氢氧化钠溶液反应的化学方程式是_____________。锥形瓶B中溶液最后呈红色_________(填“能”或“不能”)证明氢氧化钠有剩余。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】(3分)下列问题的研究中,未利用对比实验思想方法的是( )
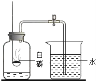
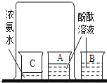
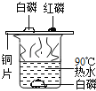
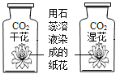
A.研究空气中氧气含量 B.研究分子运动 C.研究燃烧的条件 D.研究二氧化碳与水的反应
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】如图是a、b、c三种物质的溶解度曲线,下列说法正确的是
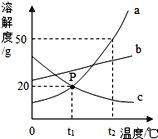
A. P点表示t1℃时,a、c两溶液的溶质质量分数相等
B. 将c物质的饱和溶液变为不饱和溶液,可采用升温的方法
C. t2℃时,将30g a物质加入到50g水中充分搅拌,得到75g a的饱和溶液
D. 将t1℃时a、b、c三种物质的饱和溶液升温至t2℃,其溶质质量分数由大到小的顺序是a>b>c
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】日本福岛第一核电站发生严重的核辐射泄漏,日本政府向核电站附近居民发放碘片,以降低放射性碘对人体的伤害。如图是元素周期表中碘元素的部分信息,则下列说法正确的是( )
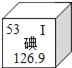
A. 碘元素为金属元素
B. 碘酸钾(KIO3)中碘元素的化合价为+5价
C. 碘原子的中子数为53
D. 碘的相对原子质量为126.9g
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】A-H图是实验室常用来制取气体的装置。

(1)仪器a的名称是______。
(2)利用过氧化氢和二氧化锰制取![]() 发生装置应选仪器______(填序号),反应方程式是______。
发生装置应选仪器______(填序号),反应方程式是______。
(3)用CO还原铁矿石应选用的仪器是______(填序号),加热前应先______,然后用酒精灯加热,实验结束应先______再______。
(4)I图为同学某利用废弃材料设计的家庭小实验,该装置右边部分相当于图A-H中的仪器______(填序号)组合,发生反应的化学方程式是______,该实验左边部分在操作上的优点是______。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】生活处处离不开化学,请用相关知识回答下列问题:
(1)自来水的生产过程中,要加入明矾,是因为明矾溶于水后可以___________水中悬浮的颗粒,形成较大的颗粒而___________,在日常生活中,可以通过___________的方法降低水的硬度。
(2)斯达舒是修正药业著名品牌,其中斯达舒分散片的主要成分是氢氧化铝,用于缓解胃酸过多引起的胃烧灼感、胃痛及慢性胃炎,请写出该药治疗胃酸过多的相应的化学方程式:_____________________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】某兴趣小组同学从实验室中收集到一桶废液,他们想从中回收金属铜和硫酸亚铁,于是设计了以下流程图
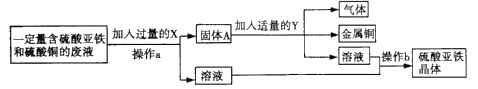
(1)固体A的成分为______;操作a和操作b都要用到一种玻璃仪器,该仪器在操作a中的作用是_______。
(2)加入Y时发生反应的化学方程式为________。
(3)理论上所得硫酸亚铁晶体的质量_________(填“>”“<”或“=”)原废液中硫酸亚铁的质量。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】下列说法正确的是( )
A.质量和质量分数均相等的氢氧化钠溶液与稀硫酸充分反应,所得溶液呈酸性
B.等质量的二氧化硫和三氧化硫,二氧化硫和三氧化硫中硫元素的质量比为4:5
C.硝酸镁样品(含有一种杂质)14.8g,溶于水,与足量的NaOH溶液充分反应生成沉淀5.5g,则样品中可能含有的杂质是MgSO4
D.向一定量的氧化铁与氧化铜的混合物中加入100g质量分数为9.8%稀硫酸,恰好完全反应,则原混合物中氧元素的质量是1.6g
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com