
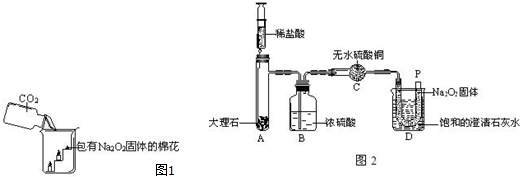
分析 (1)根据实验现象分析二氧化碳的性质;
(2)根据燃烧的条件是有可燃物,与氧气接触,温度达到可燃物的着火点解答;
实验步骤:
③根据大理石和稀盐酸反应生成二氧化碳、水、氯化钙写出化学方程式;
④根据在常温下Na2O2与H2O能发生化学反应解答;
根据资料中的信息:在常温下Na2O2和CO2能发生化学反应,并放出大量的热.分析解答.
根据纤维素完全燃烧生成的是二氧化碳和水解答.
解答 解:(1)实验过程中“下面的蜡烛先熄灭,上面的后熄灭”的现象说明二氧化碳具有不能燃烧也不支持燃烧,且密度比空气的密度大的性质;
(2)燃烧的条件是有可燃物,与氧气接触,温度达到可燃物的着火点;
实验步骤:
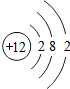
③理石和稀盐酸反应生成二氧化碳、水、氯化钙,化学方程式是:CaCO3+2HCl═CaCl2+H2O+CO2↑;
④B中的浓硫酸可以吸收水分,所以B装置的作用是干燥气体;因为白色的无水硫酸铜吸收水后变成蓝色,所以C装置的作用是证明装置中的水蒸气被除尽.
要使Na2O2与CO2反应,须除去产生的二氧化碳中的水蒸气.实验中要有B、C两装置目的是排除水的干扰;
在常温下Na2O2和CO2能发生化学反应,生成氧气,使带火星的木条复燃;并放出大量的热,溶液温度升高,氢氧化钙的溶解度减小,有固体析出,所以烧杯内的澄清石灰水变浑浊.
纤维素完全燃烧生成的是二氧化碳和水,完全燃烧的化学方程式为:C6H10O5+6O2 $\frac{\underline{\;点燃\;}}{\;}$6CO2+5H2O;
故答案为:
(1)不能燃烧也不支持燃烧,且密度比空气的密度大;
(2)氧气和温度达到棉花的着火点;
实验步骤:
③CaCO3+2HCl═CaCl2+H2O+CO2↑;
④排除水的干扰;
烧杯内的澄清石灰水变浑浊;带火星的木条复燃;
C6H10O5+6O2 $\frac{\underline{\;点燃\;}}{\;}$6CO2+5H2O;
点评 本题探究了过氧化钠与二氧化碳反应的有关知识,完成此题,需要从题干叙述中抽取有用的信息,然后进行解题.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 金属材料中一定不含有非金属元素 | |
| B. | 多数合金的抗腐蚀性能比组成它们的纯金属更好 | |
| C. | 双动力公交车所有部件都是由金属材料制造的 | |
| D. | 地球上的金属资源是取之不尽、用之不竭的 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
 .
.查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 服用含氢氧化铝的药物治疗胃酸过多 | |
| B. | 用熟石灰改良酸性土壤 | |
| C. | 用浓硫酸干燥湿润的氧气 | |
| D. | 用氢氧化钠溶液洗涤石油产品中的残留硫酸 |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
 某同学发现,上个月做实验用的NaOH溶液忘记了盖瓶盖.对于该溶液是否变质,同学们开始实验探究.
某同学发现,上个月做实验用的NaOH溶液忘记了盖瓶盖.对于该溶液是否变质,同学们开始实验探究.| 实验操作 | 可能出现的现象与结论 | 同学评价 | |
| 第1组 | 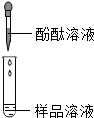 | 若溶液变红,则猜想(2)不成立 | 第2组同学认为:此方案结论不正确,理由是:碳酸钠也可以使酚酞变成红色 |
| 第2组 | 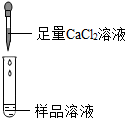 | 若有白色沉淀产生,反应方程式是:Na2CO3+CaCl2=CaCO3↓+2NaCl,则猜想(1)不成立 | 第3组同学认为:此方案还不能确定猜想(2)还是猜想(3)成立 |
| 第3组 | 第一步 第二步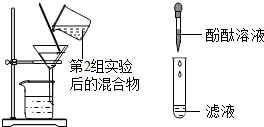 | 若滤液不变红,则猜想(2)成立;若滤液变红,则猜想(3)成立 | 第1组同学认为:不需过滤也能达到实验目的,更简单的操作方法是:将第二组实验沉淀之后取滤液 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
| 实验步骤 | 实验现象 | 解释与结论 |
| 分别取三支试管,向其中加入等质量、等浓度的稀硫酸,然后将铝、铬、铜三种金属片分别插入三支试管中 | 铝片表面产生气泡较快;铬片表面产生气泡较缓慢,溶液变蓝色;铜片无明显现象 | 猜想二成立. 铬与稀硫酸反应生成蓝色的硫酸亚铬(CrSO4),反应的化学方程式为Cr+H2SO4=CrSO4+H2↑ |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com