
【题目】
过氧化氢的分解的变化可用下式表示:
过氧化氢![]() 水+氧气
水+氧气
上述变化所涉及的物质中,属于金属氧化物的是 ,氧元素的化合价为—1价的是 。
用氯酸钾或过氧化氢制取氧气的实验中,都需要加入少量二氧化锰,二氧化锰的作用是 ;若未加入二氧化锰,则反应 (选填“不能发生”或“明显减慢”)
若实验室要制取48g氧气,至少需要氯酸钾多少克?
【答案】(1)二氧化锰(或MnO2)(1分) 过氧化氢(或H2O2)(1分)
(2)加快反应速率(或催化作用)(1分) 明显减慢(1分)
(3)解:设需要KClO3的质量为x。 (0.5分)
2KClO3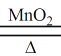 2KCl + 3O2↑ (1分)
2KCl + 3O2↑ (1分)
245 96 (2分)
x 48g
![]() =
=![]() (1分)
(1分)
x=122.5g (1分)
答:至少需要氯酸钾的质量为122.5g。
【解析】(1)金属氧化物是指由金属元素与氧元素形成的氧化物。二氧化锰中是锰、氧两种元素的化合物,属于金属氧化物。
根据化学式可计算出:在反应中的四种物质H2O2、MnO2、H2O、O2中,氧元素的化合价依次为-1、-2、-2、0。
(2)在加热氯酸钾和二氧化锰的混合物制氧气中,二氧化锰作催化剂,起催化作用;
在用过氧化氢和二氧化锰制取氧气的实验中,二氧化锰作催化剂,起催化作用。二氧化锰在两个实验中都起到了加快反应速率的作用。
催化剂的作用是改变化学反应的速率,本身的质量和化学性质在反应并未改变。所以在这两个反应中如不加入二氧化锰反应也可发生,只是速度要比加二氧化锰明显减慢。
(3)解题思路:已知氧气的质量为48g,求需要氯酸钾的质量。可根据用氯酸钾制氧气的反应中二者的质量关系进行计算。具体解题过程:
解:设需要KClO3的质量为x。 设未知量
2KClO3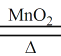 2KCl + 3O2↑ 写出反应的化学方程式
2KCl + 3O2↑ 写出反应的化学方程式
245 96 找出氯酸钾与氧气的质量比
x 48g 标出二者在反应中实际质量比
![]() =
=![]() 根据标出数值列比例式
根据标出数值列比例式
x=122.5g 求解未知量
答:至少需要氯酸钾的质量为122.5g。 写出答案


科目:初中化学 来源: 题型:
【题目】用赤铁矿冶炼生铁的化学原理是__(用化学方程式表示),铁制品在潮湿的空气中生锈是由于铁与空气中的水蒸气和__反应生成铁锈,配制农药“波尔多液”时不用铁桶盛装硫酸铜溶液的原因是_____(用化学方程式表示),常见金属铁、锌、铝的金属活动性顺序是_____.
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】水是人类最宝贵的自然资源.没有水就没有生命,根据你所掌握的有关水的知识回答下列问题:
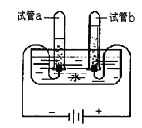
(1)小明利用如图所示的装置探究水的组成.通电一段时间后,两电极上均有气体产生,检查试管b中气体的方法是:________________;该反应的文字表达式为__________________。
(2)某实验小组从护城河中取了水样,观察到:
A.水样呈黄色,有异味
B.水样浑浊,有固体小颗粒.
他们进行了一系列的净化处理,请回答:
①针对A所观察到的现象,为达到净水的目的,可向水样中加入____________。
②生活中既能降低水的硬度,又能杀菌消毒的方法是____________________。③水是生命之源,与生活、生产关系密切.保护水环境、珍爱水资源,是每个公民应尽的责任和义务.为了防止水的污染,下列做法不利于保护水资源的是___________(填序号).
A.抑制水中所有动、植物的生长
B.不任意排放工业废水
C.大量使用化肥、农药
D.生活污水经过净化处理后再排放.
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】类推是一种重要的化学思维方法,下列推理合理的是( )
A. 碱溶液呈碱性,所以呈碱性的溶液一定都是碱溶液
B. 氧化物含有氧元素,所以含氧元素的化合物都是氧化物
C. 中和反应一定生成盐和水,所以生成盐和水的反应一定是中和反应
D. 化学变化中一定有新物质生成,所以有新物质生成的变化一定是化学变化
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】氧气和二氧化碳是两种重要的气体,请根据学过的知识作答:
①工业上用分离液态空气的方法制取氧气,主要是利用了氧气和氮气的________不同。二氧化碳的工业制法与实验室制法都选择了大理石,不仅因为这种原料含有________(填“钙元素”或“碳酸根”),而且来源非常广泛。
②根据所给的仪器回答问题
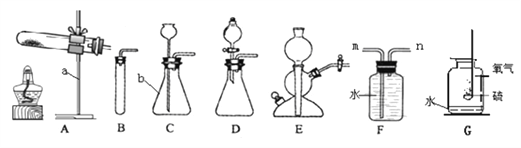
I.写出仪器名称,a ________、b _____________;
II.某同学用A装置制取氧气时发现试管位置太高,不能用外焰加热,该同学应调节下图中的旋钮_______(填“①”或“②”或 “③”)。
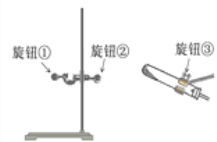
利用改正后的A装置制取氧气,反应的化学方程式:________________,若用装置F收集并粗略测出收集O2体积,还需在_________(填m或n)端接一个量筒以便测出排出的水的体积。G图是硫在氧气中燃烧的实验,观察到的现象是_____________,该反应的化学方程式是_________________________;
III.实验室也能选用D装置作为氧气发生装置,反应的化学方程式是________,为了使反应能保持较平稳地进行,应该采取的措施是___________ ;
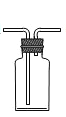
IV.B、C、D、E均可作为实验室制备CO2的发生装置,E装置制备气体的优点是__________,若用C装置制备CO2,操作时一定要___________,形成液封以免气体从长颈漏斗逸出;若用右图装置排空气法收集CO2,请在图中用箭头画出气体进出的方向_________。
V.用足量的石灰石和50克稀盐酸充分完全反应,制得二氧化碳为8.8克。试计算:
50克稀盐酸中所含HCl的物质的量(根据化学方程式列式计算);________________
稀盐酸中HCl的质量分数为___________ 。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】根据质量守恒定律解释下列问题:
(1)镁条在空气中燃烧后,生成的白色粉末的质量比原来镁条的质量增加。 ______
(2)碱式碳酸铜受热分解后,剩余的固体物质的质量比原反应物的质量减轻。 ______
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】材料是时代进步的重要标志。下列有关材料的说法中,错误的是
A.塑料属于有机合成高分子材料
B.棉花属于合成纤维
C.不锈钢属于金属材料
D.开发使用可降解塑料,能有效解决“白色污染”问题
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】
[查阅资料]有些水果、蔬菜对过氧化氢的分解有催化作用。
[实验探究1]探究苹果和土豆对过氧化氢分解是否有催化作用及催化效果:
各量取6ml的过氧化氢溶液,分别倒入1、2、3号三志试管中,取大小、形状基本相同的苹果块和土豆块,分别放入2、3号试管中,并把带火星的木条分别同时伸入三支试管口内,观察现象并记录如下:
试管编号 | 1 | 2 | 3 | |
材料名称 | 无 | 苹果 | 土豆 | |
实验现象 | 反应速率 | 很慢 | 稍快 | 较快 |
产生气泡 | 很少 | 比1中多 | 较多 | |
复燃情况 | 不复燃 | 复燃 | 很快复燃 | |
实验结论 | ||||
[实验探究2]探究浓度对过氧化氢分解速率的影响:
取10ml30%的过氧化氢三份,将其中两份分别稀释为不同浓度的溶液,同时测定收集到100ml氧气所用的时间,(其它实验条件均相同)记录如下:
实验编号 | 1 | 2 | 3 |
过氧化氢溶液浓度 | 5% | 15% | 30% |
所用时间(秒) | 205 | 25 | 3 |
实验结论 | |||
[实验条件3]用上述收集的仪器与不同位置进行反应,其中有一固体能在氧气中燃烧,发出明亮的蓝紫色火焰,生成刺激性气味的气体,该反应的化学方程式为: 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com