
【题目】铁的冶炼与利用是学习和研究化学的重要课题。
Ⅰ.铁的冶炼,竖炉炼铁的工艺流程如图1所示。
(1)“燃烧室”中CH4燃烧的作用是__
(2)写出“还原反应室”中炼铁的一个反应的化学方程式__。
(3)CH4与高温尾气中的CO2或H2O都能反应生成CO和H2,则16g CH4在催化反应室中完全反应后,理论上得到H2的质量(m)范围是__。
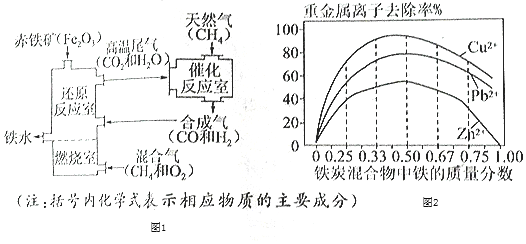
Ⅱ.铁的利用,利用铁炭混合物(铁屑和活性炭的混合物)处理含有Cu(NO3)2,Pb(NO3)2和Zn(NO3)2的铜冶炼废水。在相同条件下,测量总质量相同、铁的质量分数不同的铁炭混合物对水中重金属离子的去除率,实验结果如图2所示。
(1)铁炭混合物中铁的质量分数为100%时,水中的Cu2+、Pb2+能被除去、而Zn2+不能被除去,其原因是__。
(2)铁炭混合物中铁的质量分数为0时,也能除去水中少量的重金属离子,其原因是__。
(3)处理效果最好时,铁炭混合物中的铁的质量分数为__。
【答案】甲烷燃烧放出大量的热,提供冶炼铁需要的高温条件3H2+Fe2O3高温2Fe+3H2O
或3CO+Fe2O3高温2Fe+3CO24g<m<6g铁比铜、铅活泼,但比锌弱,所以铁可以除去铜离子、铅离子,但不能除去锌离子碳单质也能将某些金属离子还原50%
【解析】
I(1)甲烷燃烧放出了大量的热,能够给炼铁提供热量,同时生成了二氧化碳和水,提供了生产合成气的原料,所以“燃烧室”中CH4燃烧的作用是:燃烧产生热量、做生产合成气的原料;
(2)一氧化碳和氧化铁在高温的条件下生成铁和二氧化碳,化学方程式为:3CO+Fe2O3![]() 2Fe+3CO2;
2Fe+3CO2;
(3)甲烷和二氧化碳反应生成氢气的质量为x
CH4+CO2![]() 2CO+2H2
2CO+2H2
16 4
16g x
![]() =
=![]()
x=4g
甲烷和水反应生成氢气的质量为y
CH4+H2O![]() CO+3H2
CO+3H2
16 6
16g y
![]() =
=![]()
y=6g
所以理论上得到H2的质量(m)范围是4g<m<6g;
II(1)铁炭混合物中铁的质量分数为100%时,水中的Cu2+、Pb2+能被除去、而Zn2+不能被除去,原因是:铁的金属活动性排在锌的后面;
(2)铁炭混合物中铁的质量分数为0时,也能除去水中少量的重金属离子,原因是:活性炭对铜离子和铅离子具有吸附性;
(3)由图2中的数据可知,处理效果最好时,铁炭混合物中的铁的质量分数为:50%。


科目:初中化学 来源: 题型:
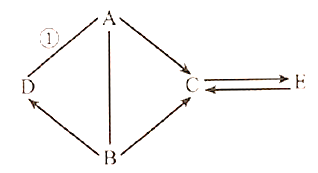
【题目】A、B、C、D、E是初中化学常见的物质。A、C是氧化物,B是胃液中含有的酸,D是通常状况下密度最小的气体,E可用作补钙剂,反应①中有红色物质生成。物质间相互关系如图所示(“一”表示两端物质能发生化学反应,“→”表示物质间的转化关系;部分反应物、生成物和反应条件已略去),请回答。
(1)A的化学式_____
(2)写出C→E的化学方程式_____。
(3)反应①的基本反应类型是_____。
(4)写出B的一种用途_____。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】(6分)用化学方程式表示:
(1)用稀盐酸除去小刀上的铁锈:_____ 。
(2)有非金属单质参加的置换反应: 。
(3)有非金属单质生成的反应: 。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】如图是我国最新研制的大型水面救援飞机,飞机的外壳主要是镁铝合金,飞机中有些零件是由钢铁制成的。
(1)镁铝合金属于_____(填“金属”或“合成”)材料。
(2)生活中常在钢铁制品表面喷漆,不仅美观,而且可有效防止铁与_____接触而生锈。
(3)向一支试管中加入一根生锈的铁钉,然后加入一定量的稀硫酸,写出稀硫酸除铁锈的化学方程式_____。铁锈消失后,将铁钉取出,若要检验试管中的液体是否含有稀硫酸,可选择的试剂是_____(填字母)
A.酚酞溶液 B.Cu
C.CuO D.BaCl2溶液
(4)金属矿物储量有限,而且不能再生。保护金属资源的有效途径,除防止金属腐蚀外,还有_____(写出一条即可)

查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】如图装置可用于多次连续进行氧气的制取和性质的实验。
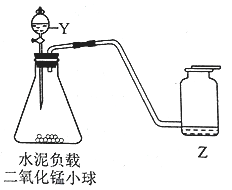
(1)仪器Y的名称是__。
(2)水泥负载二氧化锰小球用于实验时的主要优点是__。该实验中收集氧气的方法是__。
(3)做氧气的性质实验时,实验不同,Z的作用不同。
①铁丝燃烧。Z为水,其作用是__。
②硫粉燃烧。Z为NaOH溶液,其作用是__。
③蜡烛燃烧。Z为__,其作用是验证蜡烛中含有碳元素。
(4)实验时需要1.6g氧气,至少需要加入多少克5%的过氧化氢溶液________。(写出计算过程)
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】实验小组的同学将CO2通入氢氧化钠溶液时,没有观察到明显现象。为了能通过实验现象证明二氧化碳与氢氧化钠确实发生了反应,进行了以下探究。
(提出问题)如何能观察到反应的变化过程?
(查阅资料)
NaOH、Na2CO3在水中的溶解度
温度/℃ | 0 | 10 | 20 | 30 |
NaOH | 42 | 51 | 109 | 119 |
Na2CO3 | 7.1 | 12.2 | 21.8 | 39.7 |
NaOH、Na2CO3在乙醇中的溶解度
温度/℃ | NaOH | Na2CO3 |
18.5~25 | 17.3 | 不溶 |
(进行实验)注:乙醇在实验中只作为溶剂,不参与化学反应。
实验 | 实验装置 | 实验操作 | 实验现象 |
1 |
| 打开止水夹,通入 CO2,气球明显鼓起后关闭止水夹 | 一段时间后,气球明显变瘪 |
2/p> |
| 室温下,向10mL澄清饱和的NaOH溶液中通入适量CO2 | 试管内壁出现白色固体 |
3 |
| ① 室温下,向10mL饱和的NaOH乙醇溶液中缓慢通入适量CO2 | 甲中出现白色沉淀,乙中无明显现象 |
② 滴入稀盐酸 | 甲中有气泡生成,乙中澄清石灰水变浑浊 |
(解释与结论)
(1)二氧化碳与氢氧化钠反应的化学方程式为_______。
(2)实验1中,气球明显变瘪的原因是_______。
(3)实验2中,试管内壁上出现白色固体的原因是_______。
(4)实验3甲中出现白色沉淀的原因是_______。
(5)实验3中操作②的目的是_______。
(反思与评价)
(6)实验1是从________(填“反应物消耗”或“新物质生成”)角度证明化学反应发生。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】若 Na2SO3已部分被氧化变质,某同学为测定 Na2SO3样品的质量分数,设计实验方 案如下:
(方案一)沉淀法 主要操作流程图如下:

请回答下列问题:
(1)流程图中②、③的操作名称分别为②______、③______。
(方案二)测 SO2质量法 主要实验步骤如下:
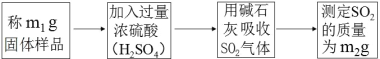
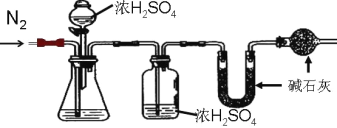
装置如图所示:
(1)该同学设计实验方案的反应原理为_____(用方程式表示)。
(2)装置中干燥管的作用是什么?_____。
(3)反应前和反应后都要吹入氮气的目的是什么?_____。
(4)样品中 Na2SO3 的质量分数的表达式为_____(用 m1、m2 表示)。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】工业上炼铁炼钢和轧制钢材的主要流程如图.

已知生铁的含碳量为 2%--4.3%,钢的含碳量为 0.03%--2%。
(1)反应:①Fe2O3+3CO ![]() 2Fe+3CO2 ,②3C + 2Fe2O3
2Fe+3CO2 ,②3C + 2Fe2O3 ![]() 4Fe + 3CO2↑。属于置换反应的是_________ ,用于高炉炼铁的原理是 _________(填序号)
4Fe + 3CO2↑。属于置换反应的是_________ ,用于高炉炼铁的原理是 _________(填序号)
(2)生铁属于 _________ (填“纯净物”或“混合物”),其熔点比纯铁 _________(填“高”或“低”),铁是由 _________ 构成的物质(填“分子”、“原子”或“离子”)。
(3)炉渣中含有硅酸钙(CaSiO3),其中硅元素的化合价是 _________ 。
(4)将钢锭轧成钢板,属于_________(填“物理变化”或“化学变化”) 。
(5)钢铁制品可能会生锈,写出用稀硫酸除锈反应的化学方程式 _____________________ 。
(6)请用一个化学方程式证明铁的活泼性大于铜 __________________________________ 。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】(题文)如图是水发生变化的微观结构模型。
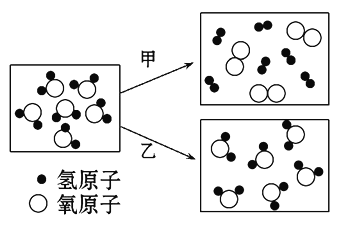
(1)甲、乙两变化中属于物理变化的是__________;从微观结构分析,该变化的特点是__________。
(2)甲、乙两变化中属于化学变化的是____________;从微观结构分析,该变化后物质的化学性质________(填“发生了”或“未发生”)改变,原因是_________________________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com