
【题目】实验小组的同学将CO2通入氢氧化钠溶液时,没有观察到明显现象。为了能通过实验现象证明二氧化碳与氢氧化钠确实发生了反应,进行了以下探究。
(提出问题)如何能观察到反应的变化过程?
(查阅资料)
NaOH、Na2CO3在水中的溶解度
温度/℃ | 0 | 10 | 20 | 30 |
NaOH | 42 | 51 | 109 | 119 |
Na2CO3 | 7.1 | 12.2 | 21.8 | 39.7 |
NaOH、Na2CO3在乙醇中的溶解度
温度/℃ | NaOH | Na2CO3 |
18.5~25 | 17.3 | 不溶 |
(进行实验)注:乙醇在实验中只作为溶剂,不参与化学反应。
实验 | 实验装置 | 实验操作 | 实验现象 |
1 |
| 打开止水夹,通入 CO2,气球明显鼓起后关闭止水夹 | 一段时间后,气球明显变瘪 |
2/p> |
| 室温下,向10mL澄清饱和的NaOH溶液中通入适量CO2 | 试管内壁出现白色固体 |
3 |
| ① 室温下,向10mL饱和的NaOH乙醇溶液中缓慢通入适量CO2 | 甲中出现白色沉淀,乙中无明显现象 |
② 滴入稀盐酸 | 甲中有气泡生成,乙中澄清石灰水变浑浊 |
(解释与结论)
(1)二氧化碳与氢氧化钠反应的化学方程式为_______。
(2)实验1中,气球明显变瘪的原因是_______。
(3)实验2中,试管内壁上出现白色固体的原因是_______。
(4)实验3甲中出现白色沉淀的原因是_______。
(5)实验3中操作②的目的是_______。
(反思与评价)
(6)实验1是从________(填“反应物消耗”或“新物质生成”)角度证明化学反应发生。
【答案】CO2 + 2NaOH = Na2CO3 + H2OCO2与NaOH反应,使压强变小生成碳酸钠的质量大于氢氧化钠质量,碳酸钠的溶解度小于氢氧化钠二氧化碳与氢氧化钠反应生成碳酸钠,碳酸钠不溶于乙醇证明二氧化碳与氢氧化钠反应生成了碳酸钠反应物消耗
【解析】
(1)二氧化碳与氢氧化钠反应生成碳酸钠和水,化学方程式为CO2 + 2NaOH = Na2CO3 + H2O;(2)实验1中,气球明显变瘪的原因是CO2与NaOH反应,使压强变小;(3)室温下,向澄清饱和的NaOH溶液中通入适量CO2,生成碳酸钠的质量大于氢氧化钠质量,由于碳酸钠的溶解度小于氢氧化钠,所以会有白色的碳酸钠固体析出;(4)室温下,向饱和的NaOH乙醇溶液中缓慢通入适量CO2,二氧化碳与氢氧化钠反应生成不溶于酒精的碳酸钠,所以 出现白色沉淀;(5)甲中有气泡生成,乙中澄清石灰水变浑浊说明甲中滴入稀盐酸后有二氧化碳生成,证明二氧化碳与氢氧化钠反应生成了碳酸钠;(6)实验1通过气球明显变瘪,说明二氧化碳被消耗,是从反应物消耗角度证明化学反应发生。


科目:初中化学 来源: 题型:
【题目】中国高铁制造已处于世界先进水平。请回答下列问题。
(1)田老师乘高铁外出学习,在列车上购买了一盒快餐,其中有米饭、酱牛肉、炒白菜,牛肉中富含的营养素是_____。快餐盒使用的是可降解塑料,这样可以减轻的环境问题是“_____”。
(2)高铁水箱中装有生活用水,在净水过程中利用了活性炭的_____性。请写出节约用水的一种做法_____
(3)越来越多的新型材料应用于高铁建设,其中合金属于_____(填“金属”或“合成”)材料。
(4)合金较其组分金属具有一定的优良性能。用钒钢合金制造高铁的钢轨,主要利用其_____的性能。

查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】探究空气中氧气含量的实验(如图所示),回答下列问题:
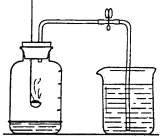
(1)甲同学点燃燃烧匙中的红磷,观察到红磷燃烧,放热,并产生大量的_________,该反应的文字表达式___________。冷却后,打开弹簧夹,出现___________的现象。
(2)乙同学用上述实验装置测定的结果是:空气中氧气含量与正常值有较明显的偏小,其原因可能是__________________。(要求答出一种)
(3)实验结束后,集气瓶中剩余的气体主要是氮气,且瓶内水面上升到一定高度后不再上升了,由此分析说明,氮气具有的一条性质:________________________________。
(4)丙同学探究能否用镁条代替红磷,将镁条点燃后迅速伸入盛有氮气的集气瓶中,发现镁条剧烈燃烧,发出白光,放热,产生一种叫氮化镁的粉末。请写出镁在氮气中燃烧反应的文字表达式________________,分析后认为________(填“能”或“不能”)代替红磷,原因是_____________。若用镁代替红磷实验,进入瓶中水的体积会________(填 > 或< 或 =)瓶内空气体积的1/5.
(5)下列有关测定空气中氧气含量实验说法正确的是___________(填字母).
A.燃烧匙中的红磷越多,水位上升越高
B.本实验可以证明空气含有N2、O2、CO2和稀有气体.
C.选用红磷是因为只能与空气中的氧气反应,且生成物为固体
D.集气瓶中先装入少量水是为了吸收生成物,防止污染空气
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】2016年11月,“冰箭”冲天,中国挺进大火箭时代。

(1)氢气的利用。火箭采用液氢、液氧作为推进剂,其内部温度极低,因此称为“冰箭”,氢气是__(填序号)。
a.常规能源 b.绿色能源 c.不可再生能源
(2)氢气的制取。利用太阳能分解水制H2与电解水制H2相比,其优点是__。
(3)氢气的储存。在常温和250kPa下,镧镍合金(LaNi5)吸收氢气生成LaNi5H7,写出该反应的化学方程式__。
(4)氢燃料电池是将化学能直接转化为__且能量转化效率高达约80%;与化石燃料相比,氢能源的优点是:①原料来源广,②产物无污染,③__。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】铁的冶炼与利用是学习和研究化学的重要课题。
Ⅰ.铁的冶炼,竖炉炼铁的工艺流程如图1所示。
(1)“燃烧室”中CH4燃烧的作用是__
(2)写出“还原反应室”中炼铁的一个反应的化学方程式__。
(3)CH4与高温尾气中的CO2或H2O都能反应生成CO和H2,则16g CH4在催化反应室中完全反应后,理论上得到H2的质量(m)范围是__。
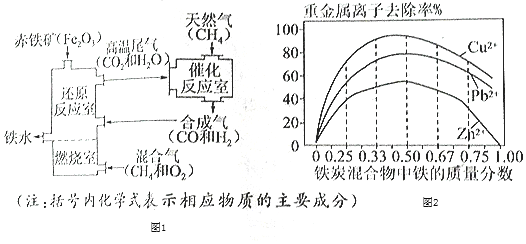
Ⅱ.铁的利用,利用铁炭混合物(铁屑和活性炭的混合物)处理含有Cu(NO3)2,Pb(NO3)2和Zn(NO3)2的铜冶炼废水。在相同条件下,测量总质量相同、铁的质量分数不同的铁炭混合物对水中重金属离子的去除率,实验结果如图2所示。
(1)铁炭混合物中铁的质量分数为100%时,水中的Cu2+、Pb2+能被除去、而Zn2+不能被除去,其原因是__。
(2)铁炭混合物中铁的质量分数为0时,也能除去水中少量的重金属离子,其原因是__。
(3)处理效果最好时,铁炭混合物中的铁的质量分数为__。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】物质可以根据其组成和性质等进行如下分类。

(1)上图所示的分类方法属于___________(填序号)
A.交叉分类法B.树状分类法
(2)以H、O、S、N、K、Cu六种元素中任意两种、三种或多种元素组成合适的常见化合物,可以有酸、碱、盐、氧化物等。
①从上述物质中选出一种含H、O、N元素的盐,写出其在水溶液中离子的符号_____。
②从上述物质中元素最高价含氧酸及碱(含Cu元素)中各选出一种能相互反应的物质,并写出其反应的化学方程式:_____。
(3)下列4组物质均有一种物质的类别与其他3种不同,且这四种物质相互作用可生成一种新物质——碱式碳酸铜,化学式为Cu2(OH)2CO3。
A.CaO、Na2O、CO2、CuO B.H2、C、P、Cu
C.O2、Fe、Cu、Zn D.HCl、H2O、H2SO4、HNO3
以上四组物质中与其他物质不同的物质依次是(填化学式):
A._____;B.______;C.______;D.______。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】
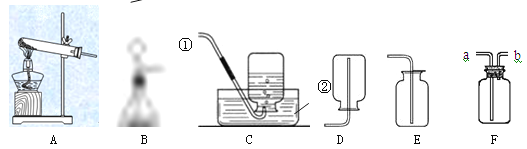
(1)写出标号仪器的名称:① ;② 。
(2)实验室用高锰酸钾制取氧气,反应的符号表达式为 ,应选用的发生装置是 (填字母,下同),以高锰酸钾为试剂利用此装置制取氧气时,还要做的改进是 ,其作用是 。用E装置收集氧气的依据是 ,检验氧气是否集满的方法是 。
用F装置收集氧气时,气体应从 (填“a”或“b”)管通入。
(3)某同学想用过氧化氢溶液和二氧化锰混合制取较纯净的氧气,他应选用的装置组合是 。由于该同学动作太慢,氧气还没有收集满,容器内的反应就停止了,若想集满这瓶气体,在不拆卸装置的前提下,请你帮他想两种方法:
① ;
② 。
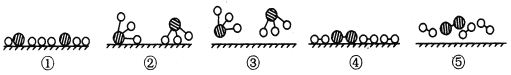
(4)通过查阅资料得知:氨气(NH3)是一种密度比空气小且极易溶于水的气体,其水溶液称为氨水。实验室用加热氯化铵和氢氧化钙的固体混合物的方法来制取氨气,你认为应选择的发生装置是 ,收集装置是 。1909年化学家哈伯在实验室首次合成了氨。2007年化学家格哈德·埃特尔在哈伯研究所证实了氢气与氮气在固体催化剂表面合成氨的过程,获得诺贝尔化学奖。将氢气和氮气在高温、高压和催化剂的条件下合成氨(NH3)。反应的化学方程式为: N2 + 3H2 ======== 2NH3。用![]() 、
、![]() 、
、![]() 分别表示N2、H2、NH3。观察下图,写出符合在催化剂表面合成氨反应过程的顺序: (将下面五张图按反应过程顺序用序号排列)。
分别表示N2、H2、NH3。观察下图,写出符合在催化剂表面合成氨反应过程的顺序: (将下面五张图按反应过程顺序用序号排列)。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】我国自行研究的大型客机C919于2015年5月成功试飞。大飞机使用了各种材料:
①铝锂合金、②玻璃钢、③钛合金、④橡胶等
(1)上述材料中,属于复合材料的是_____(填序号)。
(2)选用铝锂合金做飞机机身而不选用纯铝,主要原因是_________________________;
(3)飞机上镀铬铁制品能防锈蚀,防锈原理是________________________。
(4)如图是元素周期表中铝元素的有关信息及铝原子的结构示意图。铝元素位于元素周期表中的第_________周期,在空气中,铝的表面易形成一层保护膜薄膜,反应的化学方程式为_______________。
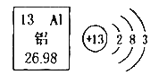
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】英国科学家法拉第曾为少年儿童做过一个有趣的“母子火焰”实验,如图所示。回答下列有关问题。
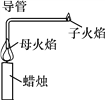
(1)子火焰的可燃物是________,蜡烛能产生母子火焰这一现象是由组成蜡烛的物质的重要物理性质决定的,该物理性质是______________________________。
(2)该实验成功的关键是导气管不宜太长,且导气管的起端必须插在蜡烛母火焰的中心部位,原因是:
①_______________________________________________;
②_______________________________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com