
【题目】下列实验方案设计正确的是
选项 | 实验目的 | 实验方案 |
A | 20℃时,配制硝酸钾饱和溶液100g(已知:20℃时,硝酸钾的溶解度为31.6g) | 20℃时,将31.6g的硝酸钾固体溶于68.4mL水中 |
B | 检验久置空气中的氢氧化钠固体是否变质 | 取样加水溶解后滴加酚酞试液,观察溶液是否变红 |
C | 除去铁钉表面的铁锈 | 取样加过量的稀硫酸,长时间浸泡 |
D | 鉴别化肥KNO3和NH4C1 | 取样与熟石灰混合研磨,闻气味 |
A.AB.BC.CD.D
【答案】D
【解析】
A、已知20℃时,硝酸钾的溶解度为31.6g,20℃时,配制硝酸钾饱和溶液100g,需要硝酸钾固体的质量为![]() ,需要加水的质量为100g-24g=76g,因此20℃时,将31.6g的硝酸钾固体溶于68.4mL水中不能配制该温度下100g的硝酸钾饱和溶液,A选项实验方案设计的不正确,不符合题意;
,需要加水的质量为100g-24g=76g,因此20℃时,将31.6g的硝酸钾固体溶于68.4mL水中不能配制该温度下100g的硝酸钾饱和溶液,A选项实验方案设计的不正确,不符合题意;
B、氢氧化钠与二氧化碳碳酸反应生成碳酸钠和水,久置空气中的氢氧化钠固体变质会含有碳酸钠,碳酸钠、氢氧化钠的溶液均呈碱性,都能使无色酚酞试剂变红,要检验久置空气中的氢氧化钠固体是否变质,通过取样加水溶解后滴加酚酞试液,观察溶液是否变红的实验操作无法达到实验目的,B选项实验方案设计的不正确,不符合题意;
C、铁锈的主要成分是三氧化二铁,三氧化二铁与稀硫酸反应生成硫酸亚铁和水,除去铁钉表面的铁锈,取样加过量的稀硫酸,长时间浸泡,三氧化二铁反应完后,铁会继续与稀硫酸反应生成硫酸亚铁和氢气,会腐蚀铁,C选项实验方案设计的不正确,不符合题意;
D、硝酸钾与氢氧化钙不反应,氯化铵与氢氧化钙在研磨时反应生成氯化钙、氨气和水,会产生有刺激性气味的气体,可以通过与熟石灰混合研磨闻气味的方案来鉴别化肥KNO3和NH4C1,D选项实验方案设计正确,符合题意。故选D。


 孟建平错题本系列答案
孟建平错题本系列答案 超能学典应用题题卡系列答案
超能学典应用题题卡系列答案科目:初中化学 来源: 题型:
【题目】有一包白色固体,可能含氯化钠、碳酸钠、硫酸钠、氢氧化钠、氢氧化钡中的一种或几种。 为了研究该混合物的成分,某同学按下列流程进行了实验( 各步均恰好完全反应);
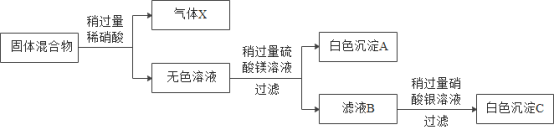
回答下列问题:
(1)气体X的化学式____,白色沉淀C的化学式__。
(2)生成白色沉淀A的化学方程式为____。
(3)通过流程图分析原固体中一定不含有的物质是____。
(4)为探究固体混合物中是否含有氢氧化钠及质量,某研究性学习小组取固体混合物样品40.0g,按上述流程图进行实验,结果产生白色沉淀A23.3g,白色沉淀C28.7g,气体X2.2g。通过以上数据计算确定固体混合物中___ (填字母序号)。
A 含有氢氧化钠
B 不含氢氧化钠
C 氢氧化钠为4.0g
D 氢氧化钠为5.9g
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】如图是自然界中碳、氧循环简图(X为H2CO3,Y为C6H12O6)。下列说法不正确的是

A. 图一中的转化1是酸雨形成的主要原因
B. 图二中可实现有机物与无机物的相互转化
C. 绿色植物通过光合作用,将太阳能转化成化学能
D. 碳循环和氧循环有利于维持大气中氧气和二氧化碳含量的相对稳定
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】已知A、D均为无色无味的气体,B、C为黑色粉末,E为红色单质。A、B、C、D、E、F六种物质之间的转化关系如图下所示。请回答:

(1)B、D的化学式分别为_______、______;
(2)反应②、③的化学方程式分别为_____、_____;
(3)①③这两个反应说明A和C具有相同的化学性质为_____填“可燃性”或“稳定性”或“还原性”或“氧化性”)。
(4)图中的反应中属于置换反应的是_______。(填序号)
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】实验室制取气体时常要考虑下列问题:
(1)选择合理的制取装置。
用如下图所示装置制取气体,请回答下列问题。

①仪器a的名称是__。
②选用A加热KMnO4制O2,装置需要改进的地方是__,反应的化学方程式为__。
③实验室用Zn和稀硫酸制取H2的化学方程式为__。
④实验室可用亚硝酸钠(NaNO2)和NH4Cl的饱和溶液加热法制备N2,应选择的发生装置和收集装置的组合是__(写出一种组合,填序号)。
(2)检验、除杂和尾气处理。
①通过饱和NaHCO3溶液洗气,可除去CO2中的HCl。洗气时化学反应方程式为__。
②实验室制备下列气体时,一般需要进行尾气处理的是__(填序号)。
a H2 b CO c CO2 d SO2
(3)反应装置的改进和反应条件的探究。
某实验小组为了探究影响H2O2分解制取氧气快慢的因素,进行了下列实验:
实验序号 | H2O2溶液的质量分数/% | H2O2溶液的体积/ml | 温度/℃ | MnO2粉末的用量/g | 收集气体的体积/ml | 收集气体所需的时间/s |
A | 5 | 1 | 20 | 0.1 | 4 | a |
B | 15 | 1 | 20 | 0.1 | 4 | b |
C | 30 | 5 | 35 | 0.1 | 4 | c |
D | 30 | 5 | 55 | 0.1 | 4 | d |
①欲探究温度对H2O2分解快慢的影响,应该选择的对照实验组是__(填实验序号)。
②该小组利用如下左图所示装置探究MnO2质量对H2O2分解快慢的影响:在三份8.0ml3%的H2O2溶液中分别加入0.03g、0.06g和0.08gMnO2粉末,获得实验数据如下右图所示(温度变化忽略不计,产生氧气的体积与装置内的压强成正比)。通过对曲线图的分析,将推理得出的结论填写在下列空白中。

结论I:在其他条件不变的情况下,所用MnO2质量越大,H2O2的分解速率__。
结论II:在其他条件不变的情况下,所用MnO2质量越大,生成氧气的总量__。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】“84”消毒液具有漂白、杀菌、消毒的功效。在新冠肺炎预防措施中使用较为广泛。某化学兴趣小组对一瓶敞口久置的“84”消毒液的成分产生兴趣,在老师的指导下,展开探究。
(査阅资料)“84”消毒液的主要成分是次氯酸钠(NaClO)和氯化钠。NaClO为有效成分,且有腐蚀性并易与空气中的CO2反应(2NaC1O+CO2+H2O=2HC1O+Na2CO3)。NaClO溶液、HC1O都具有漂白、杀菌、消毒功效。HC1O不稳定,受热或光照条件下会发生分解生成氯化氢和氧气。
(分析讨论)小组同学经过讨论,认为该消毒液中的溶质一定有______,可能还有NaClO、Na2CO3、HClO中的一种或多种。
(实验探究)
实验操作 | 实验现象 | 实验结论 |
I.向装入有色布条的试管中加入适量该消毒液 | 有色布条长时间不褪色 | 消毒液中不含的溶质____ |
П.另取少量该消毒液于试管中,滴入足量氯化钡溶液,静置 | 产生白色沉淀 | 消毒液中含有的溶质___ |
(交流反思)
(1)生活中“84”消毒液贮藏时应注意_____。一般不用“84”消毒液对蔬菜、水果进行消毒,其原因可能是_____。
(2)“84”消毒液与洁厕灵(主要成分是盐酸)混合使用易产生一种有毒气体,反应的化学方程式为NaClO+2HC1=NaCl+X↑+H2O,则X的化学式为______。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】在5mL氢氧化钠溶液中滴加2滴酚酞试液,溶液呈______色,再加入5mL稀盐酸,得到无色溶液,则无色溶液一定是_________。
Ⅰ pH≤7
Ⅱ pH=7
Ⅲ pH <7
ⅣpH>7
将无色溶液蒸发至干,看到的现象是____________。
若将40克10%氢氧化钠溶液和足量稀盐酸反应,计算生成氯化钠的物质的量。(根据化学方程式计算)_______
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】为了达到收旧利废节能减排的目的,从含有金属镁、铁、铜的粉末中,分离和提取出重要化工原料MgSO4和有关金属,实验过程如下:

(1)操作①中被磁铁吸引的金属A是________________;
(2)操作a的名称是________________;
(3)写出步骤②所涉及的化学反应方程式:___________________________;
(4)实验步骤②中除了加入稀硫酸外,还可选用下列试剂_________(填标号)。
a 硫酸铜溶液 b 氯化钠溶液 c 硝酸银溶液
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com