
����Ŀ�����Ʊ������ǿ�ѧ̽���г��õķ�������ѧ��Ӧ�Ŀ���������������йأ����¶ȡ�ѹǿ���������������������ء�����ʵ����Ƶ�Ŀ����̽����ѧ��Ӧ��������������Ĺ�ϵ��
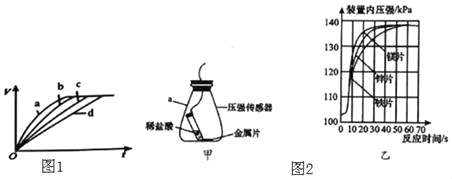
�������ķݵ����������ֱ���������������з�Ӧ��ͼ1Ϊ���ŷ�Ӧʱ��ı仯�����������V�Ĺ�ϵ���ߡ�����ʵ�������ֱ��ǣ�
a.50�桢���� b.30�桢���� c.30�桢��˿ d.20�桢��˿
��1����д���������ᷴӦ�Ļ�ѧ����ʽ��_____���÷�Ӧ����ʱ��ų�������
��2��ͨ��ʵ��a��b�Աȣ��ó��Ľ�����_____����Ҫ�ȽϽ������ı�����Է�Ӧ������Ӱ�죬Ӧѡ���ʵ�������_____��ʵ���й۲쵽�������塰����ֱ�����������͡���족��ԭ����_____��
��3������ʱ��������������п��þ���ֽ���Ƭ�ֱ���������ᷴӦ��ͼ2�У���ͼΪʵ�鷢��װ�ã���ͼΪ��õIJ�������������ͼ��ѹǿԽ��ʾ������������Խ�ࣩ��
����ʵ���У�����Ϊ����Ҫ���Ƶı�����_____��
��������ͼ���ó���Ӧ�����������H2����Ĺ�ϵ��_____��
��4����������þƬ�����ᷴӦ����ò���H2��ʵ��ֵ������ֵƫ����������ܵ�ԭ��д��һ�����ɣ���
_____��
���𰸡�Fe+2HCl��FeCl2+H2���� ��ͬ�����£��¶�Խ�ߣ��������ᷴӦ����Խ�죻 bd ����ϡ���ᷴӦ���ȣ���Ӧ���ʼӿ� �������Ŀ�����С���������IJ�ͬ�����ֱ�����ͬ�����ͬ������������ͬ�����ַ�Ӧ����������������� ��Ӧ���ȣ�ʹ�������ͣ� �����л������Ȼ������塣
��������
��1����������ϡ���ᷴӦ�����Ȼ��������������з�����
��2�����ÿ��Ʊ������Բ�ͬС���ʵ����з����Աȣ��ó���ȷ���ۣ��������ŷ�Ӧ�Ľ��У������Ũ�ȱ�С����Ӧ���ʱ������н��
��3�������ݿ��Ʊ��������з���������ϱ�����Ϣ��ͼ����Ϣ���������IJ�ͬ�����ֱ�����ͬ�����ͬ������������ͬ�����ַ�Ӧ����������������Ƚ��з������
��4�����Ƿ�Ӧ���ȣ�ʹ�������ͣ������л������Ȼ������壬���з�����
��1����������ϡ���ᷴӦ�����Ȼ���������������Ӧ�Ļ�ѧ����ʽΪ��Fe+2HCl��FeCl2+H2����
��2��ab����ʵ��������������ͬ��Ψ���¶Ȳ�ͬ���ɴ˵ó����ۣ���ͬ�����£��¶�Խ�ߣ��������ᷴӦ����Խ�죻bd����ʵ��������������ͬ��Ψ�н������ı������ͬ�������ڱȽϽ������ı�����Է�Ӧ������Ӱ�죻����ϡ���ᷴӦ���ȣ���Ӧ���ʼӿ죻
��3���ٴ˴�Ӧ���ƽ��������Ĵ�С��ͬ��
����ͼ�ң���ó��ķ�Ӧ����������ɵ���������Ĺ�ϵ�������IJ�ͬ�����ֱ�����ͬ�����ͬ������������ͬ�����ַ�Ӧ����������������ȣ�
(4)���ܵ�ԭ���У��ٷ�Ӧ���ȣ�ʹ�������͡��������л������Ȼ������塣



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij��ѧ��ȤС������ʦ�İ����¶Լ��ֳ���������Ʒ�����Ľ�����������ص�̽�����
��������⣩(1)����������ٻƽ�(2)����ȷ���ٵĽ�����ԣ�
���������ϣ�(1)�ٻƽ�ͨ���ǻ�ͭ(Cu-Zn�Ͻ�)��
(2)��(Pd)������ɫ�н��������������Ʒ��
��ʵ��ҩƷ���١�Ǧ(Pt)��ϡ���ᡢ��������Һ���Ȼ�ڕ(PdC12)��Һ
��ʵ��̽����
(1)����ƽ���Ʒ�����
ȡ�ƽ���Ʒ���Թ��еμ�ϡ�����۲쵽�ƽ���Ʒ���������ݲ�����������______��˵������ƷΪ______(ѡ����������������)�ƽ�
(2)̽��ڕ�Ľ������
���������ͬѧ�Dz���ڕ�Ļ�Կ���������Ǧ�������������������ҩƷ��������ʵ�飺
ʵ�鲽�� | ʵ������ | ʵ����� |
���ٽ�����������Һ�� | ______ | �ٵĻ�Ա����� |
��Ǧ�����Ȼ�ڕ��Һ�� | ���������� | �ٵĻ�Ա�Ǧ ______ |
�����ó����ۣ��١�����Ǧ�Ľ��������ǿ������˳��Ϊ______��
(3)��ʢ���������������������Һ���ձ��м���һ������п�۷�Ӧֹͣ������������м���ϡ���������ݲ�����Һ��һ������______��������һ����______��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��̼��̼�Ļ�������ת����ϵ�ɱ�ʾΪ��
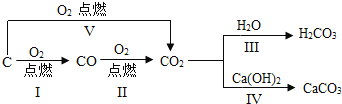
��1����Ӧ����ʵ�����п����ڼ����������______��
��2����д��ָ����Ӧ�Ļ�ѧ����ʽ������______������______��
��3���ɷ�Ӧ���뷴Ӧ���ȽϿ��Ի�ȡ�Ľ����ǣ���ѧ��Ӧ�IJ�����______�йأ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������������������Ӧ�ù㷺��
(1)�����ˮ�ܲ���������Ŀǰ�������Ϲܺ����Ͻ������Ϲܣ�������ˮһ����ͭ�ܡ����йܲ��У����ڽ������ϵ���______![]() ����ĸ���
����ĸ���![]() ��
��

(2)���������г��õĽ�������ͼ��ij��ȡůƬ�����װ��ͼƬ���á�ȡůƬ���з��ȼ���Ҫ�ɷ������ۡ�����̿���Ȼ��ơ�ˮ�ȣ��䷢��������������ʱ�ᷢ�ȡ�

![]() ���ȼ���Ӵ������Żᷢ�ȣ�ԭ������Ҫ��______�����ʹ�ͬ���òŻ����⡣
���ȼ���Ӵ������Żᷢ�ȣ�ԭ������Ҫ��______�����ʹ�ͬ���òŻ����⡣
![]() �Ʋⷢ�ȼ��ɷ����Ȼ��Ƶ�����______�����������Ƭ����������Ȼ�ͭ�Ļ����Һ�У����ܷ������û���Ӧ�Ļ�ѧ����ʽ��______��
�Ʋⷢ�ȼ��ɷ����Ȼ��Ƶ�����______�����������Ƭ����������Ȼ�ͭ�Ļ����Һ�У����ܷ������û���Ӧ�Ļ�ѧ����ʽ��______��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���ɷ�����������ԭ��������ѹ����CO2�����ɷۣ���Ҫ�ɷ���̼�����ƺ�������Σ��������й�˵����ȷ���ǣ�������
A. ���ʱҪ�����������Ϸ�����
B. ���ʱ�����˿�ȼ����Ż��
C. ��NH4��3PO4��N��H��O��ԭ�Ӹ�����Ϊ1��4��4
D. NaHCO3����Ԫ�ص�������������ʽΪ![]() ��100%
��100%
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������صIJ����ܽ�����ݼ��±���
�¶ȣ��棩 | 10 | 20 | 40 | 60 |
�ܽ�ȣ�g/100g ˮ�� | 20.9 | 31.6 | 63.9 | 110 |
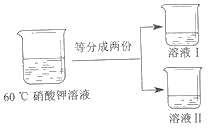
��20��ʱ����ȡ 10.0 ������ع�����뵽 40 ��ˮ�У���_____��д���������ƣ����裬����ܽ��õ�_____��ѡ��������������������������Һ��
�ڽ�������Һ������ 60�棬������Һ��������������Ϊ_____��
�۽� 60����������Һ������ͼ��ʾ������
����Һ I ���£���ʼ��������ؾ�����¶Ƚ���_____�棨ѡ����֮�䡣
A. 40-60 B. 20-40 C. 10-20 D. ���� 10
Ϊ�õ� 60��ʱ����ر�����Һ������Һ II �������� 15 ��ˮ��������ò����ܷ�ﵽʵ��Ŀ�IJ�˵������_____��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ͼ��ʾΪʵ�����г��������Ʊ�������������ռ��ͽ���ʵ��̽���IJ���������ij��ѧС���ͬѧ��������������и���ѧʵ�顣������ĿҪ����ش��������⣺
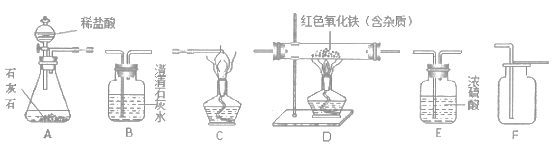
��1����ʵ�������Ʊ����ռ�����Ķ�����̼���塣
����ѡ����������˳��Ϊ��A��_____��_____����д���������ĸ����
������A�У�������Ӧ�Ļ�ѧ����ʽΪ_____��
�����й��ڶ�����̼��������ȷ����_____����A��B��C��D֮һ����
A��������̼��һ���ж������壬���ڴ�����Ⱦ��
B��������̼ͨ����ɫʯ����Һ�У���۲쵽��ɫʯ����Һ����
C��������̼�Ĺ����������ɱ������ɱ����������������˹�����
D��������̼�����ĸ���ԭ���Ƕ�����̼���ܶȱȿ�����
��2������һ����̼����ⶨij������������Ʒ�Ĵ��ȣ����ʲ���Ӧ��������֤��Ӧ����������������ʡ���ѡ����������˳��Ϊ��CO������D��B��C��
������B�����������_____��
������C��������_____��
��д��D�з�����Ӧ�Ļ�ѧ����ʽ_____��
�ܷ�ӦǰD�й����������_____��������������С������������֮һ����Ӧ��D�й������������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ѧϰ������̼����ʱ����������̼����ͨ����ɫʯ����Һ�У��۲쵽��ɫʯ����Һ��죬������ij��ѧ��ȤС�����ɫʯ����Һ���ɫԭ���ʵ��̽����
��֪ʶ������Ũ�����������ˮ�֡�
��������⣩��ʲô����ʹ��ɫʯ����ɫ�ģ�
��������裩�ٶ�����̼ʹ��ɫʯ���Ϊ��ɫ����ˮʹ��ɫʯ��Ϊ��ɫ���۶�����̼��ˮ��Ӧ���ɵ�̼��ʹ��ɫʯ���Ϊ��ɫ��
�����ʵ�飩
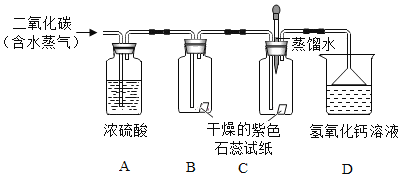
��������ǵ�ʵ�飬�ش���������
��1��װ��A��������_____��
��2��ʵ������У�B����ֽ����ɫû�б仯����˵��_____��
��3��Cװ����δͨ�������̼֮ǰ������ɫʯ����ֽ�ϵ�������ˮ��δ����ֽ��ɫ�仯��˵������_____������������ţ���ͬ����֮��ͨ�������̼��������ֽ��죬�ɴ�˵������_____������ԭ����_____���û�ѧ����ʽ��գ���
��4��D�з�Ӧ�Ļ�ѧ����ʽΪ_____��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��Ϊ�ⶨ��ͭ��Cu��Zn�Ͻ���ͭ������������ijͬѧ��20g�úϽ���뵽ʢ��100g������ձ��У�п������ǡ����ȫ��Ӧ����Ӧֹͣ����ձ���ʣ�����������Ϊ119.8g��
��1����������������Ϊ_____��
��2������Ͻ���п������_____����д��������̣�
��3������Ͻ���ͭ����������_____����д��������̣���ȷ��0.1%����
��4���������������ʵ���������_____����д��������̣���ȷ��0.1%����
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com