
【题目】某化学兴趣小组在老师的帮助下对几种常见金属饰品所含的金属进行了相关的探究活动。
(提出问题)(1)怎样鉴别真假黄金?(2)怎样确定钯的金属活动性?
(查阅资料)(1)假黄金通常是黄铜(Cu-Zn合金);
(2)钯(Pd)呈银白色有金属光泽可用作饰品。
(实验药品)钯、铅(Pt)、稀盐酸、硝酸银溶液和氯化跁(PdC12)溶液
(实验探究)
(1)鉴别黄金样品的真假
取黄金样品于试管中滴加稀盐酸后观察到黄金样品表面有气泡产生该气体是______,说明此样品为______(选填“真”或“假”)黄金。
(2)探究跁的金属活动性
依据生活经验同学们猜想跁的活动性可能与银和铅相近于是他们利用上述药品进行如下实验:
实验步骤 | 实验现象 | 实验结论 |
把钯浸入硝酸银溶液中 | ______ | 钯的活动性比银弱 |
把铅浸入氯化跁溶液中 | 无明显现象 | 钯的活动性比铅 ______ |
初步得出结论:钯、银、铅的金属活动性由强到弱的顺序为______。
(3)向盛有硝酸亚铁和硝酸银混合液的烧杯中加入一定量的锌粉反应停止后过滤向滤渣中加入稀盐酸有气泡产生滤液中一定含有______,滤渣中一定有______。
【答案】氢气 假 无明显现象 弱 银、钯、铂 硝酸银、硝酸锌 银和铁
【解析】
[实验探究] (1)取黄金样品于试管中,滴加稀盐酸后,观察黄金样品表面有气泡产生,该气体是锌和稀盐酸反应生成的氢气,说明此样品为假黄金;
(2)在金属活动性顺序中,活动性强的金属可以把活动性弱的金属从它的盐溶液中置换出来,根据结论钯的活动性比银弱,因此把钯浸入硝酸银溶液中,不会发生置换反应,表现为无现象;把铂浸入氯化钯溶液中无明显现象,说明铂的活动性比钯弱,即钯的活动性比铂强;因此三种金属的活动性顺序为:银![]() 钯
钯![]() 铂或铂
铂或铂![]() 钯
钯![]() 银;
银;
![]() 向滤渣中加入稀盐酸,有气泡产生,说明滤渣中一定含有铁,即硝酸银完全反应,滤液中不含有银离子,一定含有锌和硝酸银、硝酸亚铁反应生成的锌离子,不一定含有亚铁离子,这是因为如果硝酸亚铁完全反应时,则滤液中不含有亚铁离子,滤液中一定含有硝酸银、硝酸锌;滤渣中一定含有银和铁,可能含有锌。
向滤渣中加入稀盐酸,有气泡产生,说明滤渣中一定含有铁,即硝酸银完全反应,滤液中不含有银离子,一定含有锌和硝酸银、硝酸亚铁反应生成的锌离子,不一定含有亚铁离子,这是因为如果硝酸亚铁完全反应时,则滤液中不含有亚铁离子,滤液中一定含有硝酸银、硝酸锌;滤渣中一定含有银和铁,可能含有锌。


科目:初中化学 来源: 题型:
【题目】下列是与铁的性质有关的部分实验图,请回答下列问题。

(1)A中细铁丝燃烧生成黑色固体物质的化学式是_________________。
(2)B中铁钉最易生锈的部位是__________(填“a”、“b”或“c”)。
(3)C试管内发生反应的化学方程式是_______________________。
(4)D中反应一段时间后,试管内溶液质量与反应前相比____________(填增大、不变或减小)。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】纯净物甲是一种可再生绿色能源。在一定条件下,一定质量的甲与48g乙充分反应,反应的微观示意图如下。当乙反应完全时,生成44g丙和27g丁。
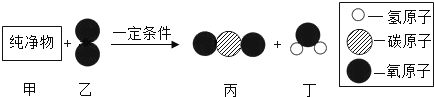
下列有关说法错误的有( )个
①参加反应的甲物质的质量为23g ②反应生成丙和丁的化学计量数比为2:3
③甲物质中碳元素和氢元素的质量比为4:1 ④参加反应的甲与丙的质量比为48:44
⑤甲物质中一定含有碳元素和氢元素,可能含有氧元素
A. 1 B. 2 C. 3 D. 4
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】在一定条件下,在一个密闭容器内发生某反应,测得反应前后各物质的质量如下表所示,下列说法错误的是( )
物 质 | 氧 气 | 二氧化碳 | 水蒸气 | W |
反应前质量/g | 50 | 1 | 1 | 23 |
反应后质量/g | 2 | 45 | 28 | x |
A. 根据质量守恒定律,x的值应为0 B. 反应后的生成物是二氧化碳和水
C. 物质W含碳、氢、氧三种元素 D. 物质W只含碳和氢两种元素
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】除去下列物质中混有的少量杂质![]() 括号内为杂质
括号内为杂质![]() ,所用方法错误的是
,所用方法错误的是![]()
![]()
A. N2 (O2):通过灼热的铜网
B. CO(CO2):通过足量澄清的石灰水
C. CaO(CaCO3):加水
D. Cu粉(Fe):加稀硫酸
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】右图为甲、乙两种固体物质的溶解度曲线,下列说法正确的是
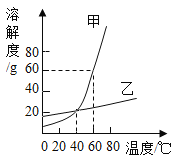
A.20℃时,甲物质的溶解度比乙物质的溶解度小
B.甲物质中混有少量乙物质,采用蒸发结晶的方法提纯甲物质
C.40℃时,甲、乙两种物质的饱和溶液中溶质质量分数相等
D.60℃时,将80g甲物质放入100g 水中,所得溶液中溶质质量与溶剂质量之比是 4:5
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】现预探究一固体混合物A的成分,已知其中可能含有NH4Cl、KNO3、Na2SO4、(NH4)2SO4、Fe2O3五种物质中的两种或多种.按图所示进行实验,出现的现象如图所示(设过程中所有可能发生的反应均恰好完全反应)
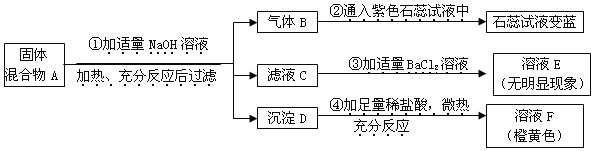
试根据实验过程和发生的现象填写以下空白:
(1)产生的气体B是(写化学式)______;
(2)溶液E中,一定存在的金属阳离子是(写离子符号)______;
(3)写出实验过程④中发生的化学反应的化学方程式______;
(4)混合物A中,肯定存在的物质是(写化学式)______.
(5)上述实验证明A中______(填“含有”或“不含”)Na2SO4,请简述理由:______.
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】模型是联系宏观与微观的桥梁。
(1)如图是钠原子结构示意图。

①X的数值为_________________。
②“11”指的是_________________。
③钠原子在化学反应中易失去1个电子,形成_______(填离子符号)。
(2)下图是氢分子和氧分子运动的示意图。

①在A、B和C中,能比较得出“温度越高,分子运动速率越快”的是__________(填标号)。
②从图中可见,影响分子运动速率的因素除温度外,还与______________________有关。
③举一个能说明“温度升高,分子运动速率加快”的生活事例:___________________________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】控制变量法是科学探究中常用的方法。化学反应的快慢常与外界条件有关,如温度、压强、催化剂、固体表面积等因素。以下实验设计的目的是探究化学反应快慢与外界条件的关系。
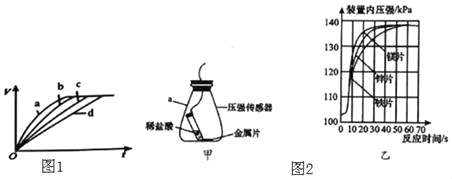
Ⅰ.现有四份等质量的铁分别与足量的盐酸进行反应,图1为随着反应时间的变化产生气体体积V的关系曲线。四组实验条件分别是:
a.50℃、铁粉 b.30℃、铁粉 c.30℃、铁丝 d.20℃、铁丝
(1)请写出铁与盐酸反应的化学方程式:_____,该反应进行时会放出热量。
(2)通过实验a和b对比,得出的结论是_____;若要比较金属铁的表面积对反应快慢的影响,应选择的实验组别是_____。实验中观察到产生气体“逐渐变快又变慢”,请解释“逐渐变快”的原因是_____。
Ⅱ.(3)常温时,用足量的铁、锌、镁三种金属片分别与等量盐酸反应,图2中,甲图为实验发生装置,乙图为测得的产生氢气的量(图中压强越大,表示产生氢气的量越多)。
①该实验中,你认为还需要控制的变量是_____;
②根据乙图,得出反应物的量与生成H2体积的关系是_____。
(4)若足量的镁片与盐酸反应,测得产生H2的实际值比理论值偏大,请分析可能的原因(写出一条即可):
_____。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com