
【题目】精还原铁粉是一种重要的化工原料,某兴趣小组对其进行下列研究:
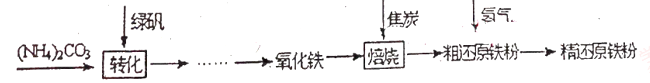
(物质制备)利用绿矾制备精还原铁粉的工艺流程如下:
粗还原铁粉中还含有少量铁的氧化物和Fe3C杂质,可用氢气在高温下进一步还原,其反应方程式为:
Fe3C+2H2![]() 3Fe+CH4 FexOy+yH2
3Fe+CH4 FexOy+yH2![]() xFe+yH2O
xFe+yH2O
(1)已知焙烧中发生的主要反应是CO夺取氧化铁中的氧元素,得到单质铁与另一种碳的氧化物,请写出该反应的化学方程式_____________。
(2)焙烧中加焦炭的作用除了可以作燃料提供反应所需高温外,还能________。
(含量测定)甲同学为得到精还原铁粉并测定粗还原铁粉中氧和碳元素的质量分数,按如下装置进行实验。已知:3CH4+4Fe2O3![]() 3CO2+6H2O+8Fe,浓硫酸有吸水性,可以吸收混合气体中的水热气,碱石灰不仅 能吸收水而且能吸收CO2。(假设每步反应都完全且不考虑装置内原有空气对测定结果的影响)。
3CO2+6H2O+8Fe,浓硫酸有吸水性,可以吸收混合气体中的水热气,碱石灰不仅 能吸收水而且能吸收CO2。(假设每步反应都完全且不考虑装置内原有空气对测定结果的影响)。
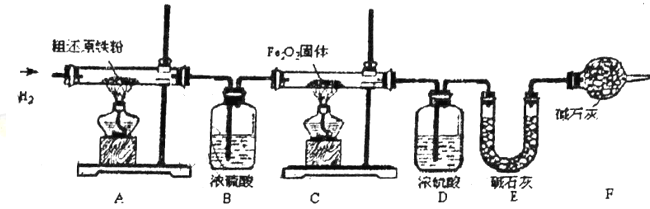
(3)主要实验步驟如下:
①按顺序组装仪器,检查装置的气密性,称量样品和必要装置的质量;
②缓缓通入纯净干燥的H2;③点燃C处酒精灯;④点燃A处酒精灯;⑤分别熄灭A、C处酒精灯;⑥再次缓缓通入H2;⑦再次称量必要装置的质量。
步骤②的目的是___________,步骤⑥的目的是__________。
(4)反应后C装置中的现象是_____________。
(5)若缺少装置F,则所测碳元素的质量分数将_____________(“偏大”、“偏小”或“不变”)。
【答案】3CO+ Fe2O3 ![]() 2Fe + 3CO2 提供CO 除去装置内的氧气,防止发生爆炸 防止铁氧化 固体由红变黑 偏大
2Fe + 3CO2 提供CO 除去装置内的氧气,防止发生爆炸 防止铁氧化 固体由红变黑 偏大
【解析】
(1)根据“焙烧中发生的主要反应是CO夺取氧化铁中的氧元素,得到单质铁与另一种碳的氧化物”和质量守恒定律可知,CO与氧化铁在高温条件下反应生成铁和二氧化碳,该反应的化学方程式为:3CO+ Fe2O3 ![]() 2Fe + 3CO2;
2Fe + 3CO2;
(2)焙烧中加焦炭的作用除了可以作燃料提供反应所需高温外,还能提供CO;
(3)氢气具有可燃性,在加热或点燃时易发生爆炸,步骤②的目的是除去装置内的氧气,防止发生爆炸,铁在高温下易与空气中的氧气反应,步骤⑤后反应生成的铁温度较高,步骤⑥再次缓缓通入H2的目的是防止铁氧化,导致实验的失败;
(4)C装置中的反应是3CH4+4Fe2O3![]() 3CO2+6H2O+8Fe,反应后C装置中的现象是固体由红变黑;
3CO2+6H2O+8Fe,反应后C装置中的现象是固体由红变黑;
(5)装置F可以吸收空气中的二氧化碳与水蒸气,否则装置F会吸收空气中的二氧化碳和水造成质量偏大,误认为生成的二氧化碳多,造成测定结果偏大。


 轻松课堂标准练系列答案
轻松课堂标准练系列答案科目:初中化学 来源: 题型:
【题目】下列实验指定容器中的水,其解释没有体现水的主要作用的是( )
实验 | A | B | C | D |
装置 |
|
|
|
|
解释 | 集气瓶中的水:吸 收放出的热量 | 量筒中的水:通过水 的体积变化得出 O2 的体积 | 集气瓶中的水:冷 却溅落熔融物,防 止集气瓶炸裂 | 集气瓶中的水:水 先将集气瓶内的空 气排净 |
A. A B. B C. C D. D
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】金属是生产生活中重要的材料,也是初中化学学习的重要内容。
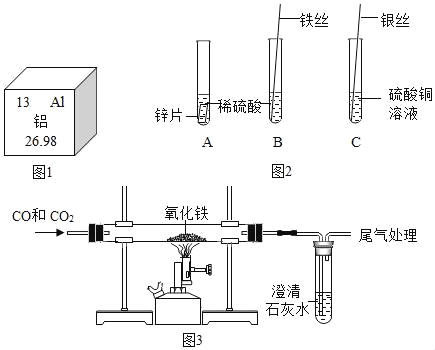
(1)如图1是铝在元素周期表中的信息,其相对原子质量是_____;比铝元素少一个周期多一个族的元素是_____。
(2)为了验证锌、铁、铜、银的金属活动性顺序,某同学进行如图2所示的实验。
①该同学能否达到实验目的______(填“能”或“不能”)?理由是____。
②自选四种试剂,另外设计实验方案,证明以上四种金属的活动性顺序,写出所用试剂即可_______________。
(3)实验室用如图3装置进行模拟炼铁的实验。
①玻璃管中的实验现象是_____;
②试管中反应的化学方程式为_____;
③要证明实验中有二氧化碳生成,还需将装置如何改进_____?
(4)金属钛生产的主要方法是在保护气中加热镁和四氯化钛的混合物使其发生置换反应。若要生产12t金属钛,理论上需要四氯化钛的质量为多少_____?
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】2017年3月22日是第25届世界水日,宣传主题是 "Wastewater"(废水),请回答下列与水有关的问题:
(1)废水中常含有难溶性杂质,除去这些杂质的操作是__________________;
(2)废水处理后,加人______可检验处理后的水是否为硬水。日常生活中通过______的方法可降低水的硬度;
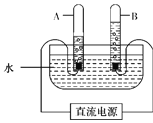
(3)实验室通常用如图所示装置来电解水,在该装置中,当A试管中产生的气体体积为10 mL时,B试管中产生的气体体积为____________;
(4)目前,河湖的污染日益严重,人们面临着水的危机,请你任举一条爱护水资源的措施:_________________
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】质量守恒定律的定量研究对化学科学发展具有重大意义。
(1)下图为某化学反应的微观模拟图,“○”和“●”分别表示两种不同的原子:
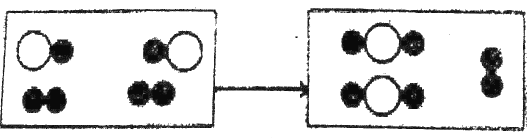
由“○●”聚集成的物质_________(填“可能”或“不可能”)是氧化物,参加反应的两种反应物的分子个数为________,此反应的基本反应类型为_________。
(2)硫化氢气体可以在氧气中燃烧生成黄色固体单质和水,反应的化学方程式是________; 镁条能在二氧化碳中燃烧,生成一种白色固体氧化物和一种黑色固体,请写出该反应的化学方程式_______。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】为测定某混合物(只含氧化镁和氧化铝)中氧元素的质量分数。进行如下实验:取18.2g的固体混合物,使之与500g质量分数为7.3%的盐酸充分反应,将反应后的溶液蒸干得到 45.7g固体。则原混合物中氧元素的质量分数约为( )
A. 42.7% B. 44.0% C. 59.3% D. 70.3%
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】张南和化学兴趣小组的同学从内蒙古伊盟地区的天然碱湖带来一种“碱”样品(含 有碳酸钠、氯化钠和泥沙)。为测定这种样品(样品中的泥沙不参加反应,也不溶于水)中 碳酸钠的含量,并得到纯净的一定浓度的氯化钠溶液。进行了如下实验:
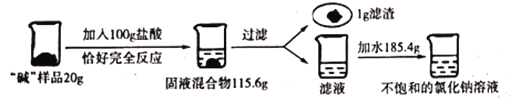
请回答下列问题:
(1)写出发生反应的化学方程式____________;
(2)根据已知条件列出求解反应中生成氯化钠的质量(X)的比例式_______;
(3)该“碱”样品中碳酸钠的含量为_______;
(4)若最终得到的滤液为不饱和溶液,则所得滤液中溶质的质量分数为______;
(5)若用36.5%的浓盐酸配制上述实验所用的稀盐酸,需浓盐酸的质量为________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】人类的日常生产、生活都离不开水.
(1)化学课上同学们分组研究水的净化及组成(装置如图).净化后的池塘水与矿泉水、蒸馏水、自来水四种水属于纯净物的是__________,实验②中净化水的方法是__________和___________。
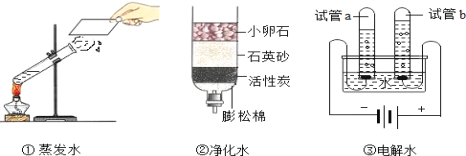
(2)实验③中通电一段时间后,试管a中的气体是 ______ (填写化学式),试管b中的气体是_______(填写化学式),该实验说明水是由 ______ 组成的,反应的化学方程式为 _____________.
(3)请根据电解水的微观示意图由于化学反应前后原子的 ______ 、 ______ 和质量都没有发生变化,因此在化学反应中质量守恒。
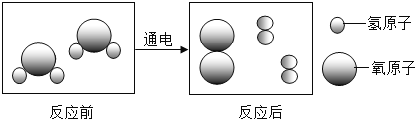
(4)从微观角度分析,实验①和③两个变化中最本质的区别是 ___________.
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】在学习质量守恒定律的内容时,我们曾经做了如图所示的实验,回答下列问题:
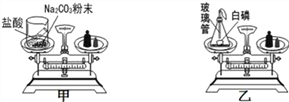
(1) 图甲中反应后天平的指针___(“偏左”“偏右”“不变”),原因是______________,该反应是否符合质量守恒定律?________。(“符合”或“不符合”), 图甲发生的化学反应方程是_____________________。
(2)图乙中在实验设计时,锥形瓶底放层细沙的原因是:____________________;玻璃管上方系一瘪气球的目的是______________。白磷刚引燃,立即将锥形瓶放到天平上称量,天平不平衡。结论是:质量不守恒。待锥形瓶冷却后,重新放到托盘天平上称量,天平平衡。结论是:质量守恒。你认为结论正确的是________(填“前一种”或“后一种”)
(3)由质量守恒定律可知,化学反应前后,一定改变的是____(填序号)
①原子种类 ②原子数目 ③分子种类 ④分子数目 ⑤元素种类 ⑥物质总质量
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com