
【题目】盐酸硫酸和硝酸是三种常用的酸,为什么初中化学只介绍了盐酸和硫酸,没有介绍硝酸呢?兴趣小组同学在实验室发现一瓶硝酸,发现硝酸保存在棕色试剂瓶中,小组的同学对此产生了好奇,并对硝酸的部分性质进行如下探究。
[查阅资料]①棕色试剂瓶常用于保存见光易分解的物质;②NO是无色气体,能与空气中的氧气迅速反应生成NO2,NO2是红棕色气体,低温时转化成液体N2O4;③相同条件下,气体的体积比等于气体分子数目之比;④无水氯化钙可干燥NO、NO2、H2、O2等。
[提出问题]硝酸具有哪些化学性质?
[提出猜想]猜想一:硝酸不稳定,易分解;
猜想二:稀硝酸可与铁反应产生氢气;
猜想三:硝酸能与氢氧化钠反应。
[实验探究]
实验操作 | 实验现象 | 实验结论 | |
① | 取少量浓硝酸于试管中,用酒精灯加热 | 产生红棕色气体 | 猜想一正确 |
② | 向稀硝酸中加入少量铁粉 | 有气泡产生,气体在试管口由无色变为红棕色,铁粉逐渐溶解,得到黄色溶液 | 猜想二不正确 |
③ | 向稀硝酸中滴加氢氧化钠溶液 | 无明显现象 | 猜想三不正确 |
[交流讨论](1)小明认为铁与稀硝酸反应产生的气体是NO,他的依据是___________________。
(2)小江认为实验③的结论不严谨,他重新设计方案验证猜想三,请补充小江的实验报告:
实验操作 | 实验现象 | 实验结论 |
_______________。 | _______________。 | 猜想三正确 |
[继续探究]为验证硝酸分解的气体产物,在老师的指导下,小组同学设计如图装置:
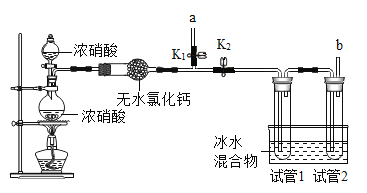
[实验步骤] I.关闭K2,打开K,加热观察到有红棕色气体产生,当有红棕色气体由导管口a逸出时,将带火星的木条放在导管口a处,观察到木条复燃;
II.打开K2,关闭K1,一段时间后,试管1中出现无色液体,试管2中无明显现象,将带火星的木条放在导管口b处,观察到木条复燃。经进一步实验确认浓硝酸分解的产物有三种,则浓硝酸分解产生的气体为____________。
[知识拓展]小江分析上述实验后,认为二氧化氮具有助燃性,请说明理由_____________。
【答案】参加反应的物质中含有氮元素和氧元素,NO是无色气体,能与空气中氧气反应生成红棕色的NO2 先向氢氧化钠溶液中滴加几滴无色酚酞试液,再逐滴加人稀硝酸(合理即可) 滴加无色酚酞试液后显红色,加人稀硝酸后颜色变浅,最后变成无色(与上空对应) NO2、O2 由硝酸分解的产物可知硝酸分解的化学方程式,其中二氧化氮与氧气的分子数目之比为4:1,即分解的气体产物中二氧化氮与氧气的体积比为4:1,二者的混合气体能使带火星的木条复燃,对比带火星的木条在空气中的现象可知二氧化氮具有助燃性(合理即可)。
【解析】
[交流讨论]
(1)铁和稀硝酸为反应物,从质量守恒定律中的元素守恒分析,可知反应生成的气体可能是一氧化氮;从现象分析,铁与稀硝酸反应产生的气体开始无颜色,上升至试管口时变成红棕色,根据[查阅资料],可知一氧化氮是无色气体,一氧化氮可与空气中的氧气迅速反应生成二氧化氮,二氧化氮是红棕色气体,所以铁与稀硝酸反应生成的气体是一氧化氮;
(2)氢氧化钠与硝酸反应生成硝酸钠和水,硝酸钠易溶于水,所以反应无明显现象,要证明反应确实发生了,可利用酸碱指示剂,先向氢氧化钠溶液中滴加几滴无色酚酞试液,再逐滴加人稀硝酸,观察到溶液先变红色,随着稀硝酸的加入,溶液颜色逐渐变浅,最后变成无色,证明反应后的溶液中没有氢氧化钠,即氢氧化钠与稀硝酸发生了反应;
[实验步骤]
根据试管1中有无色液体产生,结合二氧化氮的性质可知,浓硝酸分解生成了二氧化氮,根据带火星的木条放在导管口b处可以复燃,说明浓硝酸分解的产物中有氧气,再结合浓硝酸的分解产物有三种,根据质量守恒定律可知,另一种产物是水,即浓硝酸分解生成的气体为二氧化氮、氧气;
[知识拓展]
氧气能使带火星的木条复燃,氧气约占空气体积的五分之一,空气不能使带火星的木条复燃,根据浓硝酸分解的化学方程式![]() 可知,浓硝酸分解产生的气体中氧气占气体总体积的五分之一,根据实验现象,浓硝酸分解产生的混合气体可使带火星的木条复燃,由此可知二氧化氮具有一定的助燃性。
可知,浓硝酸分解产生的气体中氧气占气体总体积的五分之一,根据实验现象,浓硝酸分解产生的混合气体可使带火星的木条复燃,由此可知二氧化氮具有一定的助燃性。


 第1卷单元月考期中期末系列答案
第1卷单元月考期中期末系列答案科目:初中化学 来源: 题型:
【题目】2019年4月25日至4月27日,第二届“一带一路”国际合作高峰论坛在北京举行。目前,聚焦“六廊六路多国多港”主骨架,推动一批合作项目取得实质性进展。中巴经济走廊建设进展顺利,中老铁路、中泰铁路、匈塞铁路建设稳步推进。

(1)铁路建设中铺路的石子主要成分是碳酸钙,碳酸钙中碳元素的化合价为_____。
(2)如图为中巴铁路路线图。此前已建成通车中国西部出境铁路“欧亚大陆桥”一段。请写出工业上用赤铁矿炼铁的化学方程式_____。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】我国科学家研制出在可见光下将水和二氧化碳转化为甲烷的复合光催化剂,其催化反应的微观示意图如下,下列说法不正确的是

A.反应前后催化剂的化学性质不变B.反应前后氧元素的化合价不变
C.反应前后分子总数不变D.对缓解人类能源危机有重要意义
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】为探究二氧化碳能否和水反应,用四朵石蕊溶液染成紫色的干燥小花完成下图四个实验。实验I、Ⅳ中小花变红,实验Ⅱ、Ⅲ中小花不变色。下列说法不正确的是( )
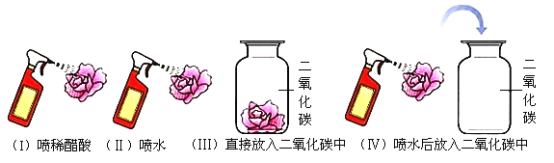
A. 实验Ⅰ、Ⅱ说明醋酸可以使小花变红
B. 实验Ⅲ说明二氧化碳不能使小花变红
C. 实验Ⅱ、Ⅲ、Ⅳ说明二氧化碳能与水发生化学反应
D. 上述实验说明二氧化碳和醋酸具有相似的化学性质
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】写出下列化学方程式:
①木炭还原氧化铜______;
②检验二氧化碳______;
③碳还原氧化铁______;
④实验室制取二氧化碳______;
⑤二氧化碳与碳反应______。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】我国科学家成功合成了世界首个全氮阴离子(N5-)的化合物[(N5)6(H3O)3(NH4)4Cl]占领了新一代超高能材料研究的国际制高点、下列关于该物质的说法正确的是
A.该化合物是由五种元素组成的
B.其中N、H、O的质量比为34:25:3
C.其中NH4+中氮元素的化合价为-2
D.其中含有两种阳离子和两种阴离子
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】下列图像与对应的实验描述相符的是
A.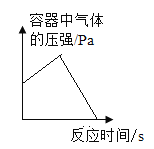 密闭容器中点燃红磷
密闭容器中点燃红磷
B.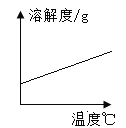 氧气在水中的溶解度
氧气在水中的溶解度
C.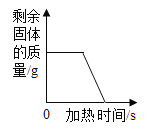 加热KClO3和MnO2的混合物制O2
加热KClO3和MnO2的混合物制O2
D.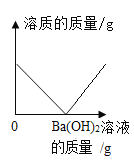 将足量的Ba(OH)2溶液逐滴滴入硫酸溶液中
将足量的Ba(OH)2溶液逐滴滴入硫酸溶液中
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】阅读下面科普短文。
“菠菜豆腐”是我国的传统菜肴,近年来,有关“菠菜豆腐”的争论主要集中在钙吸收率方面。菠菜中富含易溶于水的草酸,若单独吃菠菜,其中的草酸会结合胃内食糜中的部分铁和锌,还能够进入血液,沉淀血液中所含的钙。而将豆腐与菠菜同食,豆腐中的可溶性钙与菠菜中的草酸结合成不溶性的草酸钙(CaC2O4)沉淀,既能够保护食物中的铁和锌等元素,还能保证人体内的钙不被草酸结合。因此,豆腐与菠菜同食仍不失为一个好的搭配。
研究人员以新鲜菠菜和新鲜豆腐为材料,进行了“菠菜豆腐”烹调方法的研究。
(实验1)探究菠菜质量对菜肴中可溶性钙含量的影响。实验结果如下:
豆腐/ g | 10 | 10 | 10 | 10 | 10 |
菠菜/ g | 5 | 10 | 15 | 20 | 25 |
可溶性钙/总钙 | 0.364 | 0.287 | 0.186 | 0.125 | 0.088 |
(实验2)探究菠菜焯水时间对菜肴中可溶性钙含量的影响。
用100g豆腐和250g菠菜(焯水时间不同)制成菜肴,测定每100g“菠菜豆腐”中可溶性钙的质量,结果见下图。

以上研究表明,烹调“菠菜豆腐”时,如能适当减少菠菜的比例,并预先将菠菜焯水,则豆腐中钙的吸收率将会显著提高。
根据文章内容,回答下列问题:
(1)可溶性钙中的“钙”是指_________(“钙单质”或“钙元素”)。
(2)豆腐中富含的营养素是_____________。
A. 维生素 B. 糖类 C. 蛋白质 D. 油脂
(3)结合实验1的数据分析,可得到的结论是_________________。
(4)用焯水后的菠菜制作“菠菜豆腐”,能提高可溶性钙含量的原因是__________。
(5)草酸钙在高温下完全分解可得到两种气态氧化物和一种固态氧化物,该反应的化学方程式为____________________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】下列①~④ 选项中,实验室制取气体时,需要考虑的因素是( )
① 反应速率适中② 安全、操作方便③ 反应物和生成物中不宜有其他气体④ 生成气体的密度及水溶解性
A. ①②③ B. ①②③④ C. ①②④ D. ②③④
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com