
【题目】根据课本实验回答下列问题:
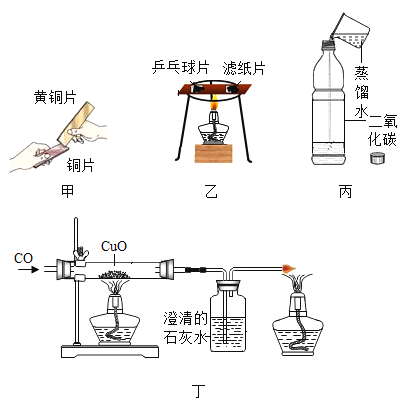
(1)甲实验中,铜片表面留下明显划痕,说明黄铜片比铜片的硬度_____(填“大”或“小”);
(2)乙实验中,乒乓球片先燃烧,滤纸片后燃烧,说明燃烧需要的条件是_____;
(3)丙实验的现象是_____;
(4)丁实验,开始时,应先_____,后_____(选填“通入CO”或“加热”)。
【答案】大 温度需要达到可燃物的着火点 瓶变瘪 通入CO 加热
【解析】
(1)铜表面有划痕,说明是黄铜在其表面划走的少量的铜,造成了划痕,因此说明黄铜硬度大于铜片;
故答案为:大。
(2)可燃物燃烧还需要满足与氧气接触和达到着火点这两个条件,乒乓球片和滤纸片都放到空气中,与氧气接触,但是乒乓球片先着了,说明加热后先达到了乒乓球片的着火点,因为说明燃烧时,温度需要达到可燃物的着火点;
故答案为:温度需要达到可燃物的着火点。
(3)二氧化碳能溶于水,且能和水反应生成碳酸,气体减少,内部压强减小,外界大气压将瓶压瘪;
故答案为:瓶变瘪。
(4)一氧化碳为易燃易爆气体,装置内有残留的空气,不得直接通入一氧化碳就加热,需要先通一氧化碳排空后,再加热,避免爆炸;
故答案为:通入CO;加热。


 阅读快车系列答案
阅读快车系列答案科目:初中化学 来源: 题型:
【题目】甲、乙、丙三种固体物质的溶解度曲线如图所示,回答下列问题。
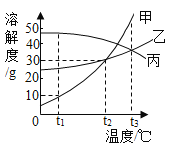
(1)t1℃时,甲、乙、丙三物质的溶解度由大到小的顺序是___________;
(2)t2℃时,甲物质的饱和溶液中溶质与溶剂的质量比为___________(写最简比);
(3)甲物质中混有少量乙,提纯甲物质可采取__________的方法;
(4)欲将接近饱和的丙溶液变为饱和溶液,可采取___________的方法;
(5)将t1℃时甲、乙、丙三种物质的饱和溶液升温到t3℃,所得溶液中溶质质量分数最大的是________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】用如图所示装置,在常温下,分别进行研究燃烧条件和研究氧气性质的实验。已知:白磷的着火点为40℃,实验时打开导管中的开关。
步骤 | (实验1)研究燃烧条件 | (实验2)研究氧气性质 |
Ⅰ | 烧杯中盛有80℃的热水,分别在燃烧匙和烧杯中导管口放置一小块白磷,塞紧瓶塞 | 烧杯中盛有NaOH溶液,燃烧匙中放入木炭,点燃木炭后迅速将燃烧匙伸入瓶中,塞紧瓶塞 |
Ⅱ | 推入适量H2O2溶液 | 推入适量H2O2溶液 |
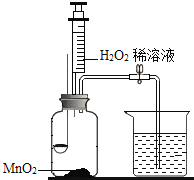
(1)实验1中,推入H2O2溶液前,燃烧匙和水中的白磷均不燃烧,燃烧匙中白磷不燃烧的原因是_____; 烧杯中白磷未燃烧的原因是_____; 推入H2O2溶液后,观察到烧杯中的现象是_____。
(2)实验2中,推入H2O2溶液后,观察到木炭燃烧得更剧烈,由此得出氧气的性质是_____;木炭熄灭后冷却一段时间,烧杯中的溶液_____(填“能”或“否”)流入集气瓶。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】下列实验不能达到实验目的的是
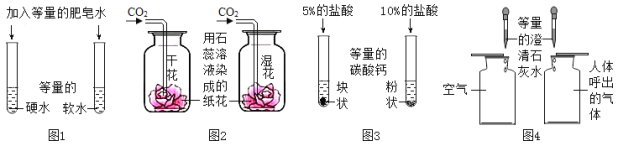
A.图1,区分硬水和软水
B.图2,探究CO2与水的反应
C.图3,探究接触面积对反应速率的影响
D.图4,比较空气与人体呼出的气体中CO2含量
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】如图是配制100g质量分数为15% 的氯化钠溶液的操作过程示意图:试回答:

(1)配制过程中需要用到的玻璃仪器是(广口瓶除外):玻璃棒、胶头滴管、量筒、 _________________ .
(2)应选择量筒的量程是______毫升(填50或100),在实验过程中,某同学用量筒量取水时,用俯视读数法,则会造成所配溶液溶质质量分数 ______(填偏大或偏小).
(3)B操作向托盘上加氯化钠时,若指针偏向分度盘的左边,应进行的操作是 _____操作E的作用是 _________________
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】向一定质量的CaCl2和HCl的混合溶液中逐滴加入溶质质量分数为10.6%的Na2CO3溶液,实验过程中加入Na2CO3溶液的质量与产生沉淀或气体的质量关系如图所示。下列说法错误的是( )
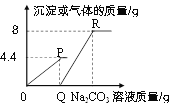
A. P点时的溶液只含一种溶质
B. R点对应横坐标的数值为180
C. 0至P过程中溶液的pH变大
D. Q至R段表示生成沉淀的过程
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】实验室常用下列装置制取气体,请你根据所学知识回答下列问题。
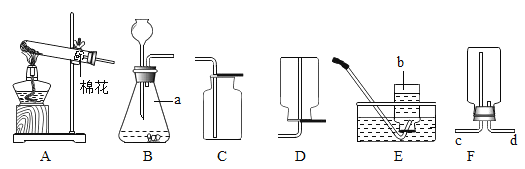
(1)写出图中仪器a、b的名称:a_____;b_____。
(2)用AE装置制取氧气,发生反应的化学方程式为_____,停止加热时必须先_____,防止_____。
(3)若用双氧水和二氧化锰制取氧气,应选择的发生装置是_____。反应的化学方程式为_____。
(4)若装置B中反应剧烈,从实验安全角度考虑,可采取的措施有_____(填序号,可多选)。
①用容积较小的锥形瓶
②控制液体的滴加速度
③加热反应物
④降低反应物浓度(反应物浓度越小,反应越慢)
(5)实验室常用稀硫酸和锌粒反应制取H2,反应原理用化学方程式表示为_____。可选用发生装置_____,若用F装置利用排空气法收集H2气体,则气体从_____端通入(填“c”或“d”)。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】下表是20℃时部分物质的溶解度数据。
物质 | NaOH | AlCl3 | Al(OH)3 |
溶解度/g | 109 | 69.9 | 0.0015 |
氢氧化铝为两性氢氧化物,能与酸反应也,能与强碱反应,与氢氧化钠反应能生成偏铝酸钠(NaAlO2)和水
(1)配制溶液。其中配制20℃时100g饱和氯化铝溶液的基本步骤是:称取氯化铝固体—量取水—溶解—装瓶贴标签。
①称取氯化铝固体的质量_____________g。
②量取水加加入烧杯溶解。
③装瓶后贴标签,在标签上填写:_____________。
(2)进行性质探究实验。20℃时,根据数据回答下列问题:
①向氯化铝溶液中通入氢氧化钠直至过量,先生成Al(OH)3,再转化为NaAlO2,可观察到的现象是___________;Al(OH)3与氢氧化钠的反应方程式反应__________。
②将100g饱和氯化铝溶液,与足量的氢氧化钠反应能生成NaAlO2___________g,同时需10%氢氧化钠溶液的质量至少为__________g。(计算结果精确到0.1)
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】A、B、C、D、E 五种物质均为初中化学常见的化合物,它们之间的关系如图所示,相互之间连线表示两者间能发生化学反应。A、C、E 均为氧化物,A 是人体呼出的主要气体;在实验室中 B 能用来制取 A,而 D 可以用来检验 A;C 和 E 反应能生成 D。
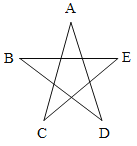
(1)A 的化学式__________________ ;
(2)B 和 D 反应的化学方程式为_____________;
(3)C 和 E 反应的化学方程式为_____________; 该反应的基本反应类型是____________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com