
【题目】甲、乙两种固体物质的溶解度曲线如图所示(已知两种物质溶解时互不影响),请回答下列问题。
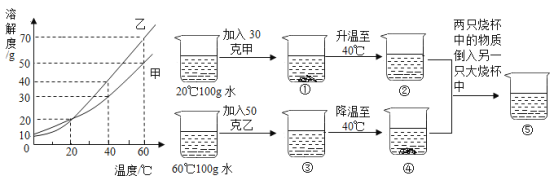
(1)甲、乙溶解度曲线交点的意义___。
(2)40℃时分别溶解甲、乙两种固体,所得溶液中质量分数的最大值是_(精确到0.1%)。
(3)图中的饱和溶液有___(填序号),③到④实验过程中析出晶体质量为___g。
(4)40℃时,将等质量的甲、乙两种物质的饱和溶液分别蒸发等质量的水后,恢复到40℃,所得溶液质量的大小关系是甲__乙(填“大于”、“等于”或“小于”)。
【答案】20℃时,甲、乙溶解度相同 28.6% ①②④ 10 大于
【解析】
(1)由图可知,在20℃甲、乙溶解度曲线有一个交点,该点的意义是20℃时,甲、乙溶解度相同。
(2)40℃时甲的溶解度为40g,乙的溶解度为30g,40℃时分别溶解甲、乙两种固体,所得溶液中质量分数的最大值应该是甲的饱和溶液的溶质质量分数,根据溶解度与溶质质量分数的关系,该溶质质量分数为![]() 。
。
(3)已知在20℃时,甲的溶解度为20g,则在20℃时100g水中加入30g甲,溶液达到饱和;在40℃时,甲的溶解度为30g,则在40℃时100g水中加入30g甲,溶液刚好达到饱和;在60℃时,乙的溶解度为70g,则在20℃时100g水中加入50g乙,溶液没有达到饱和;在40℃时,乙的溶解度为40g,则在40℃时100g水中加入50g乙,溶液达到饱和;在40℃时,将两只烧杯溶液倒入一只大烧杯中,溶剂质量为200g,则在40℃时200g水中加入30g甲和50g乙,溶液没有达到饱和。故选①②④。在40℃时,乙的溶解度为40g,则在60℃时100g水中溶解了50g乙,降温至40℃时,析出晶体质量为50 g -40 g =10g。
(4)由曲线图可知,40℃时,乙的溶解度大于甲的溶解度,将等质量的甲、乙两种物质的饱和溶液分别蒸发等质量的水后,恢复到40℃,则乙析出晶体的质量大于甲析出晶体的质量,所以所得溶液质量是甲大于乙。


 宝贝计划期末冲刺夺100分系列答案
宝贝计划期末冲刺夺100分系列答案 能考试全能100分系列答案
能考试全能100分系列答案科目:初中化学 来源: 题型:
【题目】在氯化钙和氯化钠的混合物中加入一定量的水,全部溶解得 到 75g 混合 溶液,向该溶液中逐滴加入一定溶质质量分数的碳酸钠 溶液,生成沉淀与加入碳酸钠溶液的质量关系如图所示。计 算:
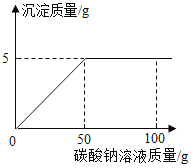
(1) 恰好完全反应 时生成沉淀 质量为 g。
(2) 若恰好完全反应时所得溶 液的溶质质量分数为 10%,则原固体混合物的质量是多少
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】某校化学活动小组准备探究气体的测定和数据处理方法。
(提出问题)如何利用石灰石与稀盐酸反应来测定生成CO2的质量和体积,并处理数据.
(实验设计)通过下列两个实验分别测定CO2的质量和体积:
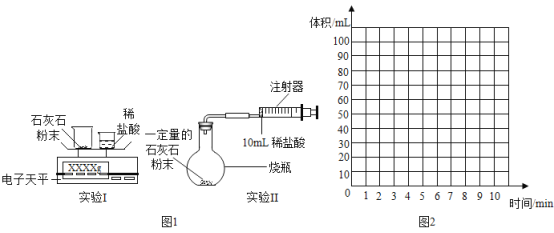
(分析与表达)
(1)上述两个实验中,反应的化学方程式为________。
(2)实验Ⅰ中,将小烧杯中的所有稀盐酸分几次加入到大烧杯中,并不断搅拌,判断石灰石中CaCO3完全反应的实验现象是________。
(3)实验Ⅱ中,先连接好装置,在检查装置的气密性(请简述方法________),然后装好药品,最后将10mL稀盐酸快速推入烧杯中,若稀盐酸是缓慢推入的,则可能造成的后果是________.
(4)(记录与处理)
已知实验Ⅰ反应前的总质量(m(大烧杯+石灰石粉末)+m(小烧杯+稀盐酸)),要计算生成CO2的质量,至少还需要的数据是___________。
A m(小烧杯) B m(大烧杯) C m(大烧杯+反应后剩余物)
(5)实验Ⅱ的实验记录如下(表中数据在相同温度、相同压强条件下测定)
时间/min | 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | 10 |
注射器读数/ml | 60.0 | 85.0 | 88.0 | 89.0 | 89.5 | 89.8 | 89.9 | 90.0 | 90.0 | 90.0 |
据以上实验过程和实验数据综合分析,最终生成CO2的体积是________ mL
注意:若答对下面题奖励4分,但化学总分不超过60分。
(6)根据你的认识,在图2中坐标图中绘制出0~10min生成CO2体积随时间变化的曲线。________
(7)(反思与评价)
经过分析,你认为实验Ⅰ的优点是________,实验Ⅱ的优点是________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】某校化学兴趣小组在实验室使用稀盐酸及某石灰石制取二氧化碳,反应后废物利用,用废水(含少量Fe3+等杂质)生产二水合氯化钙(CaC122H2O)。具体的实验流程如图所示,根据题意回答下列问题。
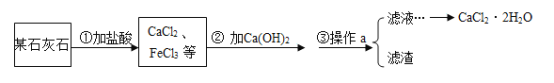
(1)写出第①步的化学方程式______。
(2)第②步发生的反应属于______反应(填基本反应类型)。
(3)操作a的名称是______。进行该操作时用到的玻璃仪器有烧杯、玻璃棒和______。
(4)滤渣的主要成分为______,它属于______(填物质分类)
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】实验室制备二氧化碳的实验如下:
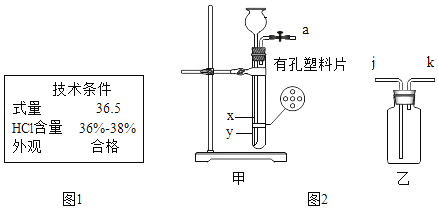
(1)市售浓盐酸的局部标签如图1所示,该盐酸中HCl质量分数的范围是________.为使制备过程中二氧化碳平稳地产生且较纯净,应将该浓盐酸________.
(2)检查甲装置的气密性的方法________.
(3)用甲装置制备二氧化碳,选择的固体药品是________(选填字母).
a 粉末状石灰石 b 块状大理石 c 粉末状熟石灰 d 块状生石灰
(4)控制所加盐酸的量,使反应时甲装置内液面位于________(选填“x”或“y”)处为宜.
(5)收集二氧化碳时,应将甲的a处与乙的________处连接(选填字母)
(6)写出用澄清石灰水检验二氧化碳的化学方程式________.
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】为测定一瓶久置的过氧化氢溶液溶质的质量分数,实验过程如图所示:
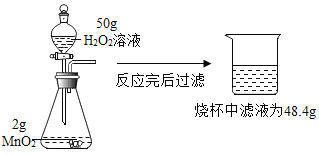
(1)实验结束后,该同学过滤出烧杯内的固体,并对其进行洗涤、干燥、称量,得到固体的质量应为____g。
(2)生成氧气的质量为____g。
(3)计算该瓶过氧化氢溶液溶质的质量分数____。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】下列为实验室常用的实验装置示意图。
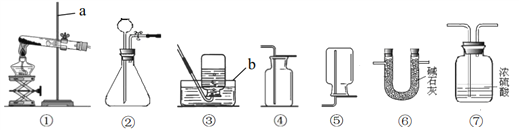
请回答问题:
(1)写出 a、b 的仪器名称:a________________;b___________________。
(2)实验室用加热氯酸钾和二氧化锰的混合物来制取氧气,所选用的装置组合是_______(填装置序号,下同),反应的化学方程式为_____________________________。
(3)若实验室需制取干燥的 CO2气体,应将待干燥的气体先通过干燥装置__________,再用装置_____________________来收集。
(4)实验室收集某气体只能用装置⑤,由此说明该气体具有的物理性质是_____________________________________________________________________。
(5)检查装置②气密性的方法是:先用夹子夹住导气管上的橡皮管,再向长颈漏斗中加入水至形成一段水柱,静置,若观察到_____________________,说明气密性良好。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】硫酸钡是一种不溶于水,也不和酸反应的固体,医疗上常用硫酸钡作透视肠胃的内 服造影剂,俗称“钡餐”。若“钡餐”中含有碳酸钡,就会致人中毒。为测定某硫酸钡样品中碳酸钡的 含量,取 100 g 样品,向其中逐渐加入一定质量分数的稀硝酸至恰好完全反应,发生反应的化学方 程式为:BaCO3+2HNO3=Ba(NO3)2+H2O+CO2↑,测得共用去稀硝酸 245.7 g,反应后称得烧杯中物质的总质量为 341.3 g。请计算:
(1)反应生成的二氧化碳为_____g。
(2)所用的稀硝酸的溶质质量分数是多少_________?原样品中硫酸钡的质量分数是多少?(计算结果保留一位小数)__________
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】下列是甲、乙两物质的溶解度曲线。下列说法正确的是( )
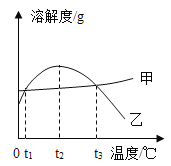
A.甲、乙两物质的溶解度相等
B.甲、乙两物质的溶解度均随温度升高而增大
C.常用降温法从甲的饱和溶液中获取甲的晶体
D.将乙的饱和溶液温度由t2℃降至0℃,有晶体析出
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com