
【题目】我国化学家侯德榜创立了侯氏制碱法,为世界制碱工业作出了杰出贡献。在实际生产的产品碳酸钠中会混有少量的氯化钠,现有纯碱样品,为测定该样品中碳酸钠的质量分数,称取样品6 g,放入20 g水中使其完全溶解,再加入稀盐酸26. 2 g,恰好完全反应,气体全部逸出,得到不饱和氯化钠溶液,溶液的总质量为50 g。试计算:
(1)生成二氧化碳的质量为多少g。
(2)样品中碳酸钠的质量。
(3)反应后所得溶液中溶质的质量分数。
【答案】(1)2.2(2)5.3g(3)13.1%
【解析】
(1)根据质量守恒定律可知,反应前后的物质的总质量不变,则反应前的质量为:6g+20g+26.2g=52.2g,反应后溶液的质量为50g,则相差的质量就是生成气体的质量,即:52.2g-50g=2.2g。故答案为:2.2;
(2)设参加反应的碳酸钠的质量为x,生成的氯化钠的质量为y。

解得x=5.3g,y=5.85g。
则样品中,碳酸钠的质量为5.3g。
(3)根据题意可知,两种溶液混合后,恰好完全反应,则此时得到的是氯化钠溶液。通过分析题意可知,氯化钠有两种来源,一种是样品中含有的,质量为6g-5.3g=0.7g。一种是碳酸钠和盐酸反应生成的氯化钠,质量为5.85g。则反应后溶质的质量为:5.85g+0.7g=6.55g。溶液的质量为50g,则恰好完全反应时,溶质的质量分数为:![]() 。
。


 名校课堂系列答案
名校课堂系列答案科目:初中化学 来源: 题型:
【题目】材料是人类社会物质文明进步的重要标志之一。回答下列问题:
(1)商代后母戊鼎代表着我国古代高超的金属制造水平,它主要是含__元素的合金。

(2)从陶瓷、玻璃、水泥到电子芯片,硅元素的用途非常广泛。工业制取高纯硅的一个反应的微观示意图如下:
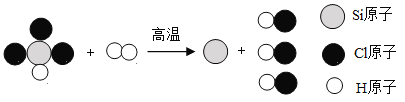
①写出该图示表示的化学方程式___,其基本反应类型是_____。
②从上图图示看出:微观上,化学反应前后分子改变了,而_____没有改变。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】实验室制取某些气体的装置如下图所示。下列说法正确的是

A.装置①和③组合可以用来制取氢气
B.装置②和③组合可以用来制取氧气
C.装置②和⑤组合可以用来制取二氧化碳
D.装置②可以控制反应的随时发生随时停止
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】小倩同学了解到:外国人把中国称为“China”,在英文中与瓷器是同一个单词。“青花瓷”又是在中国瓷器中最具代表性的。绘制青花瓷纹饰的原料中主要含有氧化钴(CoO)。
她查阅元素周期表发现钴(读音:![]() )元素符号为Co,在周期表中与铁元素同位于第4周期、第Ⅷ族。
)元素符号为Co,在周期表中与铁元素同位于第4周期、第Ⅷ族。
(提出问题)小倩同学产生疑问:为什么钴和铁都在第Ⅷ族呢?
(寻求帮助)
(1)(咨询老师)得知:因为铁与钴两种元素原子的结构具有相同点(见右图),使得二者的化学性质相似。因此把这两种元素放在一起。请你帮助小倩完成下列问题:
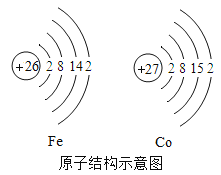
①钴元素在元素周期表中的原子序数为_______,一个钴原子比一个铁原子多一个_____(填序号)。
a.中子
b.电子
c.质子
d.电子层
②铁原子与钴原子具有相同的___(填序号,下同)。元素的化学性质主要与原子的______有关,因此二者的化学性质相似。
a.核电荷数
b.核外电子数
c.电子层数
d.最外层电子数
③在化学反应中,金属钴和铁一样,也能与稀盐酸发生反应放出氢气,反应的化学方程式为_____;钴在氧气中燃烧生成Co3O4,化学方程式为_________。
(2)(查阅资料)钴元素有着广泛的用途:钴及其化合物在材料生产、化工生产、医疗中都有着广泛的应用。钴在电池制造中需求量增长很快,钴酸锂(已知:化学式为LiCoO2,锂元素化合价为+1)常用作手机电池的正极材料,其中钻元素的化合价为____________。
(深入探讨)
(产生问题)既然钴与铁的单质具有相似的性质,那么两种元素的化合物是否也有相似的化学性质?
(设计并实验验)
(1)根据所学知识,同学们已知下列反应可以进行,并进行实验:![]()
观察记录实验现象:氧化亚铁为黑色固体;实验a中,随着稀盐酸的加入,黑色固体逐渐溶解,溶液呈现浅绿色;实验b中,加入氢氧化钠溶液后出现白色沉淀,静置在空气中,沉淀物颜色发生变化,最后变为红褐色。(查阅资料得知:原因是溶液中的Fe(OH)2遇空气中的氧气生成Fe(OH)3)
(2)同学们欲探究钴元素化合物的性质,设计并进行了如下实验:![]()
请你依据实验现象,完成下列问题:
I.实验①中,取少量灰黑色的氧化钴放入试管中,加入稀盐酸,固体被溶解,溶液呈红色,写出反应的化学方程式________________。另取一支试管加入少量氧化钴,滴入浓盐酸,固体被溶解溶液呈绿色。说明反应后钴离子在溶液中呈现的颜色与加入酸的____________有关。
Ⅱ.实验②中,加入氢氧化钠溶液,出现青蓝色沉淀。将试管静置在空气中,沉淀物颜色发生变化,最终变为棕色,试推测沉淀物颜色变化可能与空气中的____________有关。通过实验探究,同学们得出结论:铁和钴两种元素的化合物化学性质相似。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】A~G是初中化学中常见的物质,其相互反应及转化关系如图所示(部分反应条件省略)。已知A是易与人体血红蛋白结合的有毒气体,B是赤铁矿的主要成分,C是相对分子质量最小的氧化物,F是最轻的气体。
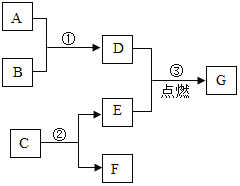
(1)G的化学式为______。
(2)反应③的实验现象_____。
(3)写出①的化学方程式________。
(4)化学反应②的基本反应类型是_____。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】阅读下面的科普短文,回答相关问题
氨是一种重要的化学物质,可用于制造硝酸和氮肥。氨主要来自于人工合成。1909年,弗里茨·哈伯成功地利用氮气和氢气合成出氨。工业合成氨的流程如图(左)所示。为了找到合成氨反应合适的催化剂,人们做了6500多次实验,发现铁触媒效果较好。在铁触媒作用下,用体积比为1:3的氮气和氢气合成氨,当容器中氨的含量不再发生变化时(平衡时),测得氨的含量分别与温度和压强的关系如图(右)所示。1913年第一座合成氨工厂建立。如今全球合成氨年产量超千万吨,其中大约85%的氨用于生产氮肥,缓解了地球上有限的耕地资源与庞大的粮食需求之间的矛盾。
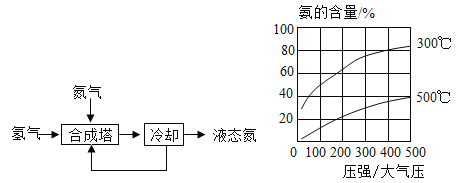
(1)工业上可用_________的方法获得合成氨的原料N2。
(2)甲烷和H2O高温下反应得到CO和原料气H2,该反应的化学方程式为_______。
(3)从“合成塔”中出来的气体是_______(填“纯净物”或“混合物”)。
(4)科学家研究合成氨反应催化剂的目的是________。
(5)按下列条件进行合成氨反应,平衡时氨的含量最高的是______(填字母)。
a 200大气压、300℃
b 200大气压、500℃
c 400大气压、300℃
d 400大气压、500℃
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】化学就在我们身边,人类的生活离不开化学,回答下列问题。
(1)人们穿的衣服通常是纤维织成的,下列属于天然纤维的是______。
A蚕丝 B涤纶 C棉花 D尼龙
(2)水是一种重要的自然资源,是生产、生活必不可少的物质。
①生活中可以通过________的方法,既可以杀灭水中的细菌,又可以降低水的硬度。
②下列各种水中属于纯净物的有___________。
A矿泉水 B糖水 C蒸馏水 D自来水
(3)服用含氢氧化铝〔Al(OH)3〕的药物可以治疗胃酸过多症,反应的化学方程式为_________,该反应属于__________(填基本反应类型)。
(4)吸烟除了影响自身健康外,也会使周围的人“被动吸烟”,其原因是_________(从微观角度解释)。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】向AgNO3、Cu(NO3)2的混合溶液中加入一定量的锌粉,充分反应,过滤。下面对反应结果的判断,不正确的是
A.若反应后溶液为蓝色,滤渣中一定不含有Zn
B.若反应后溶液为蓝色,滤渣中一定含有Ag,可能含有Cu
C.若反应后溶液为无色,滤渣中一定含有Ag和Cu
D.若反应后溶液为无色,滤渣中一定不含有Zn
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】某化学兴趣小组同学为探究硫酸的化学性质,做了如下实验:
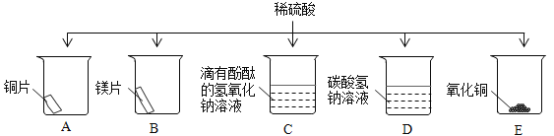
(1)能产生气泡的是__________(填序号);
(2)溶液变为蓝色的是_________(填序号),写出其中发生的化学方程式__________。
(3)能证明C中发生了反应的现象是____________。
(4)实验过程中,发现只有A中无明显现象,说明铜与稀硫酸不发生反应。
(提出问题)铜与硫酸真的不能反应吗?
(查阅资料)
①铜与浓硫酸反应的化学方程式:Cu+2H2SO4(浓)=CuSO4+SO2↑+2H2O
②SO2能使品红溶液褪色;
③SO2能与碱溶液反应;
④SO2能溶于水,但不溶于饱和NaHSO3溶液
(进行实验)
同学们在老师的帮助下用如图所示装置进行实验:
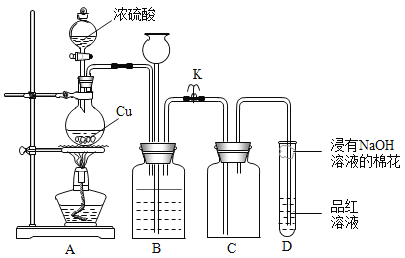
请回答下列问题:
(1)实验开始时,打开开关K,发现D中品红溶液褪色,装置D中试管口放置的棉花上浸有浓氢氧化钠溶液,其作用是__________。
(2)装置B的作用是收集贮存多余的气体,当D中有明显现象后,关闭K,移去酒精灯,但由于余热的作用,A有仍有气体产生,此时B中现象是:长颈漏斗内液面________(填“上升”或“下降”),则B中盛放的液体为_______(填序号)
A 水 B 氢氧化钠溶液 C 饱和石灰水 D 饱和NaHSO3溶液
(知识拓展)化学反应的进行与物质的溶质质量分数,反应条件都有一定的关系。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com