
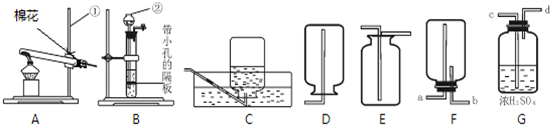
分析 (1)根据实验室常用仪器的名称和题中所指仪器的作用进行分析;
(2)根据B装置制取氧气制取氧气的反应物是过氧化氢溶液和二氧化锰,过氧化氢在二氧化锰的催化作用下生成水和氧气,排水法收集的氧气纯净,排空气法收集的氧气干燥进行分析;
(3)根据实验室制取二氧化碳的反应物是固体和液体,反应条件是常温,二氧化碳密度比空气大,易溶于水,碳酸钙和盐酸反应生成氯化钙、水和二氧化碳进行分析;
(4)根据二氧化碳密度比空气大,浓硫酸有吸水性,洗气时应该长进短出,二氧化碳和氢氧化钙反应生成碳酸钙沉淀和水进行分析.
解答 解:(1)通过分析题中所指仪器的作用可知,①是铁架台,②是长颈漏斗;
(2)B装置制取氧气制取氧气的反应物是过氧化氢溶液和二氧化锰,过氧化氢在二氧化锰的催化作用下生成水和氧气,化学方程式为:2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑,排水法收集的氧气纯净,排空气法收集的氧气干燥
,所以收集较纯净的氧气最好用:C;
(3)实验室制取二氧化碳的反应物是固体和液体,反应条件是常温,二氧化碳密度比空气大,易溶于水,所以实验室制取并收集二氧化碳应选择的装置是:BE,碳酸钙和盐酸反应生成氯化钙、水和二氧化碳,化学方程式为:CaCO3+2HCl=CaCl2+H2O+CO2↑;
(4)二氧化碳密度比空气大,所以改用F装置收集二氧化碳,则气体应从b端进入,浓硫酸有吸水性,所以要干燥二氧化碳应选取图中的G,洗气时应该长进短出,所以气体应该从c端进入,二氧化碳和氢氧化钙反应生成碳酸钙沉淀和水,所以要检验收集到的气体是否为二氧化碳气体,方法是:将气体通入澄清的石灰水,如果澄清的石灰水变浑浊,证明气体是二氧化碳,原理是:Ca(OH)2+CO2=CaCO3↓+H2O.
故答案为:(1)铁架台,长颈漏斗;
(2)2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑,C;
(3)BE,CaCO3+2HCl=CaCl2+H2O+CO2↑;
(4)b,G,c,将气体通入澄清的石灰水,如果澄清的石灰水变浑浊,证明气体是二氧化碳;Ca(OH)2+CO2=CaCO3↓+H2O.
点评 本题主要考查常见气体的发生装置与收集装置的探究,发生装置依据反应物的状态和反应条件选择,收集装置依据气体的密度和溶解性选择.


 全能测控期末小状元系列答案
全能测控期末小状元系列答案 智趣暑假温故知新系列答案
智趣暑假温故知新系列答案科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
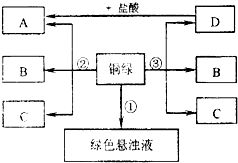 小彤的一副眼镜戴了一段时间后,发现铜质镜架上出现了一墨绿色物质,他想将其除掉.经查阅资料得知:铜在一定条件下会锈蚀生成一种绿色物质,其主要成分是碱式碳酸铜(俗称铜绿),于是他和几个同学按如下方案(如图)进行了实验.
小彤的一副眼镜戴了一段时间后,发现铜质镜架上出现了一墨绿色物质,他想将其除掉.经查阅资料得知:铜在一定条件下会锈蚀生成一种绿色物质,其主要成分是碱式碳酸铜(俗称铜绿),于是他和几个同学按如下方案(如图)进行了实验.查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 自来水澄清透明,属于纯净物 | |
| B. | 水覆盖了地球大约$\frac{3}{4}$的表面,因此不存在水危机 | |
| C. | 经济的发展、人口的增长,会造成淡水资源的紧张 | |
| D. | 长期饮用纯净水,有益于身体健康 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com