
分析 为确保实验安全,实验室对操作有明确规定.使用试管对液体加热时,为使液体均匀受热,要求试管内液体量不超过其容积的三分之一,试管口不要对着有人的方向,加热中试管要不时上下移动等.
解答 解:量取药品,如果没有说明用量,一般取最少量,液体取1-2ml,固体只要盖满试管底部.给试管里的液体加热,液体体积一般不超过试管容积的$\frac{1}{3}$,加热前先使试管在火焰上来回移动,这种方法叫预热,加热时应不时上下移动试管.为了避免伤人,加热时切记不可使试管口对着人.给试管里的固体药品加热时,试管口要略向下倾斜,
故答案为:1-2ml;盖满试管底部;$\frac{1}{3}$;预热;人;下
点评 液体受不均匀时,会出现局部沸腾而发生液体冲出,因此在对液体加热时要切记规范操作以确保安全.


 阅读快车系列答案
阅读快车系列答案科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题

查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
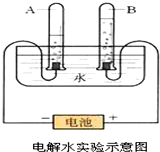 (1)图中的试管A中的气体的化学式是H2,试管B中气体的检验方法是将带火星的木条伸入试管内,如果木条复燃,可以证明是氧气;
(1)图中的试管A中的气体的化学式是H2,试管B中气体的检验方法是将带火星的木条伸入试管内,如果木条复燃,可以证明是氧气;查看答案和解析>>
科目:初中化学 来源: 题型:解答题
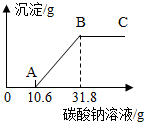 在做完“用稀盐酸和石灰石反应制取二氧化碳”的实验后,小明突然想到:是否可以测得实验所用的石灰石中碳酸钙的含量呢?小明又进行了如下实验:①将试管中反应的剩余物过滤并多次用蒸馏水洗涤,得到滤液和滤渣.②向滤渣中滴加稀盐酸,无明显的现象.③将滤渣干燥后称量,质量为0.5g.④向滤液中加入10%的Na2CO3溶液,获得了相关的数据,并绘制成如图所示的图象.根据小明的实验过程回答下列问题.(假设石灰石中的其余杂质不与稀盐酸反应)
在做完“用稀盐酸和石灰石反应制取二氧化碳”的实验后,小明突然想到:是否可以测得实验所用的石灰石中碳酸钙的含量呢?小明又进行了如下实验:①将试管中反应的剩余物过滤并多次用蒸馏水洗涤,得到滤液和滤渣.②向滤渣中滴加稀盐酸,无明显的现象.③将滤渣干燥后称量,质量为0.5g.④向滤液中加入10%的Na2CO3溶液,获得了相关的数据,并绘制成如图所示的图象.根据小明的实验过程回答下列问题.(假设石灰石中的其余杂质不与稀盐酸反应)查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | ①② | B. | ②③ | C. | ③④ | D. | ①④ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com