
【题目】为测定CuCl2和FeCl2组成的混合溶液中FeCl2的质量分数,进行如下实验:
①取200g混合溶液加入足量的AgNO3溶液,经过滤、洗涤、干燥、称量,得到143. 5gAgCl固体;
②另取原混合溶液各200g与含有杂质的废铁屑反应(杂质不溶于水,也不参与反应),共做了五组实验,其实验数据如下表。
实验组别 | 一 | 二 | 三 | 四 | 五 |
混合溶液质量/g | 200 | 200 | 200 | 200 | 200 |
铁屑质量/g | 6 | 9 | 12 | 15 | 18 |
析出铜的质量/g | 6.4 | 9.6 | m | 16 | 16 |
请分析计算:
(1)表中第三组实验的m值为____________。
(2)第___________组实验恰好完全反应。
(3)原混合溶液中FeCl2的质量分数为_________? (计算结果精确到 0.1%)
科目:初中化学 来源: 题型:
【题目】归纳总结是学习化学的重要方法,小明同学用图 1 总结了NaOH 的四条化学性质(即NaOH与四类物质能够发生化学反应)。
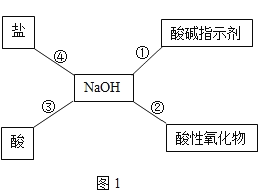
(1)写出反应②中氢氧化钠和二氧化碳反应的化学方程式_______,该反应无现象,小明为了验证反应的发生,在氢氧化钠溶液中滴加酚酞溶液后通入二氧化碳,证明反应发生。他的设计是否合理?为什么___。小芳认为向反应后的溶液中加入________就能判断反应发生了。通过小芳的帮助小明得到了正确的结论。
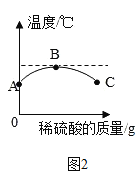
(2)小明利用温度计测出溶液的温度,溶液温度随加入稀硫酸的质量而变化的曲线来说明反应③的发生(如图 2),用化学反应方程式表示为_________________________;从该图中可以看出,反应后 B处的溶液 pH____7(填(用“<”“=”或“>”),C 点溶液中的微粒有____________。
(3)如果证明反应④能够发生,你选择的物质是_____________。
A BaCl2 B HCl C CuSO4 D MgCl2 E CaCO3
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】请根据下图回答问题:
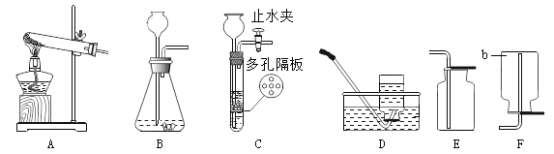
(1)用高锰酸钾制氧气,应选用的发生装置是_____(填字母序号),该反应的化学方程式为_____。
(2)常温下,用锌和稀硫酸反应制取氢气,若要随时控制反应的发生和停止,应选用的发生装置是_____(填字母序号),反应的化学方程式为 _____ ;点燃氢气前必须验纯, 为确保安全,最好选用装置 _____ (填字母序号)所示方法收集氢气。
(3)小涵通过观察发现纯锌粒与硫酸的反应明显比粗锌粒慢。通过查阅资料得知粗锌中含有一些不活泼金属,她猜想可能是粗锌中不活泼金属促进了锌与硫酸的反应。为了验证小涵的猜想,你认为应该在盛有纯锌粒和稀硫酸的试管中,加入少量的 _____溶液。
A 盐酸 B 氯化铜 C 氯化钠 D 氯化钙
(4)小川同学想通过用一定质量粗锌与足量的硫酸反应,测量生成氢气的体积来计算粗锌的纯度,于是设计了如图所示的实验装置。
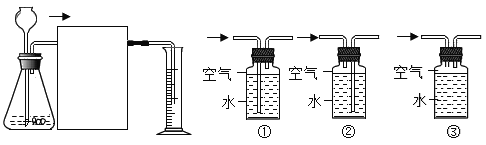
在实线框中应接入如图中的_____,广口瓶上方残留的空气_____(填“会”或“不会”)对氢气体积的测量造成影响。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】物质的性质和用途是化学的重要研究内容。
(1)浓硫酸具有吸水性,在实验室中常用它做 剂。
(2)用石灰浆粉刷墙壁,干燥后墙面就变硬了,用化学原理解释该现象。
(3)图中,用滤纸做成的小花喷洒某溶液后放在烧杯上方,片刻后变成红色。请推测喷洒液和烧杯中溶液可能是什么?(写出一组即可)
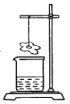
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】t1℃时,取a、b两种固体物质各25g于两只烧杯中,分别加入100g水,充分溶解后,两种固体均有剩余。升温到t2℃时,a完全溶解,b固体增多。a、b两种物质的溶解度曲线如图所示。以下判断正确的是( )
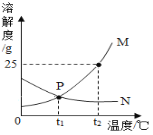
A. 图中曲线M表示b物质的溶解度曲线
B. t1℃时,两只烧杯中剩余物质的质量不相等
C. t2℃时,两只烧杯中的溶液都是饱和溶液
D. t2℃时,两只烧杯中溶液的溶质质量分数相同
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】AE 为初中化学五种不同类别的常见物质。已知 C 含有三种元素,E 为世界年产量最高的金属,A 是相对分子质量为 160 的蓝色溶液。它们之间相互关系如图所示,图中“”表示相连的物质能相互反应,“→”表示种物质转化成另一种物质(部分反应物、生成物及反应条件已略去)。请回答下列问题:
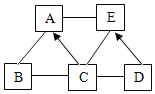
(1)物质 E 是_____。
(2)写出下列反应的化学方程式:A+E:__________;B+C:________________。
(3)图中相互关系涉及基本反应类型有_____种。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】炼铁产生的废渣中含有大量CuS及少量铁和铁的化合物,工业上以该废渣为原料生产CuCl2的流程如图所示。
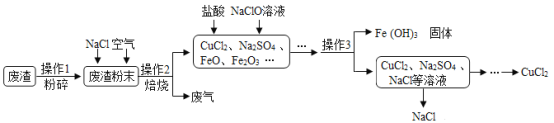
(1)NaClO中氯元素的化合价是____________________。
(2)操作1:粉碎。粉碎的目的是____________________。
(3)操作2:焙烧。高温条件下,通入空气,CuS和NaCl反应生成了CuCl2和Na2SO4,化学方程式为:__________________。
(4)操作3:__________(填操作名称),进行该操作时玻璃棒的作用是_______________。
(5)流程图中能循环利用的物质是______________________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】铝元素的相关信息如图所示,下列叙述正确的是( )
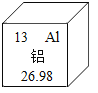
A.铝原子的最外层电子数为 3B.铝原子的核内中子数为 13
C.铝是地壳中含量最高的元素D.自然界中铝主要以单质形式存在
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】铁及其化合物的有关知识
(一)铁及其化合物的应用
1如图1为某小儿硫酸亚铁糖浆。适当服用该糖浆可治疗_____(选填序号)。
A佝偻病
B侏儒症
C贫血症
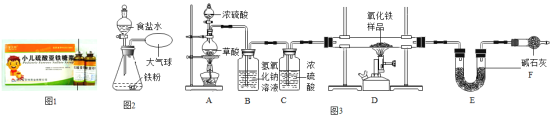
2食品保鲜“双吸剂”含铁粉、食盐等,如图2为其原理探究实验: 滴入食盐水后,关闭分液漏斗活塞。一段时间后,铁粉上出现红色固体,气球_______(选填“变大”、“不变”或“变小”)。食盐水的作用是_______。
(二)铁及其化合物的实验
某化学兴趣小组在实验室中模拟工业炼铁的原理,并探究CO与Fe2O3反应后的产物。
[查阅资料]:
草酸(H2C2O4) 固体与浓硫酸混合加热会产生一氧化碳,反应方程式为:
②NaOH溶液可以吸收二氧化碳,浓硫酸是一种常用的干燥剂,碱石灰既能吸收二氧化碳也能吸水。于是他设计了如图3的实验装置,结合装置回答下列问题:
1图中装置C作用是______;
2从实验操作程序和实验安全看,首先要检查装置的气密性,实验开始先加热_______(填A或D)处。
3该装置设计有一个明显缺陷,你认为是_______。
4将Fe粉溶于稀H2SO4,用点燃法检验生成的H2前必须_____。向反应后的溶液中滴加NaOH溶液,生成白色Fe(OH)2沉淀,随后沉淀变为灰绿色。白色沉淀变为灰绿色的原因之一是部分Fe(OH)2接触空气生成Fe(OH)3,反应的化学方程式_____。生成的Fe(OH)3分解为Fe2O3。过滤、洗涤、低温干燥得到灰绿色固体,其组成为2FeSO4·2Fe(OH)2·Fe2O3[相对分子质量为644]。
(三)灰绿色固体的热分解实验
兴趣小组称取此固体6.44g,在科研人员的指导下用下图装置进行热分解实验。
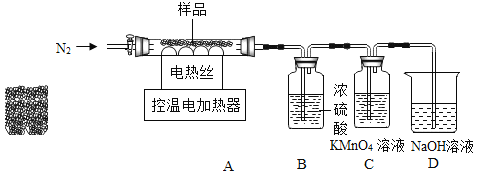
[查阅资料]①Fe(OH)2在150℃~200℃时完全分解为FeO;
②FeSO4在450℃~ 500℃时完全分解为Fe2O3,
![]()
1加热前后及过程中均通入N2,加热结束后仍通一段时间N2的目的是________。
2控制温度在不同的范围对A中样品加热。测得剩余固体质量随温度的变化如图所示。B装置中浓硫酸只能吸收SO3和H2O,当加热到t1℃时,装置C中的现象为______。
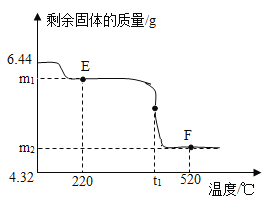
①图中E点对应的m1=_____。
②图中F点对应物质中Fe2O3的质量为___g。
③科研人员将F点所得剩余固体隔绝空气,在密闭容器中加热到1400℃,已知加热过程中发生反应,且反应前后固体总质量不变,得到纯净的化合物。请写出该化合物的化学式______。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com