
| A. | 84:85:79 | B. | 1:1:1 | C. | 23:24:18 | D. | 1:1:5 |
科目:初中化学 来源: 题型:选择题
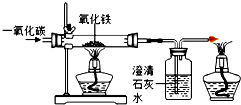
| A. | 实验开始时,应该先通入一氧化碳,一段时间后再点燃酒精灯加热氧化铁 | |
| B. | 实验过程中,试管中澄清的石灰水变浑浊,证明该反应有二氧化碳生成 | |
| C. | 实验结束后,玻璃管中红色的氧化铁粉末变成黑色,该产物不一定是铁 | |
| D. | 该反应中,一氧化碳转化为无毒无害的二氧化碳,故不需要尾气处理装置 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
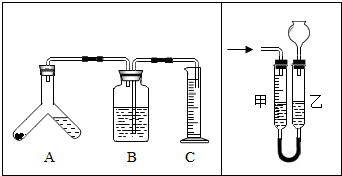 实验室利用如图装置测量锌的相对原子质量.ag锌与H2SO4反应(设锌全部参加反应,产生气体在量程范围内,气体的密度为0.089 3g/L).请回答下列问题.
实验室利用如图装置测量锌的相对原子质量.ag锌与H2SO4反应(设锌全部参加反应,产生气体在量程范围内,气体的密度为0.089 3g/L).请回答下列问题.查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题

查看答案和解析>>
科目:初中化学 来源: 题型:解答题
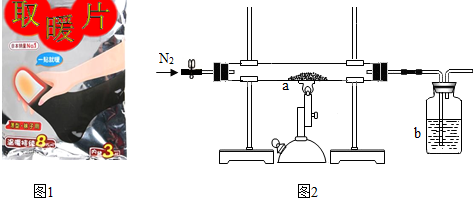
| 反应时间 | t0 | t1 | t2 | t3 | t4 |
| 烧杯和药品质量/g | 25.7 | 25.6 | 25.5 | 25.5 | m |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com