
【题目】某化学兴趣小组的同学想要探究一包长期敞口放置的氢氧化钠固体的成分.
![]() 经测定该固体已经部分变质,其成分是 ______
经测定该固体已经部分变质,其成分是 ______ ![]() 写化学式
写化学式![]() .
.
![]() 请你从石灰水、氯化钙溶液和无色酚酞试液中选择合适的试剂,设计实验来验证该固体样品中仍然存在NaOH: ______,______ .
请你从石灰水、氯化钙溶液和无色酚酞试液中选择合适的试剂,设计实验来验证该固体样品中仍然存在NaOH: ______,______ .
![]() 该小组同学又通过实验测定了样品的变质程度,实验数据如下图所示,试计算:该样品中氢氧化钠的质量分数?
该小组同学又通过实验测定了样品的变质程度,实验数据如下图所示,试计算:该样品中氢氧化钠的质量分数?![]() 数据精确至
数据精确至![]() _____
_____
![]()
【答案】NaOH和Na2CO3 氯化钙溶液 无色酚酞试液 15.2%
【解析】
(1)氢氧化钠溶液能够吸收空气中的二氧化碳,氢氧化钠和二氧化碳反应能生成碳酸钠和水,其成分是NaOH和Na2CO3混合物;
(2)为进一步探究是否全部变质,另取少量固体加水溶解后,加入过量的氯化钙溶液,碳酸钠能够和显中性的氯化钙溶液反应生成碳酸钙沉淀和氯化钠,完全反应后过滤,往滤液中滴加酚酞溶液,若酚酞溶液变红色,说明药品存在碳酸钠和氢氧化钠,即氢氧化钠部分变质.
(3)碳酸钠能与盐酸反应生成了二氧化碳,根据质量守恒定律,生成二氧化碳的质量=25g+280g-296.2g=8.8g;
烧碱样品中碳酸钠的质量为x,
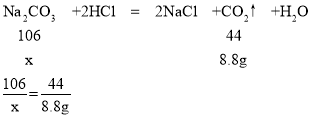
x=21.2g
样品中氢氧化钠的质量分数是=![]() ×100%=15.2%
×100%=15.2%
答:样品中氢氧化钠的质量分数是15.2%。
故答案为:
(1)NaOH和Na2CO3;
(2)氯化钙溶液;无色酚酞试液;
(3)15.2%.


 每日10分钟口算心算速算天天练系列答案
每日10分钟口算心算速算天天练系列答案科目:初中化学 来源: 题型:
【题目】金属及其化合物在生活生产中有重要的应用,请回答下列问题。
(1)某“取暖片”中发热剂的主要成分有铁粉、活性炭、氯化钠和水等,其中氯化钠的作用是_____。月饼包装袋内也会有一包铁粉,是“双吸剂”,吸收的物质是_____。
(2)工业上利用铝热反应焊接钢轨间的缝隙,焊接时人们常将铝粉与氧化铁混合在高温下反应,置换出的铁以熔融态形式流入铁轨的缝隙。该反应的化学方程式为_____。
(3)钛具有熔点高、密度小、抗腐蚀性强、与人体相容性好等优点被广泛地应用,称为“未来金属”,下列有关金属钛的用途不切实际的是_____。
①作保险丝 ②作人造骨头 ③制造炊具 ④制作轮船外壳
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】下图是甲、乙、丙三种固体物质的溶解度曲线。下列叙述错误的是
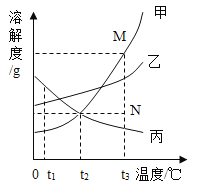
A.t1℃时,三种物质的溶解度大小顺序为:丙>乙>甲
B.t2℃时,甲、丙两种物质的溶液中溶质的质量分数相等
C.若甲物质中混有少量的乙物质,可用降温结晶的方法提纯甲
D.若要将组成在N点的甲溶液转变为M点的甲溶液,可以采用恒温
蒸发溶剂的方法
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】下列实验中溶液的pH 随加入试剂体积而变化的关系与图相符的是
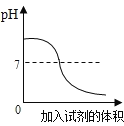
A.稀硫酸中不断滴入NaOH 溶液
B.NaCl 溶液中不断滴入稀盐酸
C.Na2CO3 溶液中不断滴入稀盐酸
D.NaOH 溶液中不断滴入蒸馏水
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】科学方法对化学学习起着事半功倍的作用。
(一) 微观粒子模型化是研究化学变化的重要方法。
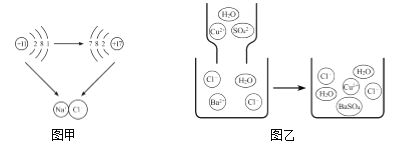
(1) 图甲是钠与氯气反应生成氯化钠示意图。该图说明在化学反应过程中一定发生变化的是_____(填序号)。
a.原子核 b.原子的最外层电子数 c.原子的电子层数
(2)图乙是硫酸铜溶液与氯化钡溶液反应的示意图。该反应的实质是A+B→C,请用微粒符号表示该反应的实质_________________________________________________________。
(二) 控制变量、设计对比实验是实验探究的重要方法。
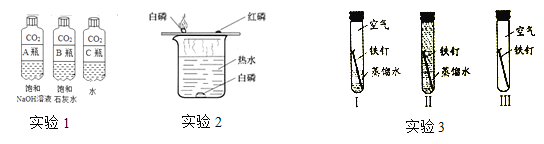
(3)实验1振荡3个塑料瓶,观察到塑料瓶变瘪的程度由大到小为_______________________(用A、B、C填写),其中变浑浊的瓶内发生反应的化学方程式为 __________;对比A瓶与______(填“B”或”C”)瓶的实验现象,可证明CO2能与NaOH发生反应。
(4)实验2探究物质燃烧的条件。将大小相同的红磷和白磷放在薄铜片的两侧,加热铜片的中部,观察现象。通过此实验,可说明燃烧的条件之一的是_____________(填序号)。
A.可燃物 B.空气 C.温度达到着火点
(5)实验3是探究铁钉条件的实验,会出现明显现象的是试管______(填“I”“II”或“III”),说明铁生锈实际上是铁与____________________________________发生反应。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】已知反应前后有元素化合价改变的反应统称为氧化—还原反应,如图为反应类型的关系图,下列有关说法正确的是 ( )
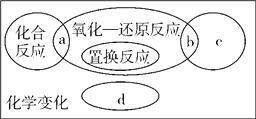
A. CO2+H2O=== H2CO3属于a处的反应
B. 2H2O![]() 2H2↑+O2↑属于氧化—还原反应
2H2↑+O2↑属于氧化—还原反应
C. c处反应后物质的质量一定减小,不符合质量守恒定律
D. 任何两种化合物之间发生反应都属于d
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】无水氯化钙在工业上有广泛的用途。以石灰石矿粉(含有SiO2、Fe2O3 、MgSO4等杂质)为原料,生产无水氯化钙的流程如图:
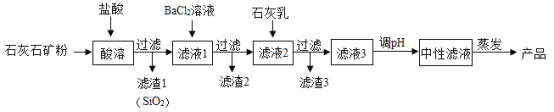
回答下列问题:
(1)从流程图中推知:SiO2具有的化学性质是________________。
(2)加入盐酸的主要作用是______________ ( 写化学方程式);
(3)滤渣3中除有Ca(OH)2外、还有_______________。(填化学式);
(4)产品中的杂质除极少量H2O外,最可能含的是______________ (填化学式)。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】用铝土矿(主要含SiO2、Al2O3和少量Fe2O3等)制取铝硅合金材料有干法、湿法等方法,其中干法制备的工艺流程如图所示。
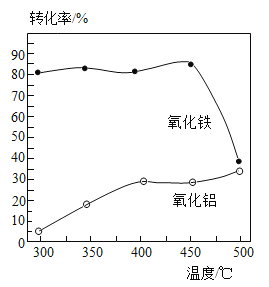
(已知:I.SiO2不溶于水、不与硫酸反应。Ⅱ.转化率是反应物转化为生成物的百分率。)
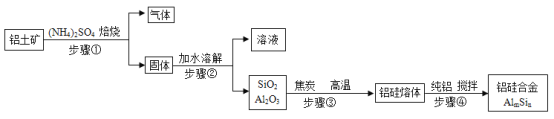
(1)铝硅合金的硬度比纯铝的硬度_______。
(2)步骤①中焙烧除铁的反应为:4(NH4)2SO4+Fe2O3![]() 2NH4Fe(SO4)2+3H2O+6NH3↑(Al2O3部分发生类似反应,SiO2不发生类似反应)。已知Fe2O3、Al2O3转化为硫酸盐的转化率与温度的关系如图所示,则焙烧除铁最适宜的温度为_______℃。
2NH4Fe(SO4)2+3H2O+6NH3↑(Al2O3部分发生类似反应,SiO2不发生类似反应)。已知Fe2O3、Al2O3转化为硫酸盐的转化率与温度的关系如图所示,则焙烧除铁最适宜的温度为_______℃。
(3)步骤②中包括加水溶解、_______、洗涤等操作。
(4)步骤③中利用焦炭还原SiO2、Al2O3会产生中间体SiC、Al4C3.写出高温下Al4C3与Al2O3反应生成A1和CO的化学方程式:_______。
(5)若用湿法处理铝土矿,加过量的硫酸浸取,所得溶液中的阳离子有_______。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】金属具有广泛的应用。
(1)下列金属制品中,利用金属导热性的是_____(填字母)。
A 金属硬币 B 铝制导线 C 铜制火锅
(2)波尔多液是一种农业上常用的杀菌剂,它由硫酸铜、生石灰加水配制而成,不能用铁质容器配制波尔多液的原因是_____(用化学方程式表示)。
(3)向一定质量AgNO3和Fe(NO3)2的混合溶液中插入一块足量的Zn片,其中固体质量随反应时间变化的情况如图所示。下列说法正确的是_____。
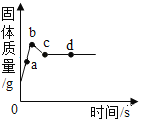
A a点时,溶液中金属离子有Ag+、Fe2+、Zn2+,Zn片表面析出金属单质有Ag、Fe
B 图标上b~c段质量减少的原因是Zn与Fe(NO3)2溶液反应
C b点时溶液中金属离子只有Fe2+,溶液颜色为浅绿色
D c点和d点对应溶液均为无色
E c点和d点溶液中金属离子的种类不同,Zn片表面析出金属单质种类相同
(4)在已经平衡的托盘天平两端各放着装有等质量、等浓度的足量稀盐酸。将一定质量的锌放入左盘烧杯中,往右盘烧杯中投入与锌等质量的铜铝合金,充分反应后天平依然保持平衡,则铜铝合金中铜与铝的质量比为_____。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com