
【题目】实验小组用传感器探究稀NaOH 溶液与稀盐酸反应过程中温度和 pH 的变化,测定结果如(如下图所示)。下列说法错误的是( )
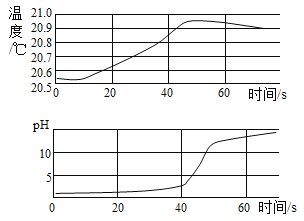
A.反应过程中有热量放出
B.该实验是将稀NaOH 溶液滴入稀盐酸
C.30s 时,溶液中溶质为HCl 和NaCl
D.40s 时,氢氧化钠与盐酸恰好完全反应
科目:初中化学 来源: 题型:
【题目】化学实验室里,同学们准备研究氢氧化钠能与二氧化碳反应的化学性质。
①在配制NaOH溶液时,看到盛有NaOH固体的试剂瓶上标注着“NaOH含量不少于96.0%”,便对该瓶试剂成分产生了质疑:
[提出问题]氢氧化钠中含有什么杂质?
[查阅资料]工业上制取NaOH的反应原理: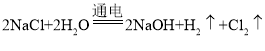 然后蒸发溶剂获得NaOH固体(在化工生产中,原料往往不能完全转化为产品)。
然后蒸发溶剂获得NaOH固体(在化工生产中,原料往往不能完全转化为产品)。
[提出猜想]
甲同学认为杂质只有氯化钠;
乙同学认为杂质还可能含有碳酸钠,原因为_______ (用化学方程式表示)。
[设计实验]取样溶于水,并分成两份。
步骤1:向一份溶液中滴加酚酞试液,溶液变_________色。
步骤2:向另一份溶液中滴加过量稀硝酸,有气泡产生。
步骤3:向步骤 2所得溶液中继续滴加_________溶液,发现有白色沉淀产生。
[实验结论]乙同学的猜想正确。
请
Ⅰ.上述实验中步骤_____(填序号)是没有必要进行的。
II.步骤2所得溶液中的溶质有________。
②同学们在配制好的氢氧化钠溶液中通入CO2气体,没有明显现象,于是设计了如下实验证明反应的发生:(不考虑氢氧化钠中的极少量杂质)
实验1 | 实验2 | 实验3 |
现象:烧杯中溶液几乎充满整个试管。 |
现象: 充分反应后,红墨水最终呈现左高右低现象。 |
现象: 滴加试剂X后,溶液中出现大量白色沉淀。 |
I .实验3中加入的试剂X是_______ (任写一种符合要求的试剂)。
II.实验1、2在设计思想上是一致的,都是通过验证反应物的消耗才能观察到明显现象,但有同学对实验1提出了质疑,他认为这个实验不足以证明CO2与NaOH发生了化学反应,其理由是_______。
Ⅲ.查阅资料:室温下,氢氧化钠易溶于酒精,而碳酸钠难溶于酒精。据此,同学们设计了实验4,请你补充完整。
实验4步骤 | 实验现象 | 实验结论 | 实验分析 |
将CO2气体不断地通入氢氧化钠酒精溶液中,观察现象。 | _______ | 氢氧化钠与二氧化碳确实发生了化学反应。 | 实验4与实验____(填实验序号)的设计思想是一致的,都是根据生成物的性质才能观察到明显现象。 |
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】认识物质及其变化,对于了解自然现象和规律至关重要。
(1)下列是初中化学常见的实验或操作,回答下列问题:
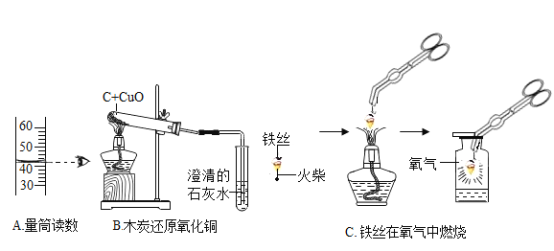
①A实验中读出液体的体积为_____mL。
②B实验中观察到的实验现象是_____。
③C实验集气瓶内预先装入少量的水的目的是_____,铁丝燃烧的化学方程式为_____。
(2)在烧杯中加入5.74g久置于空气中的铝箔,再滴加稀硫酸,放出气体的质量与所加稀硫酸质量的关系如图所示。请回答下列问题:
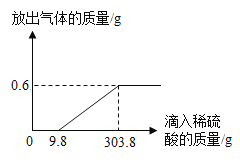
①产生氢气(H2)的总质量为_____;
②刚滴加稀硫酸时无氢气放出,是因为稀硫酸与铝箔表面的物质_____(填化学式)反应,该物质与稀硫酸反应的化学方程式为_____。
③请计算铝箔中含有金属铝的质量_____。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】金属在生产、生活中有着广泛的应用。
(1)保护金属资源的有效途径之一是防止金属锈蚀。自行车的链条常采用的防锈方法是___________。铁制品一旦生锈,可用稀硫酸除铁锈,请写出相应的化学方程式___________。
(2)铁是年产量最高的金属,工业上用赤铁矿(主要成分是氧化铁)炼铁的化学反应原理用化学方程式表示为___________。
(3)将一定质量的锌粉和铁粉放入硝酸镁和硝酸银的混合溶液中,充分反应后过滤所得滤液中一定含有的阳离子___________(写离子符号),向滤渣中加入稀盐酸,如果有气泡产生,滤渣中一定有___________(写化学式)。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】溶液在生活、生产中具有广泛的用途。
(1)海水中含量最多的物质是_______。生活中,常采用__________的方法降低水的硬度。
(2)如果不慎将浓硫酸沾到皮肤或衣服上,应立即用大量水冲洗,然后再涂上 3%~5%的______溶液。
(3)农业上常用溶质质量分数为 16%的氯化钠溶液来选种,良种会下沉,次种会漂浮。
①室温下氯化钠的溶解度约为 36 g。上述选种用的氯化钠溶液是_______ (填“饱和”或“不 饱和”)溶液。
②若用溶质质量分数为 24%的 NaCl 溶液和蒸馏水来配制 300g 溶质质量分数为 16%的 NaCl溶液,则所需 24%的NaCl 溶液与蒸馏水的质量比为_______________。
(4)甲、乙两种不含结晶水的固体物质的溶解度曲线如图所示。
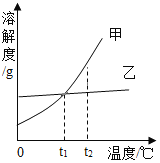
①t1℃时,甲溶液的溶质质量分数与乙溶液的溶质质量分数相比,前者与后者的关系是_________(填字母)。
a.大于 b.小于 c.等于 d.无法确定
②要从含有少量乙的甲溶液中得到较多的甲,通常可采用____ 的方法(填“蒸发结晶”或“降温结晶”)。
③等质量的甲、乙分别配成t2℃时的饱和溶液,需要水的质量:甲______乙(填“>”、“=”或“<”)。
(5)不同压强下,气体 A 的溶解度随温度的变化如图所示,图中p1 对应 的压强为 202kPa, 则p2对应的压强为________(填字母)。
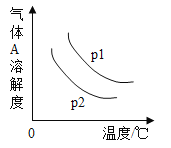
a.大于 202kPa b.小于 202kPa c.无法确定
(6)实验室用溶质质量分数为 5%的过氧化氢溶液制取氧气,若要得到 1.6g氧气,至少需要过氧化氢溶液的质量是多少?(利用化学方程式进行计算,在答题纸上写出计算过程) __________
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】实验室制取 CO2,并验证 CO2 和 CO 的性质的式样(如下图所示),请回答问题:

Ⅰ.写出标有序号的仪器名称①______②_____
Ⅱ. 能证明 CO 具有还原性的实验现象为_____,化学方程式为_____; E 处放一点燃的酒精灯的目的是_____
Ⅲ.写出 A 中反应的化学方程式_____,实验结束时,先停止 B、C 处的加热,继续通一会A 中产生的气体,其目的是_________
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】a、b、c三种不含结晶水的物质的溶解度曲线如图,下列说法正确的是( )
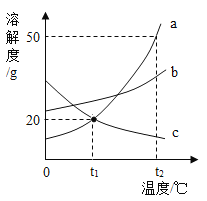
A. a的溶解度大于b的溶解度
B. 将a的溶液由![]() 降温到
降温到![]() ,一定有晶体析出
,一定有晶体析出
C. ![]() 时,50g的a溶于50g水,溶液的质量分数为
时,50g的a溶于50g水,溶液的质量分数为![]()
D. c的饱和溶液由![]() 降温到
降温到![]() ,溶液的质量分数不变
,溶液的质量分数不变
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】分析以下化学反应的微观示意图,判断有关说法正确的是( )
A. 反应前后各物质均属于氧化物
B. 参加反应的两种物质的分子个数比为2:3
C. 该反应中各元素的化合价均发生了改变
D. 在化学反应中,分子可以再分,原子不可再分
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】为测定某样品中锌的质量分数,取10g此样品,分五次向其中加入稀硫酸使之充分反应(假设锌的样品中杂质不与稀硫酸反应,且不溶于水),每次加入的稀硫酸质量及测定剩余固体的质量,记录数据如下表:
第一次 | 第二次 | 第三次 | 第四次 | 第五次 | |
加入稀硫酸的质量/g | 10 | 10 | 10 | 10 | 10 |
剩余固体质量/g | 8.4 | 6.8 | 5.2 | 3.6 | 3.6 |
请认真分析表中的数据,回答下列问题:
(1)表示样品与稀硫酸恰好完全反应的是上表中第________次操作;
(2)计算样品中锌的质量分数; ____
(3)计算实验中所用稀硫酸的溶质质量分数。 ______
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com