
分析 (1)根据建立的假设为袋内气体可能是二氧化碳,进行分析解答.
(2)根据二氧化碳的检验方法,结合二氧化碳能使澄清的石灰水变浑浊,进行分析解答.
解答 解:(1)由题意,建立的假设为袋内气体可能是二氧化碳,则他提出的问题是包装袋内充的是什么气体呢?
(2)将燃着的木条伸入已收集满该气体的集气瓶中,即使木条熄灭,也不能证明气体是二氧化碳,因为氮气等气体也能使木条熄灭.二氧化碳能使澄清的石灰水变浑浊,正确的实验方案是:将收集的该气体通入到澄清石灰水中,若澄清的石灰水变浑浊,说明假设是正确的.
故答案为:(1)包装袋内充的是什么气体呢?
(2)澄清石灰水中.
点评 本题难度不大,将常见气体的性质与生活应用相联系,体现了化学就在我们身边,掌握常见气体的性质与检验方法是正确解答本题的关键.


 名牌学校分层周周测系列答案
名牌学校分层周周测系列答案 黄冈海淀全程培优测试卷系列答案
黄冈海淀全程培优测试卷系列答案科目:初中化学 来源: 题型:解答题
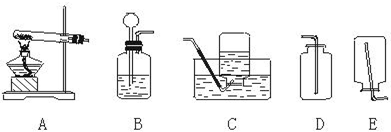
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题

查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 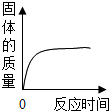 加热分解高锰酸钾 | B. | 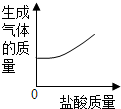 在变质的NaOH溶液中滴加稀盐酸 | ||
| C. | 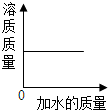 稀释NaCl溶液 | D. | 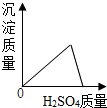 将H2SO4滴入BaCl2溶液中 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 食品包装中填充氮气以防腐、防压 | |
| B. | 用烧灼并闻气味的方法区别羊毛线和棉线 | |
| C. | 发酵面团时加入适量小苏打以提升口感和除去酸味 | |
| D. | 用甲醛溶液浸泡水产品来保鲜 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 氮气----可做食品防腐剂 | B. | 氢气----可支持燃烧 | ||
| C. | 稀有气体----可制作霓虹灯 | D. | 二氧化碳----可以灭火 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com