
| ���������� | ���� | |
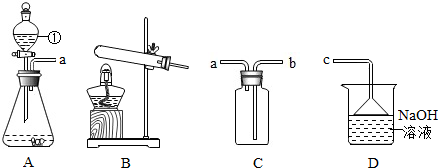
| A | N2��O2��CO2������ | ��ȼ�ŵ�ľ�����飬�۲�ľ��ȼ����� |
| B | CO��CH4 | ��ȼ��֤������Ƿ���ʹ����ʯ��ˮ����ǵ����� |
| C | ����ͭ��̼�� | �۲���ɫ�ķ�������ɫ��Ϊ̼�� |
| D | ��ˮ��Ӳˮ | �������ˮ���裬�۲������ĭ�Ķ��� |
| A�� | A | B�� | B | C�� | C | D�� | D |
���� �������ʵļ����ܽ��������������ʶ����ֳ�����Ҫ��ʹ�ø÷������м���ʱ�����������ʻ�������Բ�ͬ��ʵ���������ܽ��м���
��� �⣺A��ȼ�յ�ľ��������ƿ�����У�ʢ��N2��CO2��ƿ����ʹȼ�յ�ľ��Ϩ�𣬸÷���������������������壻
B��ȡ��Ʒ����ȼ���������������̼ʹ�����ʯ��ˮ����ǣ�������ͬ�����ܼ���
C������ͭ��̼�۶��Ǻ�ɫ�Ĺ��壬���ܼ���
D���ӷ���ˮ�����裬����Һ����ĭ���ٲ�ͬ����ĭ�ḻ��Ϊ��ˮ����ĭ�ٵ�ΪӲˮ���������ֳ�����
��ѡ��Ϊ��D��
���� ���⿼���˳������ʵļ����ڽ������ʱ�����ȷ������������ʵ����ʣ�Ȼ��ѡ���ʵ����Լ��ͷ��������ֲ�ͬ�����ɼ���


 ������ʱͬ����ϰ��ϵ�д�
������ʱͬ����ϰ��ϵ�д� ѧҵ����һ��һ��ϵ�д�
ѧҵ����һ��һ��ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ˮͨ��ֽ� | B�� | ��ѩ���� | C�� | �������� | D�� | ֲ�������� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������

| ʵ������ | ��ʵ������Ľ��� |
| ��1��a�Թ��а���ȼ�գ���ˮ�а���û��ȼ�� ��2��b�Թ��к���û��ȼ�� | ��1����ˮ�а���û��ȼ�յ�ԭ���� û������������������Ӵ� ��2��b�Թ��к���û��ȼ�յ�ԭ���� �¶�δ�ﵽ�����Ż�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
 ��
�� ��
�� ��
�� �ֱ��ʾ���к��в�ͬ��������ԭ�ӣ�����ͼʾ�ش�
�ֱ��ʾ���к��в�ͬ��������ԭ�ӣ�����ͼʾ�ش�
 =2��1��������ʾ��ͼ��ʾ�μӷ�Ӧ�ķ�Ӧ�
=2��1��������ʾ��ͼ��ʾ�μӷ�Ӧ�ķ�Ӧ� ��ͼ��ʾ�μӷ�Ӧ�ķ�Ӧ�ﹹ�ɵ����ʲ�һ�����һ����������һ������һ���������Ǹ÷�Ӧ�Ĵ�����
��ͼ��ʾ�μӷ�Ӧ�ķ�Ӧ�ﹹ�ɵ����ʲ�һ�����һ����������һ������һ���������Ǹ÷�Ӧ�Ĵ�����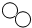 ��
��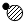 ��
�� ��
�� ��
��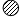 ��
�� ��
�� ��
��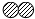
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com