
【题目】“鱼浮灵”主要成分是过碳酸钠(xNa2CO3yH2O2),俗称固体双氧水。兴趣小组对其进行以下探究:
[性质探究]
(1)取少量“鱼浮灵”于试管中加水,有持续细小气泡缓慢放出;向试管中加入少量MnO2粉末,产生大量气泡。将带火星木条伸入试管,木条________,说明有O2生成。在该反应中,MnO2粉末的作用是______。
(2)取实验(1)中上层清液,测得溶液pH>7;向溶液中滴加足量稀盐酸,产生大量气泡;将产生的气体通入澄清石灰水中,出现浑浊现象,说明有__________生成。
结论:过碳酸钠具有Na2CO3和H2O2的双重化学性质。
[工业制备]
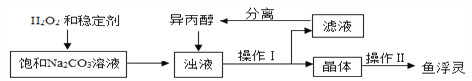
【查阅资料】异丙醇为有机溶剂,水与异丙醇可以互溶,过碳酸钠在异丙醇中溶解度较小。
(3)稳定剂中MgCl2和Na2SiO3发生复分解反应,生成一种难溶物将过碳酸钠粒子包裹住,该反应的化学方程式为_______________________。
(4)浊液中加入异丙醇的作用是______________________。
(5)操作Ⅱ中洗涤晶体的试剂最好选用___________(填字母)。
A.饱和NaCl溶液 B.水 C.异丙醇 D.稀盐酸
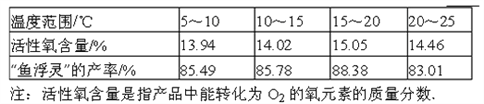
(6)根据下表数据,你认为上述制备反应的最佳温度范围是_________℃。
[组成测定]利用下图装置进行产品中活性氧含量测定和过碳酸钠(xNa2CO3yH2O2)组成的测定(杂质对测定无影响)。
查阅资料:①“鱼浮灵”中活性氧含量≥13.0%是一等品,≥10.5%是合格品。
②过碳酸钠能与酸反应放出CO2和O2。
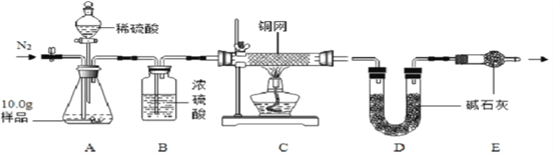
(7)实验前先缓慢通N2一段时间,加热铜网至红热后,再缓慢滴入过量稀硫酸,C装置中发生反应的化学方程式是__________________ ;A中样品完全反应后,继续缓慢通N2,其目的是_________________________。
(8)若先滴入稀硫酸,后加热铜网,会导致x:y的值________(填“偏大”或“偏小”)。
(9)装置B中浓硫酸的作用是________
(10)实验测得C装置中铜网增重1.2g,D装置增重2.2g。该产品中活性氧含量为______%;属于________(填“一等品”或“合格品”);x:y=________。
【答案】 复燃 催化作用 CO2(或二氧化碳) MgCl2+Na2SiO3=MgSiO3↓+2NaCl 降低过碳酸钠的溶解度(或减少过碳酸钠的溶解或提高产率等) C 15~20 2Cu+O2![]() 2CuO 使残留在装置中的气体全部被吸收 偏大 干燥气体 12 合格品 2:3
2CuO 使残留在装置中的气体全部被吸收 偏大 干燥气体 12 合格品 2:3
【解析】由题中信息知,“鱼浮灵”主要成分是过碳酸钠(xNa2CO3yH2O2),俗称固体双氧水。[性质探究] (1)取少量“鱼浮灵”于试管中加水,有持续细小气泡缓慢放出;向试管中加入少量MnO2粉末,产生大量气泡。将带火星木条伸入试管,木条复燃,,说明有O2生成。在该反应中,MnO2粉末的作用是催化作用 。 (2)取实验(1)中上层清液,测得溶液pH>7;向溶液中滴加足量稀盐酸,产生大量气泡;将产生的气体通入澄清石灰水中,出现浑浊现象,说明有二氧化碳生成。结论:过碳酸钠具有Na2CO3和H2O2的双重化学性质。[工业制备]
【查阅资料】异丙醇为有机溶剂,水与异丙醇可以互溶,过碳酸钠在异丙醇中溶解度较小。(3)稳定剂中MgCl2和Na2SiO3发生复分解反应,生成一种难溶物将过碳酸钠粒子包裹住,该反应的化学方程式为MgCl2+Na2SiO3=MgSiO3↓+2NaCl 。(4)浊液中加入异丙醇的作用是降低过碳酸钠的溶解度(或减少过碳酸钠的溶解或提高产率等)。(5)操作Ⅱ中洗涤晶体的试剂最好选用C.异丙醇,因水与异丙醇可以互溶,过碳酸钠在异丙醇中溶解度较小。(6)根据下表数据,制备反应的最佳温度范围是15~20℃。[组成测定] ①“鱼浮灵”中活性氧含量≥13.0%是一等品,≥10.5%是合格品。②过碳酸钠能与酸反应放出CO2和O2。(7)实验前先缓慢通N2一段时间,加热铜网至红热后,再缓慢滴入过量稀硫酸,C装置中发生反应的化学方程式是2Cu+O2 ![]() 2CuO;A中样品完全反应后,继续缓慢通N2,其目的是使残留在装置中的气体全部被吸收。(8)若先滴入稀硫酸,后加热铜网,会导致x:y的值偏大。(9)装置B中浓硫酸的作用是干燥气体。(10)实验测得C装置中铜网增重1.2g,D装置增重2.2g。该产品中活性氧含量为∶
2CuO;A中样品完全反应后,继续缓慢通N2,其目的是使残留在装置中的气体全部被吸收。(8)若先滴入稀硫酸,后加热铜网,会导致x:y的值偏大。(9)装置B中浓硫酸的作用是干燥气体。(10)实验测得C装置中铜网增重1.2g,D装置增重2.2g。该产品中活性氧含量为∶![]() ×100%=12%。属于合格品。生成氧气质量为1.2g,生成二氧化碳质量为2.2g。
×100%=12%。属于合格品。生成氧气质量为1.2g,生成二氧化碳质量为2.2g。
2xNa2CO3yH2O2+2xH2SO4=2xNa2 SO4+2xCO2↑+2﹙x+y﹚H2O+yO2↑.
88x 16y
2.2g 1.2g
![]() =
=![]() , x:y=2:3.
, x:y=2:3.
点睛∶本题主要考查过碳酸钠(xNa2CO3yH2O2)制备和性质。


 导学与测试系列答案
导学与测试系列答案 新非凡教辅冲刺100分系列答案
新非凡教辅冲刺100分系列答案科目:初中化学 来源: 题型:
【题目】用化学用语填空:
(1)2个硫酸根离子________; (2)体温计中(熔点最低)的金属元素是____________;
(3)标出氧化铁中铁元素的化合价_________;(4)3个氮分子________________;
(5)写出下列物质的名称
①FeCl2_______________;②(NH4)2SO4_____________;③HNO3______________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】按要求写出下列化学方程式。
(1)初中化学涉及到二氧化碳的化学反应有很多,请任写一个有二氧化碳参加的化合反应
(2)向装有某无色溶液A的试管中加入固体B后,观察到有无色气泡产生。请写出符合该现象的一个化学方程式 ;
(3)实验室用澄清石灰水检验二氧化碳的化学方程式 ;
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】下列关于空气的说法中错误的是
A.空气是人类宝贵的自然资源 B.空气中的氮气常用作保护气
C.空气中的稀有气体常用作灭火剂 D.空气中的氧气的主要来自植物的光合作用
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】【2016年湖南省邵阳市】近年来,部分城市因空气污染而出现了严重的雾霾天气,下列做法不利于减少空气污染的是( )
A.减少化石燃料的使用 B.提倡居民驾驶私家车出行
C.积极植树、造林、种草 D.提倡使用太阳能灯清洁能源
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】如图是甲、乙、丙三种物质的溶解度曲线,回答下列问题:
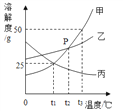
(1)P点表示的意义是__________________________。
(2)t3℃时,50g甲物质溶解在50g水中,得到溶液的质量是____________。
(3)甲、乙、丙三种物质的饱和溶液从t2℃降低到t1℃时,得到的三种物质的质量分数从大到小的顺序是______________。
(4)要使丙物质的饱和溶液变为不饱和溶液,在不改变物质的组成条件下,应采取的方法是______________。
(5)下列说法正确的是 (_____)
A.P点是表示在t2℃时,甲、乙的质量分数相等
B.t3℃时,在100g水中最多溶解50g的甲物质
C.t1℃时,在50g水中加入15ga物质,得到溶液65g
D.甲的溶解度大于丙的溶解度
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】实验室中的试剂一般要密封保存,否则可能会与空气接触而变质。某研究性学习小组发现一瓶未密闭的KOH固体,对其成分提出以下假设,并完成了实验探究。
资料:KOH的化学性质与NaOH的相似,CaCl2溶液呈中性。
假设1:只含KOH; 假设2:含KOH和K2CO3; 假设3:只含K2CO3
(1)成分中可能含有K2CO3的原因是(用化学方程式回答)________________________。
(2)取少量样品于试管中,加入足量稀盐酸,观察到________,说明假设2或假设3成立。
(3)进一步探究的过程如图-10:
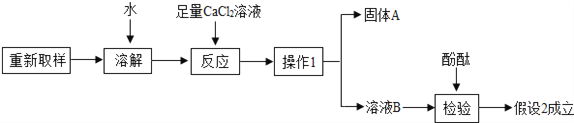
图-10
①“操作1”的名称是____________。
②加入足量CaCl2溶液的作用是_______________________________。
(4)变质试剂也有利用价值,从KOH和K2CO3的组成和性质看,这瓶变质试剂的用途是________(写出一条)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com