
【题目】如图是几种实验室制取气体的发生装置与收集装置。
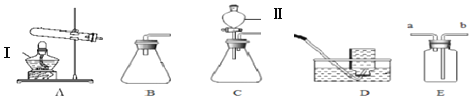
(1)写出仪器名称Ⅰ_____,Ⅱ_____。
(2)实验室可用双氧水与二氧化锰制取氧气。若要较好地控制产生氧气的速度,应选用的发生装置是_____,(填编号),反应的化学方程式是_____,二氧化锰在该反应中的作用是_____。实验室还可以用高锰酸钾制取氧气,应选用的制取并收集装置_____,(填编号),反应的化学方程式是_____。选用D装置收集氧气的原因_____。
(3)D装置收集氧气,操作的正确顺序为_____(填编号)。
a.将导管伸入集气瓶口,气体进入瓶中
b.将装满水的集气瓶倒置在水槽中
c.当气体收集满时,用毛玻璃片盖上瓶口,将集气瓶移出水面瓶口朝上放置
(4)若用装满水的E装置收集氧气,气体应从_____(填“a”或“b”)端通入。
【答案】酒精灯 分液漏斗 C 2H2O2![]() 2H2O+O2↑ 催化作用 AD或AE 2KMnO4
2H2O+O2↑ 催化作用 AD或AE 2KMnO4![]() K2MnO4+MnO2+O2↑ 氧气不易溶于水 bac a
K2MnO4+MnO2+O2↑ 氧气不易溶于水 bac a
【解析】
(1)仪器Ⅰ是酒精灯,Ⅱ是分液漏斗;故填:酒精灯;分液漏斗;
(2)过氧化氢在二氧化锰的催化作用下分解为水和氧气,用双氧水与二氧化锰制取氧气属于固液常温型,若要控制反应的速率,可选择装置C来制取;高锰酸钾在加热的条件下分解为锰酸钾、二氧化锰和氧气,该反应属于固体加热型,选择装置A来制取,氧气的密度比空气大,不易溶于水,所以可用向上排空气法或排水法来收集,故填:C;2H2O2![]() 2H2O+O2↑;催化作用;AD或AE;2KMnO4
2H2O+O2↑;催化作用;AD或AE;2KMnO4![]() K2MnO4+MnO2+O2↑;氧气不易溶于水;
K2MnO4+MnO2+O2↑;氧气不易溶于水;
(3)D装置收集氧气,操作的正确顺序为:将装满水的集气瓶倒置在水槽中,将导管伸入集气瓶口,气体进入瓶中,当气体收集满时,在水下用玻璃片盖上瓶口,将集气瓶移出水面放置。故填:bac;
(4)氧气的密度比水小,若用装满水的E装置收集氧气,气体应从短管进入;故填:a。


 期末集结号系列答案
期末集结号系列答案科目:初中化学 来源: 题型:
【题目】通过下列实验现象,能说明氢氧化钠与稀硫酸发生了化学反应的是( )
A. 在稀硫酸中加入一定量的氢氧化钠固体,用温度计测得溶液的温度显著升高
B. 在![]() 的氢氧化钠溶液中加入一定量的稀硫酸,用pH计测得溶液的pH值变为8
的氢氧化钠溶液中加入一定量的稀硫酸,用pH计测得溶液的pH值变为8
C. 在氢氧化钠溶液中先滴加无色酚酞,再逐滴加入稀硫酸,看到酚酞红色逐渐变浅
D. 在氢氧化钠溶液中先加入一定量的稀硫酸,再逐滴加入硫酸铜溶液,无明显现象
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】铁及其化合物在生产生活中应用广泛。
(一)铁的性质和应用
(1)图1为某小儿硫酸亚铁糖浆。
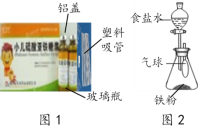
①适当服用该糖浆可治疗______(选填序号)。
A 佝偻病 B 贫血症 C 侏儒症
②图中不涉及到的材料是_______(选填序号)。
A 无机材料 B 合成材料 C 复合材料
(2)食品保鲜“双吸剂”含铁粉、食盐等,图2为其原理探究实验:
①滴入食盐水后,关闭分液漏斗活塞。一段时间后,铁粉上出现红色固体,气球___(选填“变大”、“不变”或“变小”)。
②食盐水的作用是______。
(二)铁的化合物制备
用废铁屑制备铁红(主要成分为Fe2O3)和K2SO4的部分流程如下图所示:
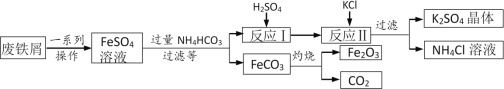
(1)加过量NH4HCO3反应时温度不宜过高的原因为______。
(2)反应Ⅰ生成的气体化学式是______。
(3)K2SO4和NH4Cl在农业生产中都可做______。
(4)为检验K2SO4中是否混有Cl—,要先加入足量_____溶液,静置后再加向上层清液中滴加少量_____溶液。
(5)在空气中灼烧FeCO3的化学方程式为_____。
(三)铁的冶炼和探究
取64.0g Fe2O3粉末,小组同学用下图装置模拟炼铁,并测定反应后固体成分。
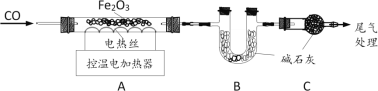
资料:碱石灰可吸收H2O和CO2。
(1)连接装置,先_________,再装入药品。
(2)实验时先通入CO,目的是_____________。
(3)控制A中温度反应,继续通CO至冷却后得到Fe和FeO的黑色固体,装置B中质量增重30.8g。请通过计算回答以下问题:
①固体中FeO质量为_______g。
②A中反应得到该黑色固体的化学方程式为_______。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】我国在2017年“世界环境日”(6月5日)确定的主题是“绿水青山,就是金山银山”.华雪与同学们积极参加了这一主题的活动,在老师的指导下,他们对一造纸厂排放的污水进行检测,发现其主要的污染物为NaOH.为了测定污水中NaOH的含量,他们首先把溶质质量分数为98%(密度1.84g/cm3)的浓硫酸20g,稀释为质量分数为10%的硫酸;然后取80g污水于烧杯中,逐滴加入10%的硫酸至49g时恰好完全反应(假定污水中的其它成分不与硫酸反应).请计算:
(1)把20g上述浓硫酸稀释为质量分数为10%的硫酸,需要水的质量是______g.
(2)污水中所含NaOH的质量分数是___________?(写出计算过程)
(3)取80g该污水于烧杯中放置几天后,若其中的氢氧化钠全部转化为碳酸钠.则此时应逐滴加入10%的硫酸______克才能使碳酸钠恰好完全变成硫酸钠.
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】钛享有“未来的金属”的美称,它是火箭、导弹和航天飞机不可缺少的材料。下列说法不正确的是( )
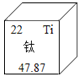
A. 钛原子的核内质子数为22B. 钛的相对原子质量是47.87g
C. 钛属于金属元素D. 钛元素的元素符号是Ti
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】如图所示,A、B、C为三种物质的溶解度曲线,请根据图示信息回答下列问题。
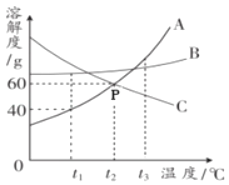
(1)P点的含义是_____。
(2)t1℃时,将30 g A物质投入50g水中,充分溶解,温度不变,所得溶液质量为_____。
(3)要使接近饱和的C溶液变成饱和溶液,可采用的方法_____(写出一种);当A中含有少量B时,可采用_____的方法提纯A。
(4)t2℃时,将A、B、C的饱和溶液分别降温至t1℃,所得溶液中溶质质量分数的大小关系是_____。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】将6.5g含有一种杂质的锌粉与足量的稀硫酸反应,生成0.18g氢气,则该锌粉中混有的杂质是_____(填“铜”或“铝”);将纯净的锌粉加入到含有Cu(NO3)2和AgNO3的混合溶液中,充分反应后过滤,若滤液中只含有一种溶质,则滤液中一定含有_____,若滤渣中含有两种金属,则滤液中可能含有_____.
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】中国高铁制造已处于世界先进水平。请回答下列问题。
(1)田老师乘高铁外出学习,在列车上购买了一盒快餐,其中有米饭、酱牛肉、炒白菜,牛肉中富含的营养素是_____。快餐盒使用的是可降解塑料,这样可以减轻的环境问题是“_____”。
(2)高铁水箱中装有生活用水,在净水过程中利用了活性炭的_____性。请写出节约用水的一种做法_____
(3)越来越多的新型材料应用于高铁建设,其中合金属于_____(填“金属”或“合成”)材料。
(4)合金较其组分金属具有一定的优良性能。用钒钢合金制造高铁的钢轨,主要利用其_____的性能。

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com