
【题目】我国化学家侯德榜创立的侯氏制碱法为纯碱工业技术的发展做出了杰出的贡献。在制备纯碱的过程中涉及Na2CO3、NaCl、NH4Cl、NaHCO3等物质。请结合表格数据回答下列问题:
温度/℃ | 0 | 10 | 20 | 30 | 40 | 50 | 60 | |
溶解度/g | Na2CO3 | 7 | 12.2 | 21.8 | 39.7 | 48.8 | 47.3 | 46.4 |
NH4Cl | 29.4 | 33.3 | 37.2 | 41.4 | 45.8 | 50.4 | 55.2 | |
NaHCO3 | 6.9 | 8.2 | 9.6 | 11.1 | 12.7 | 14.5 | 16.4 | |
(1)表中三种物质中,溶解性属于可溶的物质是__________。
(2)在50℃时,向100g水中加入48gNa2CO3充分搅拌所得溶液质量为___________ ;保持烧杯中各物质质量不变,降温至40℃时,所得溶液溶质的质量分数会_________(填“变小”、“不变”或“变大”)。
(3)请根据表格中数据,在下图中绘制出碳酸钠的溶解度曲线。
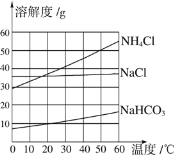 __________
__________
(4)根据溶解度曲线回答下列问题:
①60℃时,向等质量的上述四种固体物质中分别加水配成饱和溶液,所得溶液质量由大到小的顺序是_____________________________。
②侯氏制碱法的关键步骤是:先向饱和食盐水中通入氨气,制成饱和氨盐水,氨盐水吸收二氧化碳后生成碳酸氢钠和氯化铵,其化学方程式为NaCl+NH3+H2O+CO2=NH4Cl+NaHCO3。请问生成的碳酸氢钠和氯化铵,哪种物质首先析出______________,理由是_________________。
【答案】 碳酸氢钠(或NaHCO3) 147.3g 变大 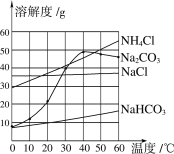 NaHCO3、NaCl、Na2CO3、NH4Cl(或NaHCO3>NaCl>Na2CO3>NH4Cl) 碳酸氢钠(或NaHCO3) NaHCO3的溶解度远小于NH4Cl的溶解度(或NaHCO3的溶解度较小;或反应生成的碳酸氢钠质量大于氯化铵,且相同温度下NaHCO3的溶解度远小于NH4Cl的溶解度)
NaHCO3、NaCl、Na2CO3、NH4Cl(或NaHCO3>NaCl>Na2CO3>NH4Cl) 碳酸氢钠(或NaHCO3) NaHCO3的溶解度远小于NH4Cl的溶解度(或NaHCO3的溶解度较小;或反应生成的碳酸氢钠质量大于氯化铵,且相同温度下NaHCO3的溶解度远小于NH4Cl的溶解度)
【解析】本题考查了纯碱的制取,溶解度曲线应用。
(1)20℃时,溶解度大于1g小于10g的物质属于可溶物质,所以表中三种物质中,溶解性属于可溶的物质是碳酸氢钠(或NaHCO3);
(2)碳酸钠的溶解度是47.3g,50℃时,100g的水中最多溶解47.3g Na2CO3,向100g水中加入48gNa2CO3充分搅拌所得溶液质量=100g+47.3g=147.3g,保持烧杯中各物质质量不变,降温至40℃时,溶解度变大,烧杯中未溶解的碳酸钠继续溶解,所得溶液溶质的质量分数会变大;
(3)依据表中的数据绘制出碳酸钠的溶解度曲线如图: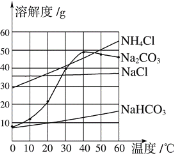
(4)①60℃时,氯化铵的溶解度最大,碳酸钠的溶解度次之,碳酸氢钠的溶解度最小,所以向等质量的上述四种固体物质中分别加水配成饱和溶液,所得溶液质量由大到小的顺序是:NaHCO3、NaCl、Na2CO3、NH4Cl(或NaHCO3>NaCl>Na2CO3>NH4Cl);
②侯氏制碱法的关键步骤是:先向饱和食盐水中通入氨气,制成饱和氨盐水,氨盐水吸收二氧化碳后生成碳酸氢钠和氯化铵,其化学方程式为:NaCl+NH3+H2O+CO2=NH4Cl+NaHCO3,生成的碳酸氢钠和氯化铵,碳酸氢钠首先析出,理由是:NaHCO3的溶解度远小于NH4Cl的溶解度(或NaHCO3的溶解度较小;或反应生成的碳酸氢钠质量大于氯化铵,且相同温度下NaHCO3的溶解度远小于NH4Cl的溶解度)。


科目:初中化学 来源: 题型:
【题目】某氢氧化钠样品中混有氯化钠,为测定样品中氢氧化钠的质量分数,称取5.0g样品,加水完全溶解后,缓慢加入稀盐酸,同时测定溶液的pH。当pH=7时,恰好用去10%的稀盐酸36.5g。(反应的化学方程式为:NaOH + HCl = NaCl + H2O)试计算:
(1)将100g质量分数为36 %的浓盐酸稀释成10 %的稀盐酸,需加水的质量为________g。
(2)样品中氢氧化钠的质量分数_____。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】世界环境日为每年的6月5日。中国2017年环境日主题:“绿水青山就是金山银山”,旨在动员引导社会各界尊重自然、顺应自然、保护自然,自觉践行绿色生活,共同建设美丽中国。
(1)自然界消耗二氧化碳气体的主要途径有:①植物的光合作用,植物在光照和叶绿素作用下吸收二氧化碳和水生成葡萄糖(C6H12O6)和氧气,②海水的吸收等。请用化学反应方程式表示出其中一个消耗CO2的途径:____________________。
(2)请举一例你在日常生活中能做到的“节能减排”的做法____________________。
(3)下列关于乙醇汽油的说法正确的是__________(填序号)。
A.乙醇属于可再生能源 B.乙醇汽油不能用作汽车燃料
C.使用乙醇汽油可减少大气污染
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】有一包固体粉末,可能含有镁粉、碳粉、氧化铜、硫酸钾、氢氧化钠中的一种或几种。为探究固体的组成,某化学兴趣小组进行了如图所示实验。
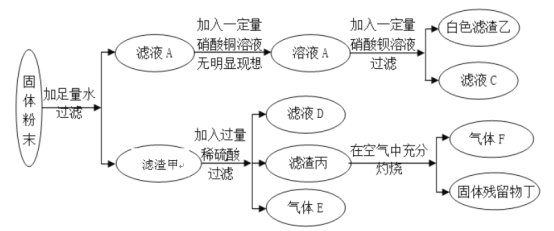
请回答下列问题:
(1)实验中生成白色滤渣乙的化学方程式是__________。
(2)原固体中一定不含有的物质是__________。
(3)原固体中一定含有的物质是__________。
(4)实验结束后,该兴趣小组将滤液C和滤液D都倒入废液缸,有白色沉淀生成,则滤液C中一定含有的溶质是__________。
(5)如果滤渣丙的质量等于固体残留物丁的质量,则气体F与固体残留物丁的质量比为__________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】丁基锂(C4H9Li)是橡胶合成工业中一种常用的试剂。白色粉末,熔点-95℃,沸点80℃,遇水、空气均易自燃。下列关于丁基锂的说法正确的是
A. 丁基锂是由4个碳原子、9个氢原子、1个锂原子构成的
B. 丁基锂中碳元素质量分数为75%
C. 丁基锂运输或使用过程中如果发生燃烧,可以用水浇灭
D. 丁基锂是有机高分子化合物
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】科学家已经在实验室中制造出了“冰七”(ice Ⅶ),这种冰需要在含有大量水源和极高的压强下才能够生成,水分子会整齐排列或排成一列非常整齐有规则的冰晶,像是一个立方体的牢笼裹合物。下列说法不正确的是
A. 冰七和水的化学性质不完全相同
B. 冰七中分子之间的距离比普通冰中的小
C. 海水在一定条件下可以形成冰七
D. 冰七中的分子永不停息地运动
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】粽子是端午节的传统美食,海南粽子用料讲究,除了糯米外,还有猪肉、咸蛋黄等,味道香糯可口,食之唇齿留香。
(1)煮粽子时,小海老远就闻到香味。从微观的角度分析, 其原因是___________;
(2)在煮粽子时为了避免把锅熏黑,在锅外面贴上一层报纸(如图), 小海发现粽子煮好后,报纸仍然没有燃烧,其原因是_____(填序号,下同);

A.着火点升高了 B.温度没有达到着火点 C.没有与氧气接触
(3)小海的午餐是粽子,从营养均衡的角度看,他还应该增加的食物是_____。
A.馒头 B.鸡腿 C.青菜
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】下图是甲、乙、丙三种固体物质的溶解度曲线,据图回答下列问题。

(1)0℃时,乙物质的溶解度是___________。
(2)t1℃时,三种物质溶解度由大到小的顺序是___________。
(3)t3℃时,将70g甲物质加到100g水中,充分搅拌后所得溶液的质量是______g。
(4)t3℃时,将甲、丙两物质的饱和溶液同时降温至________℃,它们溶质的质量分数相等。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】如图是某能量型饮料及标签中的部分成分,请回答下列问题:
(1)该饮料提供了人体所需六大营养素中的水、糖类和_______。
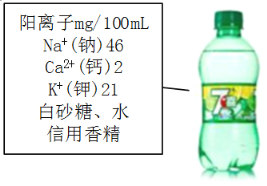
(2)该饮料中的钠元素由氯化钠提供,则配制100mL饮料需要氯化钠的质量是_______mg
(3)白砂糖在催化剂作用下可转化为葡萄糖(C6H12O6),葡萄糖可以发生如下反应:C6H12O6![]() 2X+2CO2
2X+2CO2![]() ,则X的化学式为__________。
,则X的化学式为__________。
(4)饮料瓶的材料是PET,化学式为(C10H8O4)n,它属于__________(填“有机化合物”或无机化合物”)。在饮料瓶的生产过程中,以下做法合理的是_________。
a.加高烟囱排放废气 b.采用新技术加强污水处理
c.采用“光伏发电”和“煤改气工程”提供能量
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com