
科目: 来源: 题型:
【题目】人被蚊虫叮咬后,蚊虫在人的皮肤内分泌出蚁酸,使叮咬处又痛又痒。化学小组同学对蚁酸产生了浓厚的兴趣,决定对其进行探究。
[提出问题] 蚁酸的成分是什么?它有什么性质?
[查阅资料] I.蚁酸是一种有机酸,化学名称叫做甲酸,化学式为HCOOH;
II.蚁酸在隔绝空气并加热的条件下会分解生成两种氧化物。
[实验探究]
(1)向盛有蚁酸溶液的试管中滴加紫色石蕊试液,观察到溶液颜色变成____色,说明蚁酸溶液显酸性;
(2)小芳同学根据蚁酸中含有________元素,推测出蚁酸在隔绝空气并加热的条件下分解生成的一种产物是水;
(3)蚁酸在隔绝空气并加热的条件下分解生成的另一种氧化物是气体,小敏提出两种猜想:
①猜想I:该气体是CO2; 猜想II:该气体是________;
他们将蚁酸分解产生的气体通过下图的装置。
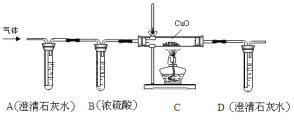
②实验时装置A中无明显变化,则猜想I ______(填“成立”或“不成立”);若猜想II成立,则:
③实验时装置B的作用是_______________________;
④实验时装置C中的现象是___________________;
⑤实验时装置D中发生反应的化学方程式为_______________;
[讨论交流] 从环保角度看,该装置存在明显的缺陷,处理方法是______________;
[拓展延伸] 当你被蚊虫叮咬后,在叮咬处涂抹一些物质可减轻痛痒。下列物质中,你不会选择的物质是_____。
A 苏打水 B 肥皂水 C 食醋 D 氨水
查看答案和解析>>
科目: 来源: 题型:
【题目】有一包白色粉末,可能由CuSO4、Na2SO4、Na2CO3、BaCl2、NaOH中的一种或几种组成。为探究其组成,同学们查阅资料得知NaCl、BaCl2溶液呈中性,经过思考设计并进行了以下实验:
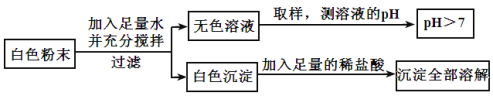
(1)白色粉末中一定不含_____________;可能含有____________。
(2)为最终确定白色粉末的组成,还需要对无色滤液中呈碱性的物质进行探究。
(提出问题)无色滤液中呈碱性的物质是什么?
(作出猜想)猜想Ⅰ:Na2CO3
猜想Ⅱ:NaOH
猜想Ⅲ:Na2CO3和NaOH
(进行实验)
实验步骤 | 实验现象 | 实验结论 |
① 取无色滤液少许于试管中,滴加过量的BaCl2溶液 | ________ | 猜想Ⅱ不成立 |
② 在①反应后的试管中滴加________ | 溶液变为红色 | 猜想Ⅲ成立 |
(得出结论)白色粉末的成分是________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】A、B、C、D、E 分别为氧化铁、盐酸、氢氧化钙、碳酸钙、铁中的一种,它们之间的反应或转化关系如图(图中→表示转化关系,--表示可相互反应,部分物质和反应条件已略去)。回答下列问题:
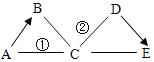
(1)已知 C 是盐酸,D 是氧化铁,则 A、B、E 的化学式分别为____、_____、_____;
(2)写出反应①、②的化学方程式:①_________________________;②_____________。
查看答案和解析>>
科目: 来源: 题型:
【题目】A—J都是初中化学常用的物质。其中B、E、H、J是单质,其余均为化合物,气体C可用于灭火。“C→B”的转化过程,在自然界中称为光合作用。它们相互间的转化关系如下图所示(部分反应物、生成物及反应条件已略去)。
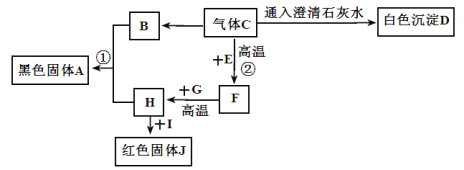
请回答下列问题:
(1)写出物质D、J的化学式:D___________,J___________。
(2)反应①的反应条件___________,其基本反应类型___________。
(3)写出反应②的化学方程式:______________________。
(4)若要实现“H+I→红色固体J”的转化,物质I可能是___________。
查看答案和解析>>
科目: 来源: 题型:
【题目】甲、乙、丙、丁都是初中化学中最常见的物质,已知它们分别是HCl、NaOH、Ca (OH)2、CaCl2、Na2CO3等五种物质中一种,丙与甲、乙、丁三种物质都能发生反应.将这四种物质的溶液按图所示相互滴加,现象为:试管①产生白色沉淀;试管②有气泡冒出;试管③无明显现象。
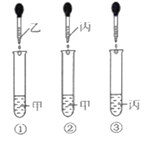
(1)甲物质是______。
(2)丙与丁反应的化学方程式是______。
(3)向试管③滴加的溶液溶质没有标注,它可能是_____或______。
(4)甲、乙、丙、丁不可能是_____。
查看答案和解析>>
科目: 来源: 题型:
【题目】下列曲线能正确表达对应的反应或过程的是 ( )
A. 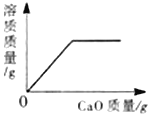 向一定量的水中加入生石灰
向一定量的水中加入生石灰
B. 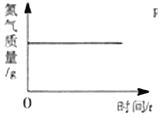 红磷在装有空气的密闭容器中燃烧
红磷在装有空气的密闭容器中燃烧
C. 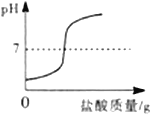 向一定量的烧碱溶液中加入盐酸
向一定量的烧碱溶液中加入盐酸
D.  向饱和KNO3溶液中加入NaCl固体
向饱和KNO3溶液中加入NaCl固体
查看答案和解析>>
科目: 来源: 题型:
【题目】中和反应在工农业生产和生活中有有泛的应用。某学生课外兴趣小组对中和反应进行研究。
(实验一)对于没有明显实验现象的中和反应,如稀盐酸与稀氢氧化钠溶液的反应,要证明它们之间确实发生了化学反应,可通过如下实验来进行。
将稀盐酸逐滴匀速加入一定量的稀氢氧化钠溶液中,用数字化仪器对反府过程中溶液的pH、温度进行实验测定,得到的曲线如图、如图所示中。
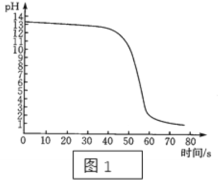

如图、如图均能证明中和反应发生了,如图能证明中和反应的判断依据是________________________________。由如图还能得出的其他结论是____________________________________。
(实验二)取少量难溶的氢氧化镁置于试管中加水振荡,得到浑浊液,再加入稀盐酸,若观察到现象_____,就可说明反应已经发生。该反应的化学方程式是____________________________________。
(实验反思)在敞口久置的氢氧化钠溶液中加入盐酸后,意外发现有气泡产生,同学们认为产生意外现象是因为______________________________而变质,变质后的物质和盐酸反应生成了___________气体。
(实验三)用白色无水硫酸铜粉末证明酸与碱之间能发生中和反应。

(1)在试管①和②中加入等质量的无水硫酸铜粉末,并在试管②里加入一些固体氢氧化钠和无水醋酸与无水硫酸铜粉末混合,段时间后试管②中无水硫酸铜粉末先变蓝,说明有水生成,从而证明中和反应发生了。
(2)小艺认为上述对照试验不能证明酸与碱发生了中和反应,小艺的理由是________________________________________________.你认为应怎样改进试验?______
(实验四)利用如图所示的原理来证明酸与碱可以发生中和反应。
(1)在盛有10mL浓硫酸的烧杯中倒入5mL氢氧化钠溶液,溶液温度迅速上升,由此证明硫酸与氢氧化钠发生了中和反应。小涵认为该实验不能证明硫酸与氢氧化钠发生了反应,小涵的理由是___________________.
(2)该实验可能造成的危害是_____________________________________________.
查看答案和解析>>
科目: 来源: 题型:
【题目】亚硫酸钠是种常见食品添加剂,亚硫酸钠在加热条件下可以和酸反应生成氧化硫气体。为检验某食品中亚硫酸钠的含量(以1kg样品生成的SO2质量计),某研究小组设计了如下实验流程:

(1)为防止煮沸时发生暴沸,可以先向烧瓶中加入___________________________.在实验装置中先通入![]() 的目的是___________________________.
的目的是___________________________.
(2)写出氢氧化钠溶液吸收SO2的化学方程式:_______________________________________________.
(3)要得到SO2的质量,实验中需要称量反应前碱液的质量和_____________的质量。
(4)若用盐酸代替稀硫酸处理样品,则对实验结果的影响是_____________(填“偏高”、“偏低”或“无影响”),这是因为盐酸具有_____________性。
查看答案和解析>>
科目: 来源: 题型:
【题目】铝是重要的轻金属,广泛应用于航空、电讯和建筑等领域。
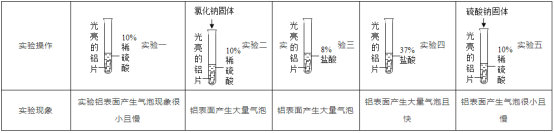
(1)依据金属的活动性顺序,铝的金属活动性比锌__________.但是将铝片和锌粒分别投入稀硫酸中,铝片表面产生的气泡却比锌粒少而慢。为了探究影响铝与酸反应速率的因素,振兴同学用相同质量、相同形状、除去氧化膜的铝片设计如图所示实验。
(2)写出实验中发生反应的化学方程式_______________________________________.
(3)比较实验三、四说明铝与酸反应产生氢气的速率,与_____________________有关.
(4)比较实验一、二说明铝与酸反应产生氢气的速率,可能与_________、_________(填粒子符号)、与和温度、金属与酸的接触面积等各种因素有关。
(5)比较实验一、二、五可以得出的结论是____________________________________.
查看答案和解析>>
科目: 来源: 题型:
【题目】活泼金属可以和酸反应生成氢气,现在利用如图所示装置制取氢气,塑料片上放有足量锌粒,从漏斗中加入稀盐酸。
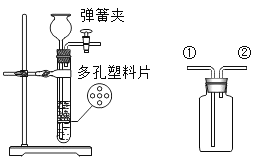
(1)该气体发生装置的优点是__________________,收集氢气可以从导管__________通入(填序号),点燃瓶中氢气前应进行的操作是____________________________________.
(2)锌粒和稀盐酸刚接触时没有气泡产生,过会才产生大量气泡其原因可能是_________________________.
(3)该气体发生装置一般不用于过氧化氢溶液和二氧化锰制氧气,其原因是__________________________,过氧化氢溶液和二氧化锰制氧气的化学方程式是____________________________________.
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com