
科目: 来源: 题型:
【题目】铜是一种不活泼的金属,但长期露置在潮湿的空气中会锈蚀生成“铜绿”[化学式:Cu2(OH)2CO3]。某科研小组为探究铜绿生成的条件,并从已部分锈蚀的废铜屑中回收铜(假设不含其它杂质),实验设计如下:
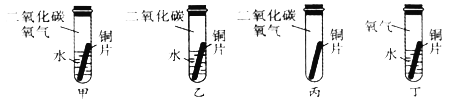
(1)证明生成铜绿的条件除存在O2和H2O外,还必须有CO2。为“证明必须有CO2”需要进行以上实验中的_____(填实验编号)。
(2)利用已部分锈蚀的废钢屑按照以下实验方案回收铜。
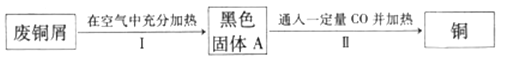
①已知铜绿受热分解为固体A、CO2和H2O,则步骤I中发生的反应类有_____。
②步骤Ⅱ中主要发生的化学反应方程式为_____。
③若步骤Ⅱ所得钢中含有少量Cu2O,你认为可能的原因是_____(写一条即可)。
④若用CO还原16.0gCuO得到Cu和Cu2O混合物的质量为ag,则a的取值范围为_____。
查看答案和解析>>
科目: 来源: 题型:
【题目】实验室有一瓶失去标签的NaOH溶液。为测定溶液中NaOH的质量分数,取m2 g NaOH溶液于量热器中,加入m1 g质量分数为10.0%的盐酸,进行若干次实验(实验中始终保持m1+m2=50g),测量并记录每次实验溶液均匀混合后的最高温度,实验结果如图所示。
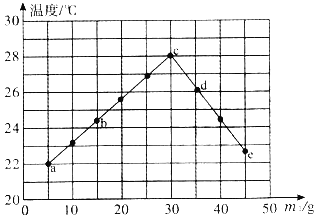
(1)图中____点表示盐酸与NaOH溶液恰好完全反应(填标号)。
(2)计算溶液中NaOH的质量分数(结果精确到0.1%)。____
查看答案和解析>>
科目: 来源: 题型:
【题目】图1所示转化关系涉及的物质均为初中化学常见的物质。其中常温下乙的水溶液pH>7,甲、乙、丙均含有元素X,元素X的原子结构示意图如图2所示。图中“→”表示相连两种物质之间的转化关系,“一”表示相连的两种物质可以发生反应,反应条件、部分反应物及生成物已略去。
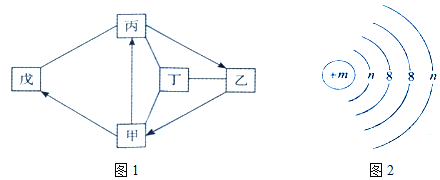
请回答下列问题。
(1)元素X的名称为______。
(2)丙和戊在一定条件下可以发生化合反应,其化学方程式为______。
(3)写出甲与丁反应的化学方程式______。
(4)乙在生产和生活中的用途是______(写一条即可)。
查看答案和解析>>
科目: 来源: 题型:
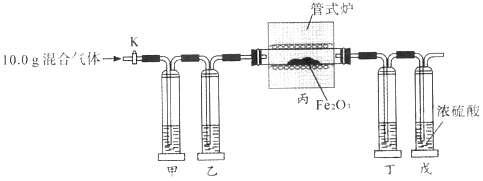
【题目】某同学利用以下实验装置准确测定出某混合气体中(成分:CO、CO2、H2)各组分的质量分数。实验时先通一段时间氮气,再继续实验(已知:3H2 +Fe2O3![]() 2Fe+3H2O.实验中供选用试剂:①NaOH溶液,②澄清石灰水,③浓硫酸。且装置中试剂均足量)。
2Fe+3H2O.实验中供选用试剂:①NaOH溶液,②澄清石灰水,③浓硫酸。且装置中试剂均足量)。
下列说法正确的是( )
A. 甲、乙、丁中依次盛装试剂①、试剂③、试剂②
B. 实验时,应先打开活塞K,再用管式炉加热
C. 装置戊的作用是吸收反应生成的水蒸气
D. 测得装置甲、装置丁反点前后的质量差即可求出各组分的质量分数
查看答案和解析>>
科目: 来源: 题型:
【题目】向AgNO3、Cu(NO3)2、Mg(NO3)2的混合溶液中加入一定量的铁粉,充分反应后过滤,滤液呈蓝色。下列判断正确的是( )
A. 滤液中有可能只含有两种溶质
B. 与原溶液相比,滤液的质量可能增大
C. 若滤渣中只有一种金属,则滤液中溶质一定有四种
D. 若滤渣中只有两种金属,则滤液中溶质一定有三种
查看答案和解析>>
科目: 来源: 题型:
【题目】某同学利用自制的紫色紫薯汁进行“溶液酸碱性检验”的探究实验,实验现象记录如下。
溶液 | 白醋 | 盐酸 | 蔗糖水 | 肥皂水 | 石灰水 |
加入紫薯汁后溶液的颜色 | 红色 | 红色 | 紫色 | 绿色 | 绿色 |
下列结论或推论错误的是( )
A. 蔗糖水呈中性
B. 溶液的pH:肥皂水![]() 蔗糖水
蔗糖水![]() 白醋
白醋
C. 将等体积的盐酸与石灰水混合,溶液pH一定等于7
D. 将等体积的白醋与盐酸混合,溶液pH一定小于7
查看答案和解析>>
科目: 来源: 题型:
【题目】下图是A、B、C三种物质的溶解度曲线:

请写出三点符合图中溶解度曲线的不同类型的信息。
(1)_______________________________________________________________________。
(2)_______________________________________________________________________。
(3)_______________________________________________________________________。
查看答案和解析>>
科目: 来源: 题型:
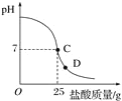
【题目】为测定标有质量分数为32%的盐酸的实际质量分数,小明实验时先在烧杯中加入20 g 40%的氢氧化钠溶液,再逐滴加入该盐酸,测定出加入盐酸的质量与烧杯中溶液pH的关系如图。
(1)所用氢氧化钠溶液中溶质的质量为_____g。
(2)请认真看清上图信息后回答以下问题。
①当滴加盐酸到C点时,所消耗的盐酸中溶质的质量是多少?_____。
②该盐酸的实际质量分数是多少?(保留到0.1%)_____。
③导致盐酸溶液的溶质质量分数改变的原因是_____。
④当滴加盐酸到图像中D点时,烧杯中溶液的溶质是_____(填化学式)。
查看答案和解析>>
科目: 来源: 题型:
【题目】某同学家中有一袋化肥,可能混入了其他化肥,且化肥包装袋上的字迹模糊.该同学进行了如下探究,请你参与探究并填空:
[提出问题]该化肥中含有什么物质?
[收集信息]经询问得知,该化肥为铵态氮肥.
[提出猜想]该化肥所含的阴离子可能是Cl-、![]() 、
、![]() ;中的一种或几种.
;中的一种或几种.
[实验、记录与分析]
实验操作步骤 | 实验现象 | 实验分析 |
(1)取少量该化肥样品和少量熟石灰放在研钵中混合研磨 | ________ | 含有铵根离子 |
(2)另取少量该化肥样品于试管中,加入适量的水完全溶解,滴加足量的硝酸钡溶液,再滴加少量稀硝酸,过滤 | 产生白色沉淀,沉淀不溶解 | 没有________(填化学式)存在 |
(3)取(2)中所得滤液少量于试管中,滴加________ | ________ | 有Cl-存在 |
[实验结论]若该化肥中只含有一种阳离子,则其中一定含有的物质是(写化学式)________________________________________________________________________.
[实验反思]若步骤(2)中用氯化钡溶液代替硝酸钡溶液是否可行?________(填“是”或“否”),请简要说明原因:________________________________________.
查看答案和解析>>
科目: 来源: 题型:
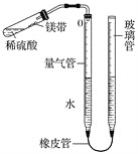
【题目】某课外活动小组同学用图中装置(固定装置未画出)测定含有杂质的镁带中镁单质的质量分数(杂质与酸接触不产生气体)。实验过程如下:
①取一段镁带样品,准确称得其质量为0.030 g;
②往量气管内装水至低于刻度“0”的位置,如图所示,(未装药品)装配好仪器;
③_________________________;
④在试管中加入足量的稀硫酸,稍倾斜试管,将用水湿润的镁带小心贴在试管壁上,塞紧橡皮塞;
⑤调整量气管液面,使两边的液面保持同一水平,记录量气管中液面位置;
⑥把试管底部略为抬高,使镁带与稀硫酸接触完全反应;
⑦待冷却至室温后,再次记录量气管中液面位置;
⑧算出量气管中增加的气体体积为23.96 mL;
已知:同温同压下,不同气体混合后体积等于混合前各气体体积之和。
请回答下列问题:
(1)写出镁与稀硫酸反应的化学方程式:____________________。
(2)能否用托盘天平称量0.030 g镁带样品________(填“能”或“不能”)。
(3)操作③是_________________________。
(4)实验过程⑦中再次记录量气管的液面位置时,试管中留有氢气,是否会影响实验最终结果________(填“是”或“否”),理由是_______________________。
(5)若实际测得氢气的体积与理论值相比偏大,则可能的原因是________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com