
科目: 来源: 题型:
【题目】某混合气体中可能含有CO、CO2、SO2三种气体中的一种或几种。几位同学们对该混合气体的成分进行了探究。
(查阅资料)
I.SO2能使品红溶液褪色,易与高锰酸钾溶液反应而被吸收,此外能与氢氧化钠溶液反应,也能使澄清的石灰水变浑浊。
Ⅱ.CO和CO2均不能使品红溶液褪色,也不与高锰酸钾溶液反应。
(实验探究)
该班同学们在老师指导下设计并进行了如下实验:
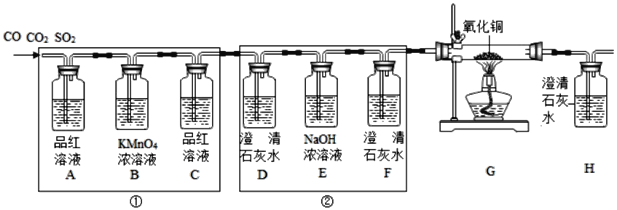
(现象与结论)
(1)装置C的作用是_____:要证明气体中含有CO则在装置G中会发生的化学反应是_____。
(2)装置H中发生反应的化学方程式为_____。
(反思与评价)
(3)若将装置①和装置②互换位置,将不能证明气体中一定含有_____(填化学式)。
(4)实验结束后发现G中红色粉末又变成黑色,原因可能为:(用化学方程式表示)_____。
(5)该实验还缺少的装置是_____。
查看答案和解析>>
科目: 来源: 题型:
【题目】A、B、C、D分别为二氧化碳、铁、稀硫酸、氢氧化钠溶液中的一种,它们之间的反应关系如图.图中“﹣”表示两种物质可相互反应.则:
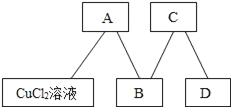
A和B反应的化学方程式为_____;
C和D反应的化学方程式为_____;
D在生产或生活中的一种用途是_____.
查看答案和解析>>
科目: 来源: 题型:
【题目】牙膏是人们生活中的必需品,在牙膏生产过程中常添加一种摩擦剂.这种摩擦剂是一种经过一系列加工而制得的极细的碳酸钙粉末.其生产过程如图.
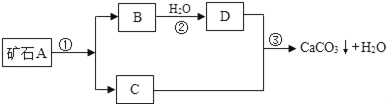
根据上图回答:
(1)写出B,C,两种物质的化学式:B_____; C_____;
(2)写出上述过程中反应①的化学方程式_____.上述过程中没有涉及的基本反应类型是_____
(3)许多牙膏中都含有_____元素,因为如果缺少这种元素,就容易得龋齿.
查看答案和解析>>
科目: 来源: 题型:
【题目】在20℃时,刘冰同学向100g水中依次加入NaCl固体,充分溶解,实验过程如图所示。下列说法错误的是( )
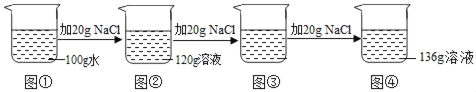
A. 图②中的溶液是不饱和溶液
B. 图③中的溶液是饱和溶液
C. 图③中溶液的溶质质量为40 g
D. 图③和图④中NaCl溶液的溶质质量分数相等
查看答案和解析>>
科目: 来源: 题型:
【题目】甲烷和水反应可以制备水煤气(混合气体),其反应的微观示意图如图所示:根据以上微观示意图得出的结论中,正确的是( )
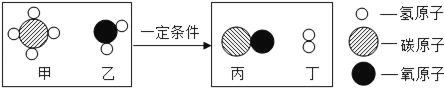
A. 水煤气的成分是一氧化碳和氧气
B. 反应中甲和丙的质量之比为4:7
C. 反应中含氢元素的化合物有三种
D. 反应前后碳元素的化合价未发生变化
查看答案和解析>>
科目: 来源: 题型:
【题目】小明对铁的锈蚀进行如下探究,室温时,将包有样品的滤纸包用大头针固定在橡胶塞上,迅速塞紧,装置如图,观察到量筒内水沿导管慢慢进入广口瓶(净容积为146 mL)。当温度恢复至室温,且量筒内水面高度不变时读数(此时瓶内氧气含量近似为零)。记录起始和最终量筒的读数以及所需时间如表
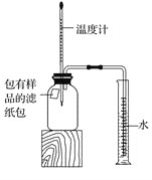
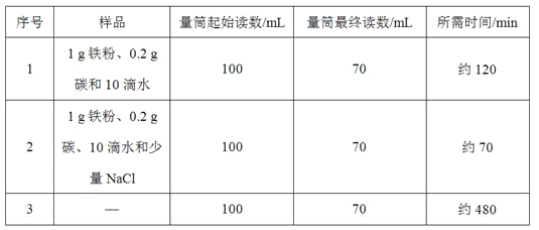
(1)实验①和②说明NaCl可以____铁锈蚀的速率。
(2)实验开始后,广口瓶内温度有所上升,说明铁的锈蚀过程是____(填“放热”或“吸热”)过程。
(3)实验结束后取出滤纸包,观察到有红棕色物质生成,该物质的化学式是______。
(4)已知碳能够加快铁的生锈速度,小明想通过实验①和③是探究碳对铁锈蚀速率的影响,请在表格空白处填写实验③的样品组成___。
(5)该装置还可用于测量空气中氧气的含量,根据上述数据计算氧气的体积含量是___(小数点后保留1位)。
查看答案和解析>>
科目: 来源: 题型:
【题目】请你阅读下列一段新闻,并完成有关问题。
2005年6月16日《海峡都市报》报道:位于我市河东社区外的琼东河,已被建筑垃圾、生活垃圾、破砖头、牛奶包装盒等挤占了大半个河道。
(1)城市处理垃圾的方法有多种,填埋是其中的一种。垃圾填埋后会产生沼气,沼气的主要成分_,其完全燃烧的化学方程式为__。
(2)生活垃圾中的塑料矿泉水瓶、塑料袋都属于___(填“金属”“有机高分子材料”或“非金属材料”)有机高分子材料。在日常生活中各种塑料制品已被广泛应用。请分析使用塑料的利弊(各写一点):利:____。弊:___。
查看答案和解析>>
科目: 来源: 题型:
【题目】某化学兴趣小组根据右图所示进行模拟炼铁的实验,并对产物成分进行探究。
经初步无色气体A不含有单质气体,黑色粉末B含有两种单质中的一种或者两种。
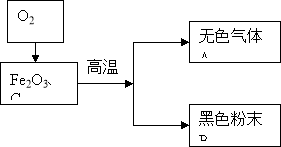
高炉炼铁的原理为:Fe2O3+3CO![]() 2Fe+3CO2,请写出反应器中一氧化碳是如何产生的化学方程式: 。
2Fe+3CO2,请写出反应器中一氧化碳是如何产生的化学方程式: 。
兴趣小组又分成甲乙两组分别对无色气体A和黑色粉末B的成分进行探究。
【猜想与假设】
甲组在分析了炼铁的原理后,认为无色气体A中可能有CO2,也可能有未反应的 。
乙组认为黑色粉末的成分中存在以下三种情况:
假设一:只含有铁。 假设二:只含有 。 假设三:以上两种物质都含有。
【实验探究】
(1)为验证甲组的猜想,大家按下图示进行实验(箭头表示气体流向):
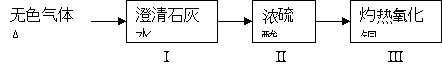
当看到Ⅰ中澄清石灰水变浑浊,Ⅲ中灼热的氧化铜变红,可以确定无色气体A的成分为: ,Ⅱ中浓硫酸的作用是: 。
(2)为验证乙组中假设三成立,大家用物理和化学两种方法来进行探究
实验方法 | 实验操作 | 实验现象 | 实验结果 |
物理方法 | 假设三成立 | ||
化学方法 | 取少量黑色粉末B于试管中,加入过量的稀盐酸 | 假设三成立 |
写出黑色粉末B中加入过量的稀盐酸反应的化学方程式: 。
【交流反思】
在做甲组的实验中发现其存在一个很不环保的缺陷,请指出来 。
查看答案和解析>>
科目: 来源: 题型:
【题目】(9分)某化学小组利用如图所示装置(图中固定装置已略去)测定铜锌合金中锌的质量分数.
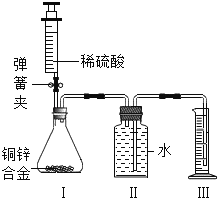
探究过程如下:
①连接实验装置并检查装置气密性.
②向装置Ⅰ中的锥形瓶加入2.0g的铜锌合金样品粉末,由注射器缓缓注入稀硫酸,待到锥形瓶中不再产生气体时,准确读取注射器内读数,减少10.5mL稀硫酸,同时立即夹紧弹簧夹,移出装置Ⅲ中的导管,准确读取量筒内水的体积为214.0mL.(注:样品中的杂质不参加反应)
③装置Ⅰ中剩余固体物质经过适当处理后,准确称量其质量1.4g.
④该小组的三位同学利用实验过程测得不同数据,计算铜锌合金样品中锌的质量分数.
甲同学利用装置Ⅰ中反应前后固体的质量进行计算;
乙同学利用装置Ⅰ中加入稀硫酸的量进行计算;
丙同学利用装置Ⅲ中量取水的体积进行计算,并查得:在标准状况下,氢气的密度为0.09g/L.
回答下列问题:
(1)装置Ⅰ中反应的化学方程式为 ,实验过程中须加入稀硫酸至不再产生气体,目的是 .
(2)步骤③中称量剩余固体之前的正确操作是 、洗涤、干燥.
(3)根据实验测定的数据,上述三位同学中 (填“甲”、“乙”或“丙”)同学无法进行计算样品中锌的质量分数.
(4)化学小组同学发现:按照丙同学的方案进行计算,致使实验结果出现较大偏差.以下因素可能造成偏差的有 (填标号).
A.移出装置Ⅲ时,导管内留存了一部分水
B.实验测量前,没有排除装置Ⅰ中的空气
C.数据处理时,未排除加入稀硫酸所占的体积.
查看答案和解析>>
科目: 来源: 题型:
【题目】某化学小组利用如图所示装置(图中固定装置已略去)测定铜锌合金中锌的质量分数,探究过程如下:
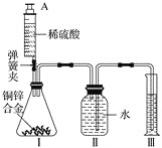
①连接实验装置并检查装置气密性。
②向装置Ⅰ中的锥形瓶加入2.0g的铜锌合金样品粉末,由注射器缓缓注入稀硫酸,待到锥形瓶中不再产生气体时,准确读取注射器内读数,减少10.5mL稀硫酸,同时立即夹紧弹簧夹,移出装置Ⅲ中的导管,准确读取量筒内水的体积为214.0mL(注:样品中的杂质不参加反应
③装置Ⅰ中剩余固体物质经过适当处理后,准确称量其质量为1.4g
④该小组的三位同学利用实验过程测得不同数据,计算铜锌合金样品中锌的质量分数
甲同学利用装置Ⅰ中反应前后固体的质量进行计算;
乙同学利用装置Ⅰ中加入稀硫酸的量进行计算;
丙同学利用装置Ⅲ中量取水的体积进行计算,并查得:在标准状况下,氢气的密度为0.09gL-1。
回答下列问题:
(1)装置Ⅰ中反应的化学方程式为___,实验过程中须加入稀硫酸至不再产生气体,目的是___。
(2)步骤③中称量剩余固体之前的正确操作是_______、洗涤、干燥。
(3)根据实验测定的数据,上述三位同学中________(填“甲”、“乙”或“丙”)同学无法进行计算样品中锌的质量分数。
(4)化学小组同学发现:按照丙同学的方案进行计算,致使实验结果出现较大偏差。以下因素可能造成偏差的有________(填标号)。
A 移出装置Ⅲ时,导管内留存了一部分水
B 实验测量前,没有排除装置Ⅰ中的空气
C 数据处理时,未排除加入稀硫酸所占的体积
【答案】(1)![]() ;使样品中的锌完全反应;(2)过滤;(3)乙;(4)AC;
;使样品中的锌完全反应;(2)过滤;(3)乙;(4)AC;
【解析】
试题(1)由于铜排在了氢的后面,所以与酸不反应,反应物是锌和硫酸,生成物是硫酸锌和氢气,氢气后面标上上升符号;实验过程中须加入稀硫酸至不再产生气体,目的是使样品中的锌完全反应;(2)从铜和硫酸锌溶液的混合物中得到铜,先进行过滤,得到带有硫酸锌溶液的铜,再进行洗涤除去表面的硫酸锌,再进行干燥除去水即可;(3)根据加入稀硫酸的量进行计算需要知道稀硫酸的溶质质量分数,而题中没有告知;(4)由于锌与硫酸反应生成硫酸锌和氢气时,放出热量,如果没等冷却到室温,根据热涨冷缩的原理可知进入量筒中水偏多,所以误认为得到的氢气多,再就是数据处理时,未排除加入稀硫酸所占的体积,计算的结果就偏大;
考点:金属的化学性质;化学方程式;实验误差分析;
点评:熟记金属活动性顺序表,知道排在氢之前的金属和稀盐酸或者硫酸反应生成氢气,而排中氢之后的金属和稀盐酸或者稀硫酸不生成氢气;化学反应中物质的质量比都是纯净物之间的质量比,而溶液中溶质的质量=溶液质量×溶质质量分数;本题容易出错的地方是对实验结果的评价,要知道锌与硫酸反应放出热量,会造成相应的误差,必须冷却到室温才能进行观察和计算。
【题型】实验题
【结束】
30
【题目】用1000t含氧化铁80%的赤铁矿石,理论上可以炼出含铁96%的生铁的质量是多少?
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com