
科目: 来源: 题型:
【题目】将质量相等的铝粉和铁粉分别与质量、浓度均相同的稀硫酸充分反应,下列所述的反应情况与图示可能相符的是
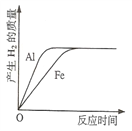
①铝粉、铁粉和硫酸均有剩余 ②硫酸、铝粉、铁粉均反应完
③硫酸、铁粉均反应完,铝粉有剩余
④硫酸、铝粉均反应完,铁粉有剩余
⑤铝粉、铁粉均反应完,硫酸有剩余
⑥硫酸反应完,铝粉、铁粉有剩余
A. ①③⑤ B. ③⑥ C. ④⑥ D. ②③⑤⑥
查看答案和解析>>
科目: 来源: 题型:
【题目】如图所示:把同样大小的滤纸碎片和乒乓球碎片,分开放在一块薄铜片的两侧,用酒精灯加热铜片的中部(假设铜片各处温度相等)。关于该探究燃烧条件的实验,下列说法中正确的是
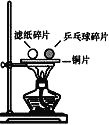
A. 实验中使用铜片,是利用了铜的导电性
B. 实验过程中滤纸碎片先燃烧,乒乓球碎片后燃烧
C. 乒乓球片和滤纸片切勿取大块,实验时要从侧面观察
D. 实验说明燃烧的条件之一是与氧气接触
查看答案和解析>>
科目: 来源: 题型:
【题目】碳酸钠在实际生产、生活中有着广泛的用途,如制造玻璃、造纸和纺织等。
(1)碳酸钠俗称苏打或____。如图为侯氏制碱法的流程图,通过步骤I后得到的悬浊液中有小苏打(在该溶液中难溶)和一种氮肥,请写出步骤I中发生反应的化学方程式:_____;上述过程中得到的氮肥遇碱会生成具有刺激性气味的______(填化学式),该气体能使_____;从流程图中可得出小苏打的一条化学性质是_____。
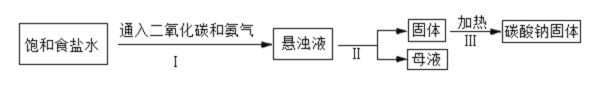
(2)氢氧化钠在空气中容易变质生成碳酸钠,现有放在空气中一段时间的氢氧化钠溶液,其中溶质的成分可能是:猜想①:NaOH;猜想②:Na2CO3;猜想③:_____。请设计实验证明猜想③正确。(写出相关的步骤和现象)________
(3)某海洋化工集团生产的碳酸钠产品中含有少量氯化钠杂质,其产品包装袋上标明:碳酸钠≥96%。为测定该产品中碳酸钠的质量分数,现取11.0g碳酸钠样品放入烧杯中,称得烧杯及所盛碳酸钠样品的总质量为158.0g,然后向烧杯中加入100g稀盐酸,充分反应,实验数据记录如下:
反应时间/min | 3 | 6 | 9 | 12 |
烧杯及所盛物质的总质量/g | 255.8 | 254.0 | 253.6 | 253.6 |
请你据此分析计算,该产品中碳酸钠的质量分数_____(是、否)符合标准。(写出计算过程,结果精确到0.1%)
查看答案和解析>>
科目: 来源: 题型:
【题目】九年级某班的化学兴趣小组同学对“氢氧化钠与稀盐酸的中和反应”进行了实验探究。小组同学采用的是测量溶液温度变化的方法。向一定体积10%的氢氧化钠溶液中滴加10%的稀盐酸,并对反应过程中溶液的温度与加入稀盐酸体积的变化进行记录,结果如图所示:
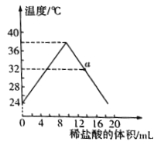
(1)据图判断a点时溶液显___性。
(2)拓展探究:该小组同学的实验中除了温度变化,没有其他明显现象,用什么方法可以证明溶液温度达到最高时,此反应恰好完全反应呢?请你帮助该小组同学设计一个实验方案。(1.写出实验操作、预期现象及结论;2.采用除了测pH值以外的方法)_______
查看答案和解析>>
科目: 来源: 题型:
【题目】根据下列实验装置图,回答有关问题:
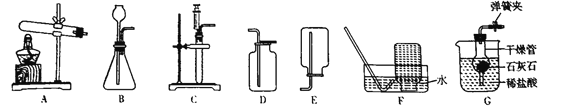
(1)实验室常用锌粒和稀硫酸反应制取氢气,若要控制产生氢气的速率,应选择的发生装置和收集装置是_____(从A~F中选择)。
(2)实验室现用G装置制取二氧化碳气体。
①将装有石灰石的干燥管放入装有稀盐酸的烧杯内,同时打开弹簧夹,写出干燥管内发生反应的化学方程式:_____。
②一段时间后,关闭弹簧夹,反应停止,其原理是_____。
查看答案和解析>>
科目: 来源: 题型:
【题目】化学兴趣小组同学用红磷燃烧的方法对空气中氧气的含量进行测定,实验过程中红磷足量、装置气密性良好、操作规范,实验结束后测定结果却低于20%,用测定氧气浓度的传感器测得反应后装置内氧气浓度为8.85%。小组同学查阅资料后改用足量白磷进行实验,测得反应后装置内氧气浓度为3.21%。请回答下列问题:
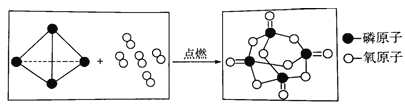
(1)白磷燃烧的微观示意图如图,写出白磷燃烧的化学方程式_____。
(2)采用教材装置测定空气中氧气含量时,改用白磷能使测定结果更准确的原因是_____。
查看答案和解析>>
科目: 来源: 题型:
【题目】在如图所示的转盘中,A~F分别代表Na2CO3、NaNO3、NaOH、HNO3、Na2SO4、NaCl六种物质中的一种。B的俗名为纯碱,E的物质类别为酸,A、B、C、D、E都能转化成F,A、B、C、D能依次转化。请根据初中所学化学知识回答下列问题:
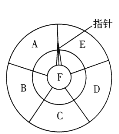
(1)F的化学式为____。
(2)让指针顺时针从当前位置开始转动,若所指物质不能转化为下一种物质,指针可继续转动,否则停止。则指针将停止在_____ (填字母编号)物质上。
(3)写出C转化成D的化学方程式: ______。
查看答案和解析>>
科目: 来源: 题型:
【题目】下图是A、B两种物质的溶解度曲线,请回答:
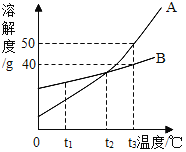
(1)在其他条件不变的情况下,若把t2℃时A、B的饱和溶液分别降温至t1℃,此时两种溶液中溶质的质量分数的大小关系为A____(填“>”“<”或“=”)B。
(2)若B物质中混有少量A物质,要提纯B物质,可采用的方法是_____。
(3)t3℃时,把70gB的饱和溶液稀释为10%,需要加水___g。
查看答案和解析>>
科目: 来源: 题型:
【题目】(1)如图是某微型实验的装置图,试管中的反应发生后,a、b两处及烧杯中的现象是________。
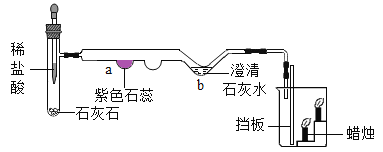
(2)采用微型实验装置的优点是____________(答出一条即可)。
查看答案和解析>>
科目: 来源: 题型:
【题目】某溶液含有Cu(NO3)2和AgNO3,先向其中加入一定量的铁粉进行处理,并绘制参加反应的铁与溶液中溶质种类的关系图(如下图)。下列说法正确的是( )

A. 当参加反应的铁的质量为m1时,溶质的种类、金属单质种类均为3种
B. 当参加反应的铁的质量为m1、m2时,两者溶液中Cu(NO3)2的质量分数相等
C. 溶质种类为2种时,金属单质种类可能为2种
D. 当溶质种类为1种时,金属单质种类可能为1种
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com