
科目: 来源: 题型:
【题目】为测定空气中氧气的含量,小华和小强同学分别设计如下方案:
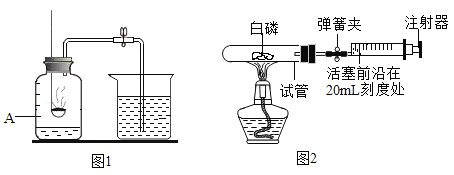
小华:采用图1装置进行实验.(燃烧匙中药品为红磷)
小强:图2将过量的白磷放入试管,通过导管与针筒注射器组成如图的实验装置.用小华设计实验,回答问题:
(1)红磷在集气瓶中燃烧的现象为_____化学式反应式为_____。
(2)待燃烧停止,装置冷却后,打开止水夹,观察到进入集气瓶中水的体积不到总容积的1/5,你认为其原因可能是_____(写2点)。
(3)如将燃烧匙中红磷换成硫粉,能否成功?为什么?_____。
(4)图2的设计操作与图1比较,其优点是_____(写2点)。
查看答案和解析>>
科目: 来源: 题型:
【题目】元素周期表是学习化学的重要工具。下表是元素周期表中的部分信息。
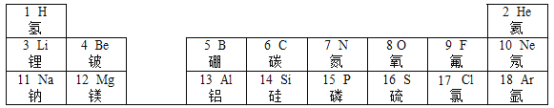
(1)画出硫原子的结构示意图_____,硫原子在化学反应中易得到电子,形成_____(填粒子符号)。
(2)在第二周期中,各原子结构的共同之处是_____。
(3)9号元素与17号元素化学性质相似的原因是_____。
(4)碳元素与氮元素的本质区别在于_____。
(5)等质量的钠、镁、铝,所含原子个数最多的是_____。
查看答案和解析>>
科目: 来源: 题型:
【题目】酸奶作为世界公认的长寿食品之一正愈来愈受到人们的重视和喜爱。酸奶中的酸味来自乳酸(化学式为C3H6O3)。
(1)酸奶主要提供人类营养物质中的哪一类?_____。乳酸在人体内可被完全氧化为CO2和H2O,1.8g乳酸完全氧化消耗O2的质量为_____g。
(2)为了测定某品牌酸奶中乳酸的含量,振华同学取100mL酸奶和100mL蒸馏水于烧杯中,慢慢滴入0.4%的NaOH溶液并不断搅拌,用传感器测得溶液pH随加入NaOH溶液体积V的变化关系如图所示。计算该酸奶中乳酸的含量为_____克每升。

(已知:乳酸的钠盐可表示为CH3CH(OH)COONa,测定所用NaOH溶液的密度为1.0g/mL,计算结果精确到0.01,无计算过程不给分)。
查看答案和解析>>
科目: 来源: 题型:
【题目】氯化钙(CaCl2)可用作干燥剂、混凝土防冻剂等。实验室用工业大理石(含有少量Al2O3、Fe2O3、SiO2等杂质)制备氯化钙的主要流程如下:

请回答下列问题:
(1)配制31%的稀盐酸730 g,需要36.5%的浓盐酸______g。
(2)酸溶时碳酸钙参与反应的化学方程式为_______。
(3)滤渣I的成分为____,滤渣II中含有Al(OH)3和______。
(4)过滤使用到的玻璃仪器有____。操作I采用的方法是:蒸发浓缩、_____、过滤。
(5)加入试剂a的目的是中和稍过量的石灰水,该反应的化学方程式为_____。
查看答案和解析>>
科目: 来源: 题型:
【题目】半水煤气是工业合成氨的原料气,其主要成分是H2、CO、CO2、N2和水蒸气。某化学兴趣小组为检验半水煤气的某些成分,设计的实验方案如下图所示。
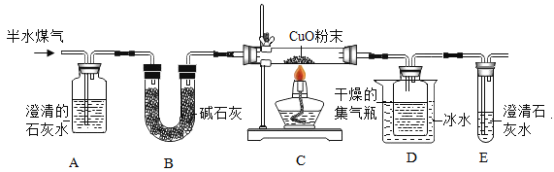
查阅资料可知碱石灰是CaO和NaOH的混合物。回答下列问题:
(1)A瓶中产生白色沉淀,证明半水煤气中含有_____,反应的化学方程式是____。
(2)B装置的作用是____。C装置的硬质玻璃管中发生置换反应的化学方程式是____。
(3)证明半水煤气中含有H2的现象是_____。
(4)证明半水煤气中含有CO的现象是____。
(5)测定半水煤气中H2、CO质量的实验方案如下:

若步骤Ⅳ中浓硫酸质量增加ag,步骤Ⅴ的KOH溶液质量增加bg,则半水煤气中H2与CO的质量比为______(用含字母a、b的代数式表示)。
查看答案和解析>>
科目: 来源: 题型:
【题目】实验室提供下列仪器:
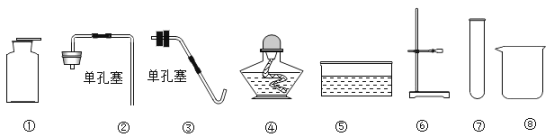
(1)用石灰石和稀盐酸制得CO2并观察CO2与石蕊溶液反应的现象,所需仪器按组装顺序依次是_____(填序号),发生化合反应的化学方程式是_____。
(2)用氯酸钾和二氧化锰制取O2,所需仪器按组装顺序依次是____(填序号),反应的化学方程式是____。
查看答案和解析>>
科目: 来源: 题型:
【题目】2019年是元素周期表诞生的第150周年,联合国大会宣布2019年是“国际化学元素周期表年”。下面是元素周期表中1~18号元素原子核外电子排布:
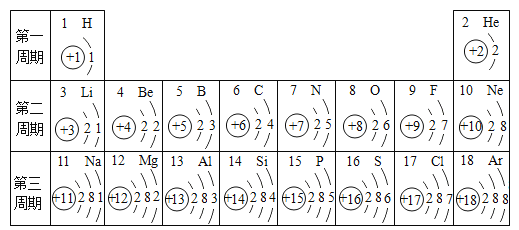
请回答下列问题:
(1)地壳中含量最多的金属元素原子核内质子数为_____,燃煤产生的两种氧化物易形成酸雨,组成这两种氧化物的元素中,原子序数最大的元素位于周期表中第____周期。
(2)第9号元素的钠盐常被添加到牙膏里以预防龋齿,该元素的离子结构示意图为_____。元素X的原子核外电子总数为最外层电子数的3倍,单质X在空气中燃烧生成的化合物化学式为____。
(3)在元素周期表中,19号元素钾与钠位于同一族,则钾原子的电子层数为____,金属钾与钠性质有许多相似之处,原因是____。
查看答案和解析>>
科目: 来源: 题型:
【题目】根据图所示溶解度曲线判断,下列说法正确的是
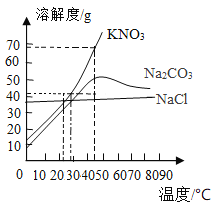
A. 28℃时,将40gKNO3溶于100g水得到饱和溶液
B. 将43℃的Na2CO3饱和溶液升高10℃,有晶体析出
C. 三种物质的饱和溶液由40℃降温至23℃,所得溶液中溶质质量:m(NaCl)=m(KNO3)>m(Na2CO3)
D. 除去KNO3中混有的Na2CO3,可在40 ℃配成饱和溶液,再降温结晶、过滤
查看答案和解析>>
科目: 来源: 题型:
【题目】高铁酸钾(K2FeO4)可用于净水,也可用作电池的电极材料,可通过下列反应制备:①MnO2+4HCl(浓)![]() MnCl2+Cl2↑+2H2O ②3Cl2+2Fe(OH)3+xKOH=2K2FeO4+6KCl+yH2O下列说法正确的是
MnCl2+Cl2↑+2H2O ②3Cl2+2Fe(OH)3+xKOH=2K2FeO4+6KCl+yH2O下列说法正确的是
A. 在反应①中,氯的化合价全部发生了改变
B. 反应②中x=10,y=6
C. 反应①②中共涉及了5种类型的化合物
D. 上述反应不属于四种基本反应类型中的任何一种
查看答案和解析>>
科目: 来源: 题型:
【题目】大连物化所研究发现,利用催化剂在低温下可将甲烷转化为甲醇,其反应微观示意图如图。下列说法错误的是
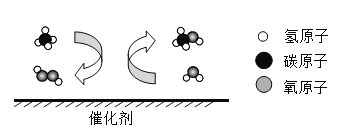
A. 甲醇的化学式为CH4O
B. 图示物质中有3种氧化物
C. 该反应中分子、原子个数均不变
D. 催化剂在反应前后质量不变
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com