
科目: 来源: 题型:
【题目】水是人类生活中不可缺少的物质.2016年3月22日是第二十四届“世界水日”,今年的宣传主题是“水与就业”,请回答下列问题:
(1)净水时,常用_________ 做吸附剂除去水中的色素和异味.如果想知道海水是软水还是硬水,可加入_________ 来检验.生活中降低水的硬度的方法为__________.
(2)氢气是理想的清洁高能燃料,以水为原料生产氢气的方法有多种.
方法Ⅰ:电解水法.小花同学设计了如图电解水简易装置,其中A、B电极由金属曲别针制成,通电后的现象如图所示.
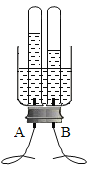
与A电极相连的试管中收集到的气体是________,电解水的化学方程式为:__________.如果A试管内收集到10毫升气体,理论上B试管内可以收集到________毫升气体.
方法Ⅱ:光解水法.我国科学家已研制出在新型高效光催化剂作用下,利用太阳能分解水制氢气.水在通过并接触催化剂表面时,分解的微观过程用示意图表示如下:(“○”表示氢原子,“●”表示氧原子,“![]() ”表示催化剂).
”表示催化剂).
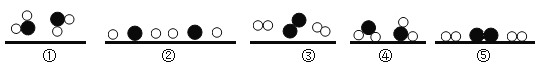
则水分解微观过程的正确顺序是 _____(填数字序号).上述过程中,不能再分的微粒是______.
(3)有些科学家预言:“世界上最后一滴水就是人类的眼泪”.这句话警示我们应树立保护水资源的意识:一是节约用水,二是防止水体污染.请你举一例节约用水的做法_________:
查看答案和解析>>
科目: 来源: 题型:
【题目】了解物质的结构,有利于理解和认识化学问题。
(1)稀土元素铕(Eu)是激光及原子能应用的重要材料。已知氯化铕的化学式为EuCl3(铕元素部分信息如图所示)。
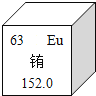
①该铕元素的相对原子质量为_____;
②该铕原子的核外电子数为_____;
③氧化铕的化学式为________。
(2)下图为A、B、C、D是四种微粒的结构示意图。
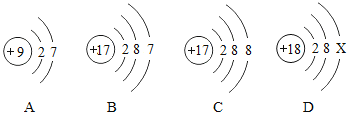
①A、B、C、D中属于阴离子的是__________(填序号);
②A、B、C、D中属于同种元素的微粒是_________(填序号);
③A微粒的化学性质与B、C、D中哪一种微粒的化学性质相似____________(填序号);
④具有相同原子数和电子数的分子或离子叫等电子体,等电子体具有相似的结构和性质。下列各组微粒中属于等电子体的是________(填字母序号)。
A NO和O2 B CO和N2 C SO2和CO2 D H2O和NH3
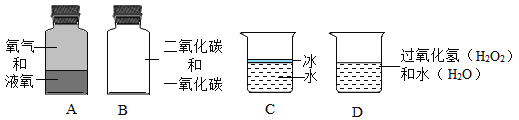
(3)分别盛有下列不同物质的容器中,所盛物质属于氧化物的是_____________(填字母)
查看答案和解析>>
科目: 来源: 题型:
【题目】化学符号是学好化学的基础,身边的化学物质有多种用途.
(1)用化学符号表示:
①两个铝原子__________
②三个氮分子______
③人体中含量最多的物质_________
④铁锈的主要成分_____
(2)现有四种物质,选择相应物质的字母填空:
A 焦炭 B 干冰 C 武德合金 D 汞
①_____________可用作工业炼铁的原料
②___________是温度计中常用的金属
③____________可用作人工降雨
④____________可制作保险丝
(3)按要求写出有关化学方程式
①铁丝在氧气中燃烧___________________;
②锌与稀硫酸反应___________________;
③一氧化碳还原四氧化三铁____________;
④硝酸铵受热分解生成N2O气体和水______。
查看答案和解析>>
科目: 来源: 题型:
【题目】下列各项指定数据前者小于后者的是
选项 | 数据 | ||
A | 溶液温度 | 室温下10gNH4NO3溶于100g水 | 室温下10gNaOH溶于100g水 |
B | 氧元素的质量分数 | 甲醛(HCHO) | 葡萄糖(C6H12O6) |
C | 二氧化碳的体积分数 | 人体呼出的气体 | 人体呼入的气体 |
D | 含碳量 | 生铁 | 钢 |
A.AB.BC.CD.D
查看答案和解析>>
科目: 来源: 题型:
【题目】学习结晶时,同学们对硝酸钾的制备产生浓厚兴趣.
(一)通过查阅资料发现硝酸钾在农业市场用途十分广泛.工业上常采用硝酸钠与氯化钾在一定条件下反应制得硝酸钾和氯化钠.然后再利用硝酸钾和氯化钠在不同温度下的溶解度不同可将其分离,具体流程可以表示为:
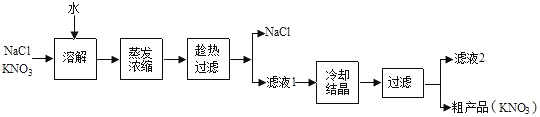
(1)溶解时需要不断搅拌,其目的是_____.
(2)化学实验室蒸发操作所需的玻璃仪器除玻璃棒外还有_____.
(3)分离氯化钠晶体和滤液1时需要趁热过滤的目的是_____.
(4)滤液1一定是_____的饱和溶液.
(5)冷却结晶后获得的硝酸钾晶体中还混有少量的NaCl,为获得更纯净的KNO3,还应进行的操作是洗涤、干燥,洗涤最佳的洗涤剂为_____.
A 常温下的蒸馏水 B 饱和的NaCl溶液 C 饱和的KNO3溶液
(6)洗涤后的液体应该_____.
A 不经处理直接排放到下水道
B 不经处理直接排放到农田
C 倒入原混合溶液中,节约资源并提高产率
(二)为测定洗涤前的粗产品中硝酸钾的质量分数,设计如下实验:取5g粗产品配成50g溶液,然后加入过量的硝酸银溶液(已知NaCl+AgNO3═AgCl↓+NaNO3,硝酸钾和硝酸银不反应),根据沉淀质量先求出NaCl质量,再确定硝酸钾的质量分数.
(7)硝酸银溶液需要过量的原因是_____,证明硝酸银已过量的方法是:静置后,在上层清液中加入硝酸银溶液,如果观察到_____(填有或无)沉淀生成,则已过量.
(8)在其他操作均正确的情况下,若在配制溶液过程中,仰视刻度量取蒸馏水,则所配制溶液中的硝酸钾的质量分数_____(填偏大、偏小或无影响),对所测定的粗产品中硝酸钾的质量分数_____.(填偏大、偏小或无影响)
(9)经精确测定AgCl沉淀的质量为1.435g,则5g粗产品配成的50g溶液中NaCl的质量分数为_____;该粗产品中硝酸钾的质量分数_____.(写出计算过程,相关物质的相对分子质量:NaCl 58.5,AgCl 143.5).
查看答案和解析>>
科目: 来源: 题型:
【题目】含杂质的Fe2O3固体样品20g,高温下用足量的CO完全还原(杂质不与CO反应),将生成的CO2气体用足量的澄清石灰水充分吸收后,产生30g白色沉淀。则下列说法正确的是
A. 通入的CO质量为8.4g B. 反应后剩余固体质量为11.2g
C. 样品中氧化铁的质量分数为80% D. 样品中氧元素质量分数一定为24%
查看答案和解析>>
科目: 来源: 题型:
【题目】某实验小组用氯酸钾和二氧化锰为原料制取氧气,反应过程中测量的有关数据记录如下:
反应时间(min) | 0 | 1 | 2 | 3 | 4 |
试管中固体质量(g) | 13.25 | 11.65 | 10.05 | 8.45 | 8.45 |
(1)反应到____min时,氯酸钾就完全分解。
(2)反应完全时生成氧气的质量为________。
(3)原固体中氯酸钾的质量是____?
(4)画出反应过程中生成氧气质量与时间的变化关系曲线____。
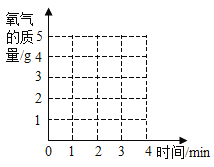
查看答案和解析>>
科目: 来源: 题型:
【题目】“塑化剂”是一种工业原料,但不法商人把它添加到饮用品当中,人喝了这样的饮用品,会对身体造成严重的危害。已知“塑化剂”的主要成分是邻苯二甲酸二辛酯,化学式为C24H38O4,完成下列问题:
(1)邻苯二甲酸二辛酯的相对分子质量是___。
(2)邻苯二甲酸二辛酯中碳、氢、氧三种元素的质量比是___。
(3)邻苯二甲酸二辛酯中碳元素的质量分数是___。(精确到0.1%)
(4)390克邻苯二甲酸二辛酯中碳元素的质量是___。
查看答案和解析>>
科目: 来源: 题型:
【题目】合成氨是人类科学技术上得一项重大突破,对社会发展与进步做出了巨大贡献。合成氨的工艺流程图如下:

(1)合成氨需要的氮气来自空气,空气中氮气的体积分数约为____。
(2)制取氢气的反应过程为:C+H2O![]() CO+H2。上述化学方程式中表现还原性的物质是___(填化学式)。
CO+H2。上述化学方程式中表现还原性的物质是___(填化学式)。
(3)写出N2、H2反应生成NH3的化学方程式_____,属于____反应。(填“化合反应”或“分解反应” )
(4)将沸点不同的气体分离开来,常采用液化分离法。如,控制温度在-183℃时,可将空气中N2与O2分离。根据下表中物质的沸点判断,要将产物NH3与N2、H2分离开来,最适宜的温度应该控制在_____℃。
物质 | H2 | N2 | O2 | NH3 |
沸点 | -252℃ | -195.8℃ | -183℃ | -33.35℃ |
查看答案和解析>>
科目: 来源: 题型:
【题目】化学是一门以实验为基础的学科。根据下图回答问题:

(1)仪器①的名称是_____。
(2)实验室用氯酸钾和二氧化锰制取氧气,反应的化学方程式为__,选用的发生装置是_____(填字母序号,下同)。
(3)实验室制取二氧化碳,发生装置要能达到“随开随起,随关随停”,需要选用的仪器和用品有____;反应的化学方程式为______;选用的收集装置是C,则二氧化碳从_____(填导管的序号)进入。检验收集到的气体是二氧化碳方法是_____其中发生的反应方程式为_____
(4)我们发现H装置中蜡烛由低到高依次熄灭,说明二氧化碳具有的性质是____
(5)小明同学以废弃的“棒棒冰”塑料管为材料,制成的气体发生装置(各部分连接紧密后,如图所示)。

该实验设计的优点有:能控制反应速率和_____。(写一点即可)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com