
ΩΤΡΩΘΚ ά¥‘¥ΘΚ Χβ–ΆΘΚ
ΓΨΧβΡΩΓΩΜ·―ß”Ο”ο «―ßœΑΜ·―ßΒΡ÷Ί“ΣΙΛΨΏΘ§ «ΙζΦ Ά®”Ο”ο―‘ΓΘ«κ”Ο Β±ΒΡΜ·―ß”Ο”οΧνΩ’ΓΘ
Θ®1Θ©ΚΛΤχ______ΘΜ
Θ®2Θ©2ΗωΟΨάκΉ”_____ΘΜ
Θ®3Θ©4ΗωΝρ‘≠Ή”______ΘΜ
Θ®4Θ©ΒΊΩ«÷–Κ§ΝΩΉνΕύΒΡΫπ τ‘ΣΥΊ_____ΘΜ
Θ®5Θ©3Ηω«βΖ÷Ή”_____ΘΜ
Θ®6Θ©5ΗωΙ·‘≠Ή”______ΘΜ
Θ®7Θ©Εΰ―θΜ·ΟΧ_______
Θ®8Θ©±ξ≥ωΙΐ―θΜ·«β÷–―θ‘ΣΥΊΒΡΜ·ΚœΦέ_____ΓΘ
≤ιΩ¥¥πΑΗΚΆΫβΈω>>
ΩΤΡΩΘΚ ά¥‘¥ΘΚ Χβ–ΆΘΚ
ΓΨΧβΡΩΓΩΓΑΚξΙέ±φ Ε”κΈΔΙέΧΫΈωΓ± «Μ·―ß―ßΩΤΒΡΚΥ–ΡΥΊ―χ÷°“ΜΘ§œ¬Ν–ΥΒΖ®’ΐ»ΖΒΡ «Θ®ΓΓΓΓΘ©
ΔΌΜ·―ß±δΜ·÷–Θ§Ζ÷Ή”ΚΆ‘≠Ή”ΒΡ÷÷άύΕΦ≤ΜΖΔ…ζΗΡ±δ
ΔΎ±υ―©»ΎΜ·ΒΡΙΐ≥Χ÷–Υ°Ζ÷Ή”÷°ΦδΒΡΦδΗτΖΔ…ζΝΥ±δΜ·
ΔέΆ§÷÷Ζ÷Ή”ΙΙ≥…ΒΡΈο÷ «¥ΩΨΜΈο
Δή2Fe3+ΚΆ3N÷–ΒΡΓΑ3Γ±ΕΦ±μ ΨΈΔΝΘΒΡΗω ΐ
ΔίΧΦ-14Θ®14CΘ©‘≠Ή”ΚΥΡΎΚ§”–6Ηω÷ Ή”ΚΆ8Ηω÷–Ή”
Δό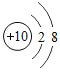 ΓΔ
ΓΔ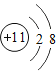 ΚΆ
ΚΆ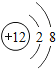 ±μ ΨΒΡΈΔΝΘΕΦ¥χΒγΚ…
±μ ΨΒΡΈΔΝΘΕΦ¥χΒγΚ…
A.ΔΌΔΎΔέB.ΔΎΔέΔίC.ΔΎΔήΔόD.ΔήΔίΔό
≤ιΩ¥¥πΑΗΚΆΫβΈω>>
ΩΤΡΩΘΚ ά¥‘¥ΘΚ Χβ–ΆΘΚ
ΓΨΧβΡΩΓΩœ¬Ν–Μ·―ßΖΫ≥Χ Ϋ ι–¥’ΐ»ΖΒΡ «Θ®ΓΓΓΓΘ©
A.2H2O![]() 2H2+O2
2H2+O2
B.2NaOH + CuCl2 = Cu(OH)2Γΐ + 2NaCl
C.2KMnO4®TK2MnO4+MnO2+O2
D.Zn+H2SO4®TZnSO4+H2
≤ιΩ¥¥πΑΗΚΆΫβΈω>>
ΩΤΡΩΘΚ ά¥‘¥ΘΚ Χβ–ΆΘΚ
ΓΨΧβΡΩΓΩ2019 Ρξ «ΓΑΙζΦ Μ·―ß‘ΣΥΊ÷ήΤΎ±μΡξΓ±
Θ®1Θ©÷–ΙζΩΤ―ß‘Κ‘Κ Ω’≈«ύΝΪΕ‘νςΓΔ“ΩΓΔ’ύΒ»ΒΡœύΕ‘‘≠Ή”÷ ΝΩΒΡ≤βΕ®Ήω≥ωΝΥΫή≥ωΙ±œΉΓΘ’ύ ‘ΣΥΊ‘Ύ‘ΣΥΊ÷ήΤΎ±μ÷–ΒΡ≤ΩΖ÷–≈œΔ»γœ¬ΆΦΥυ ΨΘ§’ύΒΡœύΕ‘‘≠Ή”÷ ΝΩΈΣ_________Θ§ΗΟ‘ΣΥΊ τ”Ύ-________Θ®ΧνΓΑΫπ τ‘ΣΥΊΓ±ΜρΓΑΖ«Ϋπ τ‘ΣΥΊΓ±Θ©ΓΘ

Θ®2Θ©÷–ΙζΩΤ―ßΦ“ΫΣ―©ΖεΒ±―ΓΈΣΓΑ»Ϊ«ρ«ύΡξΜ·―ßΦ“‘ΣΥΊ÷ήΤΎ±μΝρ‘ΣΥΊ¥σ ΙΓ±ΓΘ
ΔΌœ¬ΆΦ «Νρ‘≠Ή”ΫαΙΙ Ψ“βΆΦΘ§Νρ‘≠Ή”ΒΡΉνΆβ≤ψΒγΉ” ΐ «________ΘΜΝράκΉ”ΒΡΖϊΚ≈ΈΣ________ΘΜΝράκΉ””κΝρ‘≠Ή”ΒΡΜ·―ß–‘÷ ________Θ®ΧνΓΑœύΆ§Γ±ΜρΓΑ≤ΜΆ§Γ±Θ©ΓΘ
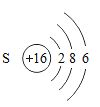
ΔΎΜπ“© «÷–ΙζΙ≈¥ζΥΡ¥σΖΔΟς÷°“ΜΓΘΚΎΜπ“©±§’®ΒΡΖ¥”ΠΈΣS+3C+2KNO3 ![]() X+3CO2Γϋ+N2ΓϋΘ§X ΒΡ Μ· ―ß Ϋ « ________ ΓΘ
X+3CO2Γϋ+N2ΓϋΘ§X ΒΡ Μ· ―ß Ϋ « ________ ΓΘ
≤ιΩ¥¥πΑΗΚΆΫβΈω>>
ΩΤΡΩΘΚ ά¥‘¥ΘΚ Χβ–ΆΘΚ
ΓΨΧβΡΩΓΩ“ΜΕ®ΧθΦΰœ¬Θ§Υ°‘ΎΟή±’»ίΤςάοΒΡά以Ιΐ≥Χ÷–Θ§Έ¬Ε»ΚΆ ±ΦδΒΡΙΊœΒ»γœ¬ΆΦΥυ ΨΓΘΔΌΓΔΔΎΓΔΔέ±μ ΨΥ°‘Ύ≤ΜΆ§ ±ΩΧΒΡ¥φ‘ΎΉ¥Χ§Θ§œ¬Ν–”–ΙΊ≈–Εœ’ΐ»ΖΒΡ «Θ® Θ©
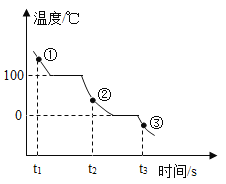
A.Υ°Ζ÷Ή”ΦδΒΡΦδΗτΘΚΔΌΘΨΔέB.Υ°Ζ÷Ή”ΒΡ‘ΥΕ·ΥΌ¬ ΘΚΔΎΘΨΔΌ
C.Ή¥Χ§ΔέΒΡΥ°Ζ÷Ή”Ψ≤÷Ι≤ΜΕ·D.ΔΌΓζΔΎΖΔ…ζΝΥΜ·―ß±δΜ·
≤ιΩ¥¥πΑΗΚΆΫβΈω>>
ΩΤΡΩΘΚ ά¥‘¥ΘΚ Χβ–ΆΘΚ
ΓΨΧβΡΩΓΩΈ“ΙζΒΡ±±ΕΖΒΦΚΫΈά–«œΒΆ≥≤…”Οο®‘≠Ή”÷”Θ§ΧαΙ©ΨΪ»Ζ ±ΦδΓΘ»γΆΦ «ο®‘ΣΥΊ‘Ύ‘ΣΥΊ÷ήΤΎ±μ÷–ΒΡœύΙΊ–≈œΔΘ§œ¬Ν–ΥΒΖ®’ΐ»ΖΒΡ «
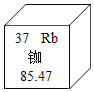
A. ο®‘ΣΥΊ τ”ΎΖ«Ϋπ τ‘ΣΥΊB. ο®‘ΣΥΊΒΡœύΕ‘‘≠Ή”÷ ΝΩΈΣ85.47g
C. ο®‘≠Ή”ΒΡ÷ Ή” ΐΒ»”Ύ÷–Ή” ΐD. ο®‘ΣΥΊΒΡ‘≠Ή”–ρ ΐΈΣ37
≤ιΩ¥¥πΑΗΚΆΫβΈω>>
ΩΤΡΩΘΚ ά¥‘¥ΘΚ Χβ–ΆΘΚ
ΓΨΧβΡΩΓΩ ·Μ“ · «÷ς“ΣΩσ≤ζΤΖ÷°“ΜΘ§Ρ≥―ß–Θ―–ΨΩ–‘―ßœΑ–ΓΉιΈΣΝΥ≤βΝΩΒ±ΒΊΩσ ·…Ϋ ·Μ“ ·÷–CaCO3ΒΡ÷ ΝΩΖ÷ ΐΘ§»Γ“Μ–©Ωσ ·―υΤΖΘ§≤Δ»ΓœΓ―ΈΥα200gΘ§ΤΫΨυΖ÷≥…4ΖίΘ§Ζ÷4¥ΈΫχ–– Β―ιΘ§ΫαΙϊ»γœ¬ΘΚ
Β―ι | 1 | 2 | 3 | 4 |
Φ”―υΤΖΒΡ÷ ΝΩΘ®gΘ© | 5 | 10 | 15 | 20 |
…ζ≥…CO2ΒΡ÷ ΝΩΘ®gΘ© | 1.76 | 3.52 | 4.4 | m |
Έ ΘΚΘ®1Θ©ΡΡΦΗ¥Έ Β―ι÷–Ωσ ·”– Θ”ύΘΩ_____ΓΘ
Θ®2Θ©±μ÷–mΒΡ ΐ÷Β «_____ΓΘ
Θ®3Θ© ‘ΦΤΥψ’β÷÷ ·Μ“ ·÷–CaCO3ΒΡ÷ ΝΩΖ÷ ΐ_____ΓΘ
Θ®4Θ© ‘ΦΤΥψ’β÷÷œΓ―ΈΥα»ή÷ ΒΡ÷ ΝΩΖ÷ ΐ_____ΓΘ
≤ιΩ¥¥πΑΗΚΆΫβΈω>>
ΩΤΡΩΘΚ ά¥‘¥ΘΚ Χβ–ΆΘΚ
ΓΨΧβΡΩΓΩΡ≥ΆΊ’Ι–‘―ßœΑ–ΓΉι‘Ύ―ß–ΘΩΤ―ß Β―ι¥¥–¬±»»ϋ÷–Θ§ΉωΝΥ“ΜΗω”–»ΛΒΡ Β―ιΘ§ΉΑ÷Ο»γΆΦΓΘ
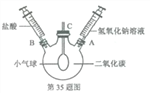
Β―ι…ηΦΤ»ΐΨ±…’ΤΩ÷–≥δ¬ζΕΰ―θΜ·ΧΦΤχΧεΘ§AΨ±ΓΔBΨ±Ζ÷±πΝ§Ϋ”≥δ¬ζ«β―θΜ·ΡΤ»ή“ΚΚΆ―ΈΥαΒΡΉΔ…δΤςΘ§CΨ±≤ε”–ΝΫΕΥΩΣΩΎΒΡ≤ΘΝßΒΦΙή(…λ»κΤΩΡΎΒΡ“ΜΕΥΝ§”––ΓΤχ«ρ)Θ§ΉΑ÷ΟΤχΟή–‘ΝΦΚΟΓΘ
Β―ι≤ΌΉςΘΚœ»Ά®ΙΐAΨ±ΆυΤΩΡΎΉΔ»κ«β―θΜ·ΡΤ»ή“ΚΘ§Ιέ≤λΒΫ–ΓΤχ«ρΒΡ–ΈΉ¥ΖΔ…ζΝΥ±δΜ·ΘΜΙΐ“ΜΕΈ ±ΦδΚσ‘ΌΆ®ΙΐBΨ±ΆυΤΩ÷–ΉΔ»κ―ΈΥαΘ§ΖΔœ÷–ΓΤχ«ρΒΡ–ΈΉ¥”÷ΖΔ…ζΝΥΗΡ±δΓΘ
«κΟη ω–ΓΤχ«ρ–ΈΉ¥ΒΡ±δΜ·«ιΩωΘ§≤ΔΕ‘¥ΥΉς≥ωΚœάμΒΡΫβ ΆΓΘ_________________________
≤ιΩ¥¥πΑΗΚΆΫβΈω>>
ΩΤΡΩΘΚ ά¥‘¥ΘΚ Χβ–ΆΘΚ
ΓΨΧβΡΩΓΩ–ΓΖΦ‘Ύ Β―ι “”Ο ·Μ“ ·ΚΆœΓ―ΈΥα÷Τ»ΓΝΥΕΰ―θΜ·ΧΦΘ§≤ΔΕ‘ Β―ι≤ζ…ζΒΡΖœ“ΚΫχ––»ή÷ ≥…Ζ÷ΦχΕ®ΘΚ»ΓΖœ“Κ…œ≤ψ«ε“Κ50ΩΥΘ§ΒΈΦ”÷ ΝΩΖ÷ ΐΈΣ26.5%ΒΡΧΦΥαΡΤ»ή“ΚΘ§≥ωœ÷Τχ≈ίΘ§ΒΈΦ”÷Ν10ΩΥΩΣ Φ≥ωœ÷ΑΉ…Ϊ≥ΝΒμΘ§ΦΧ–χΒΈΦ”÷Ν≥ΝΒμ≤Μ‘Ό≤ζ…ζΘ§Ιΐ¬ΥΘ§œ¥Β”Θ§Η…‘οΘ§≥ΤΒΟ≥ΝΒμ÷ ΝΩΈΣ5ΩΥΘ§≤ΔΜφ÷ΤΝΥΆΦœσΘ§»γΆΦΘΚ
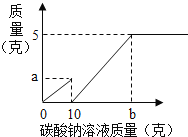
Θ®1Θ©ΆΦœσ÷–ΒΡaΒψ ΐ÷Β
Θ®2Θ©Ζœ“Κ÷–Κ§”–ΒΡ»ή÷ « Θ®–¥Μ·―ß ΫΘ©
Θ®3Θ©Ά®ΙΐΦΤΥψΥΒΟςΘ§ΆΦœσΚαΉχ±ξ÷–bΒψ±μ ΨΒΡ»ή“ΚΒΡ÷ ΝΩ «Εύ…ΌΘΩ
≤ιΩ¥¥πΑΗΚΆΫβΈω>>
ΩΤΡΩΘΚ ά¥‘¥ΘΚ Χβ–ΆΘΚ
ΓΨΧβΡΩΓΩ–Υ»Λ–ΓΉι Β―ι÷–,ΫΪNaOH»ή“ΚΒΈ»κCuSO4»ή“Κ÷–Θ§ΫαΙϊ»ή“Κ÷–…ζ≥…ΝΥ«≥¬Χ…ΪΒΡΙΧΧεΓΘ”Ύ «Θ§ΥϊΟ«Ε‘ΗΟ«≥¬Χ…ΪΙΧΧεΒΡ≥…Ζ÷Ϋχ––ΧΫΨΩΓΘ
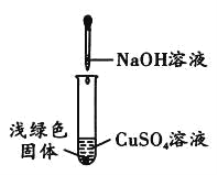
Θ®≤ι‘ΡΉ ΝœΘ©
ΔΌNaOH”κCuSO4Ζ¥”ΠΜα…ζ≥…CuΘ®OHΘ©2Θ§“≤Μα…ζ≥…Cu2Θ®OHΘ©2SO4Θ®Φν ΫΝρΥαΆ≠Θ©ΓΘ
ΔΎCuΘ®OHΘ©2‘Ύ80ΓφΜαΖ÷Ϋβ…ζ≥…CuO
ΔέCu2Θ®OHΘ©2SO4≤Μ»ή”ΎΥ°Θ§Ρή”κΥαΖ¥”ΠΘ§Ζ÷ΫβΈ¬Ε»–η300Γφ
Θ®≤¬œκ”κΦΌ…ηΘ©
≤¬œκ“ΜΘΚ«≥¬Χ…ΪΙΧΧεΈΣCuΘ®OHΘ©2ΘΜ
≤¬œκΕΰΘΚ«≥¬Χ…ΪΙΧΧεΈΣCu2Θ®OHΘ©2SO4ΘΜ
≤¬œκ»ΐΘΚ«≥¬Χ…ΪΙΧΧεΈΣCuΘ®OHΘ©2ΚΆCu2Θ®OHΘ©2SO4ΓΘ
Θ®Μώ»Γ ¬ Β”κ÷ΛΨίΘ©
Θ®1Θ©»Γ…ΌΝΩ«≥¬Χ…ΪΙΧΧεΖ≈»κ ‘Ιή÷–Θ§Φ”»»÷Ν100ΓφΘ§Ιέ≤λΒΫΚΎ…ΪΙΧΧεΈο÷ Θ§ΥΒΟς«≥¬Χ…ΪΙΧΧε÷–¥φ‘Ύ_____ΓΘ
Θ®2Θ©Νμ»Γ…ΌΝΩ«≥¬Χ…ΪΙΧΧεΖ≈»κ ‘Ιή÷–Θ§Φ”»κΉψΝΩœΓœθΥαΘ§‘ΌΒΈΦ”BaΘ®NO3Θ©2»ή“ΚΘ§≥ωœ÷ΑΉ…Ϊ≥ΝΒμΘ§ΗΟΑΉ…Ϊ≥ΝΒμ_____ΓΘΘ®ΧνΜ·―ß ΫΘ©
Θ®3Θ©Θ®Ϋα¬έΘ©Ζ÷Έω’ϊΗω Β―ιœ÷œσΘ§ΡψΡήΒΟ≥ωΒΡ Β―ιΫα¬έ «_____ΓΘ
Θ®4Θ©Θ®”Π”ΟΘ©Φν ΫΝρΥαΆ≠‘Ύ÷≤Έο±μΟφ…œΡή÷π≤Ϋ ΆΖ≈Ά≠άκΉ”Θ§“÷÷Τ’φΨζφΏΉ”Ο»ΖΔΚΆΨζΥΩΖΔ”ΐΘ§Ρή”––ßΖά÷ΈΉςΈοΒΡ’φΨζΦΑœΗΨζ–‘≤ΓΚΠΓΘ≈©“Β…œ≥Θ”ΟΉς_____ΓΘ
≤ιΩ¥¥πΑΗΚΆΫβΈω>>
ΙζΦ ―ß–Θ”≈―Γ - ΝΖœΑ≤αΝ–±μ - ‘ΧβΝ–±μ
Κΰ±± ΓΜΞΝΣΆχΈΞΖ®ΚΆ≤ΜΝΦ–≈œΔΨΌ±®ΤΫΧ® | Άχ…œ”–ΚΠ–≈œΔΨΌ±®Ή®«χ | Βγ–≈’©Τ≠ΨΌ±®Ή®«χ | …φάζ Ζ–ιΈό÷ς“ε”–ΚΠ–≈œΔΨΌ±®Ή®«χ | …φΤσ«÷»®ΨΌ±®Ή®«χ
ΈΞΖ®ΚΆ≤ΜΝΦ–≈œΔΨΌ±®ΒγΜΑΘΚ027-86699610 ΨΌ±®” œδΘΚ58377363@163.com