
科目: 来源: 题型:
【题目】KCl和KNO3在不同温度下的溶解度数据如表所示,下列说法中正确的是
温度/℃ | 20 | 30 | 60 | |
溶解度/g | KCl | 33 | 38 | 45 |
KNO3 | 31 | 64 | 110 |
A. 60℃时,100g水中最多溶解45 g KCl
B. 随着温度的升高,某饱和KCl溶液中会有固体析出
C. KNO3的溶解度始终大于KCl
D. 60℃时,某KNO3溶液中溶质的质量分数一定为 ![]()
查看答案和解析>>
科目: 来源: 题型:
【题目】有一包白色粉末,可能由 Na2CO3,BaCl2,NaOH,CuSO4 中的一种和几种组成,为了探究固体的成分,现做如下实验:
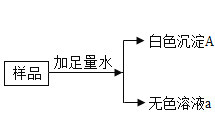

(1)原固体中一定没有_____________;
(2)原固体中一定有____________;
(3)生成气体的化学方程式_____________;
(4)无色溶液a 中一定含有的溶质____________;
(5)下列关于溶液和白色沉淀的设想,合理的是___________。
A除去硝酸钡中的硝酸,加入过量的白色沉淀A
B无色溶液a 能除去氯化钠中少量的盐酸
C鉴别盐酸和碳酸钠:用溶液 b、c、d
查看答案和解析>>
科目: 来源: 题型:
【题目】根据所学知识并结合下图所示装置回答问题。
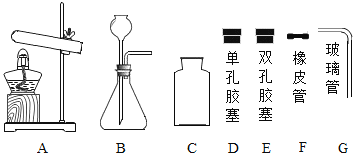
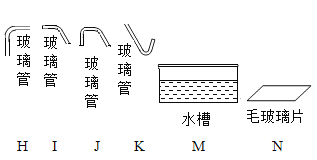
(1)图中能够提供热源的仪器名称是_________;
(2)在实验室里,用KMnO4来制取并用排水法收集氧气。
①该反应的化学方程式是_____________;
②除选用A装置外,还应该选择所给仪器中的F、I、K、M、N和______________。
(3)在实验室里,选用B装置和其它仪器组合制取二氧化碳并做性质实验。
①若要制取4.4g二氧化碳,需要含碳酸钙80%的大理石_____________g;
②用向上排空气法收集二氧化碳气体验满的操作是_____________。
查看答案和解析>>
科目: 来源: 题型:
【题目】现欲配制70g溶质质量分数为20%的氢氧化钠溶液,该实验的部分操作如下图所示:
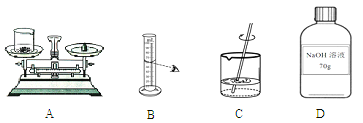
(1)需要称取氢氧化钠的质量是14g(使用了砝码和游码),若称量时出现了右盘高的现象(如图A),接下来的操作应该是___________;
A.向右移动游码 B.左盘中增加氢氧化钠 C.左盘中减少氢氧化钠
(2)若按照图B的方法量取水,会使配制的溶液质量分数______(选填“偏大”或“偏小”);
(3)D中所贴标签有一项内容不正确,请加以改正___________;
(4)若要将已配好的70g溶质质量分数为20%的氢氧化钠溶液,稀释成10%的氢氧化钠溶液,需要加水__________g。
查看答案和解析>>
科目: 来源: 题型:
【题目】我们常通过对比实验来获得信息。根据下图所示三个对比实验回答问题:
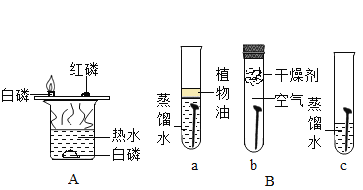
(1)实验 A 中,铜片上的白磷燃烧,而水下的白磷不燃烧,这说明可燃物燃烧的条件之一是_______;
(2)实验B 中,通过试管 a 和试管 c 内现象的对比,说明铁钉锈蚀的条件之一是与_________接触;
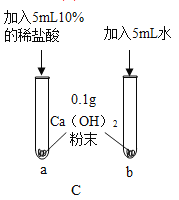
(3)实验C 中,试管___________内剩余的Ca(OH)2 粉末多。
查看答案和解析>>
科目: 来源: 题型:
【题目】结合验证铁、铜、银活动性的实验,回答下列问题:
(1)将铜丝和铁丝分别放入相同的浓度的稀H2SO4中,依据____________现象,可以判断 Fe 的活动性比Cu 强;
(2)将铜丝放入AgNO3 溶液中,Cu 与AgNO3 溶液反应的化学方程式为__________;
(3)铝比铁活泼,但铝比铁的耐腐蚀性强,原因是__________。
(4)向 AgNO3 和 Cu(NO3)2 的混合溶液中加入一定量的 Zn 粉,充分反应后过滤,向滤渣中加盐酸有气泡,则滤渣中一定含有的金属是__________。
查看答案和解析>>
科目: 来源: 题型:
【题目】分析甲、乙两种固体的溶解度曲线,回答问题。
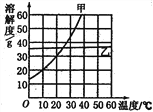
(1)在10℃时,甲的溶解度约是__________ g;
(2)使20℃时接近饱和的乙溶液变成饱和溶液,可以采取的方法之一是__________;
(3)将由50g甲、10g乙的混合物完全溶解在100g40℃的水中,当温度降低到20℃时,析出部分晶体,该晶体是__________ 。
查看答案和解析>>
科目: 来源: 题型:
【题目】根据给出的元素周期表中部分原子的结构示意图,回答下列问题。
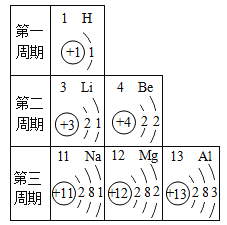
(1)原子序数为 20 的元素名称为____________;
(2)在化学反应中,Mg2+容易 ____________个电子变成镁原子;
(3)氧原子的结构示意图为____________,推测氧元素应排在 第__________周期。
查看答案和解析>>
科目: 来源: 题型:
【题目】某化学兴趣小组对酸、碱、盐的部分性质进行探究。
(探究一)氢氧化钠与二氧化碳反应
甲同学设计实验方案如图1所示:

(1)图1中的实验现象为_____________,甲同学由此判断氢氧化钠和二氧化碳发生了反应。
(2)小组内其他同学认为甲同学方案不完善,理由是________________。并对实验进行了改进,改进装置如图2所示:在A处放置适量干冰,B处装入适量的浓NaOH溶液,量筒中加入足量的稀盐酸,实验过程中,观察到量筒中有气泡冒出,原因是______________。一段时间后,观察到的现象是:①量筒中溶液倒吸入B中;②_________________,说明二氧化碳确实与氢氧化钠发生了反应。
(探究二)氢氧化钠和盐酸发生中和反应时放出热量
乙同学向一定量10﹪的氢氧化钠溶液中滴加10﹪的盐酸,滴加过程中温度变化如下表:
加入盐酸体积V/mL | 2 | 4 | 6 | 8 | 10 | 12 | 14 | 16 | 18 | 20 |
混合溶液温度T/℃ | 15.2 | 19.6 | 22.0 | 26.0 | 28.2 | 26.7 | 25.7 | 24.7 | 23.7 | 22.9 |
(3)反应的化学方程式为________________。
(4)根据表中数据分析混合溶液温度变化的原因_______________。
(5)小组内其他同学提出“将10﹪的盐酸直接滴入氢氧化钠固体中也能得出相同结论”,你认为是否合理并说明理由_______________。
(6)丙同学将甲同学和乙同学实验后的溶液混合,未发现明显现象。现将混合液中的氯化钠进行提纯,具体的操作为____________。
(探究三)碳酸钠溶液与稀盐酸的分步反应
(查阅资料)向碳酸钠溶液中逐滴加入稀盐酸的反应是分步反应,第一步反应生成碳酸氢钠和氯化钠,当碳酸钠反应完后才发生第二步反应。
丁同学向106g质量分数为10﹪的碳酸钠溶液中逐滴加入质量分数为3.65﹪的稀盐酸,生成二氧化碳的质量变化如图3所示(不考虑CO2的溶解)。
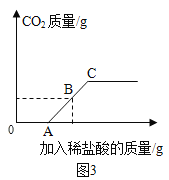
(7)A→Cspan>段发生反应的化学方程式为________________。
(8)若B点横坐标为150,则其纵坐标为______________。
查看答案和解析>>
科目: 来源: 题型:
【题目】工业上利用表面含有油污且生锈的废铁屑制备硫酸亚铁晶体。
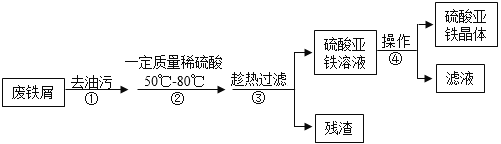
(1)下列能够去油污的试剂是__________(填字母)。
A水 B纯碱溶液 C明矾溶液 D稀硫酸
(2)步骤②中属于复分解反应的化学方程式是______________。控制“一定量稀硫酸”的目的是使铁过量,其原因是____________。
(3)步骤③要趁热过滤的原因是___________。
(4)步骤④的操作为___________、降温结晶、过滤、洗涤、干燥等。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com