
科目: 来源: 题型:
【题目】甲、乙、丙三种不含结晶水的固体物质的溶解度曲线如图所示,下列说法中正确的是( )
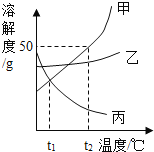
A.t2℃时将50g甲物质放入50g水中,充分搅拌后得到100g甲溶液
B.t2℃时配制等质量的三种物质的饱和溶液,甲所需要的水最少
C.分别将t2℃时三种物质的饱和溶液降温至t1℃,所得溶液中溶质的质量分数的大小关系为乙>甲=丙
D.分别将t2℃时三种物质的饱和溶液降温到t1℃,甲溶液中析出的晶体最多,丙溶液中无晶体析出
查看答案和解析>>
科目: 来源: 题型:
【题目】在一烧杯中盛有42.2gCaCO3和CaCl2的粉末状混合物,向其中加入188.8g水,使混合物中的可溶物完全溶解。然后再向其中逐滴加入溶质的质量分数为10%的稀盐酸,烧杯中难溶固体物质的质量与所滴入稀盐酸的质量关系曲线如下图X所示。请根据题意回答下列问题:
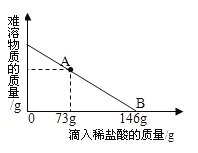
(1)在滴入稀盐酸的过程中,观察到的明显现象是:
①_______________ ,②_______________。
(2)当滴入10%的稀盐酸至图中A点时,烧杯中溶液里含有的溶质是(写化学式)________。
(3)当滴入10%的稀盐酸146g时(即B点),试通过计算,求此时烧杯中所得不饱和溶液的质量_____。(计算结果精确到0.1g)
查看答案和解析>>
科目: 来源: 题型:
【题目】城市生活垃圾的处理是世界性难题,某垃圾处理厂对生活垃圾进行处理与综合利用的部分流程如图:
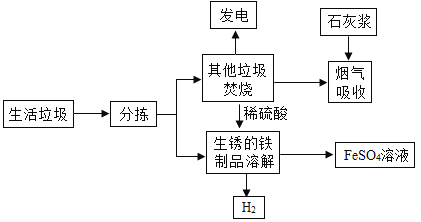
资料1:垃圾焚烧产生的烟气中含有SO2、HCl等有害气体
资料2:石灰浆的主要成分是氢氧化钙
资料3:+2价的铁元素容易被空气中的氧气氧化。
回答下列问题:
(1)吸收步骤中,石灰浆的作用是_____。
(2)溶解步骤中,产生的H2的化学方程式为_____。
除此反应外,溶解步骤还能发生两个反应:
①Fe2O3+3H2SO4═Fe2(SO4)3+3H2O
②Fe+Fe2(SO4)3═3FeSO4,
(3)将所得硫酸亚铁溶液在氮气环境中加热蒸发浓缩、冷却结晶、_____(填操作名称),得到硫酸亚铁晶体,其中氮气的作用是_____。
(4)请你就我们汕头市日常生活垃圾处理提一条建议:_____。
查看答案和解析>>
科目: 来源: 题型:
【题目】A﹣K为中学常见的物质,其中A为黑色粉末,H是一种建筑材料的主要成分,它们之间的转换关系如图所示。
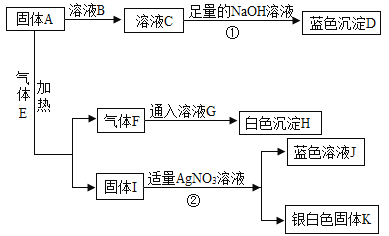
(1)D,F的化学式:D为_____,F为_____;
(2)A、H的名称:A为_____,H为_____;
(3)反应①的基本反应类型是_____;反应②的化学方程式是_____;
(4)气体E的用途是_____(写一条)。
查看答案和解析>>
科目: 来源: 题型:
【题目】如图是初中化学中常见仪器装置,回答下列问题:
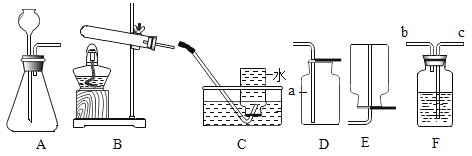
(1) D中仪器a的名称是_____________________。
(2)实验室用氯酸钾和二氧化锰制取氧气的化学方程式为_______________,选用的发生装置为_______________,(填装置编号,下同)。若收集一瓶氧气,供硫粉在氧气中燃烧的实验使用,最好选择的收集装置为_______________。
(3)用大理石和盐酸制取并收集二氧化碳,可选用的发生装置是_____________,收集装置为__。将生成的气体通入澄清石灰水,若无明显现象,可能的原因是_______________。
(4) F装置有多种用途。用于气体干燥、除杂时,气体应从_______________处进入(选填导管口编号)。干燥二氧化碳时,瓶中液体可以是_______________;除去一氧化碳中的二氧化碳时,瓶中液体可以是_______________。
查看答案和解析>>
科目: 来源: 题型:
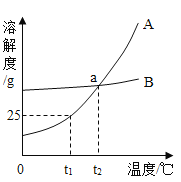
【题目】如图是甲、乙两物质(均不含结晶水)的溶解曲线,据此回答以下问题:
(1)t1℃时,A物质的溶解度为 g;
(2)a点的含义是 ;
(3)溶解度受温度影响小的物质是 ;
(4)从A、B的混合物中分离A物质,一般采用 的方法.
查看答案和解析>>
科目: 来源: 题型:
【题目】用“![]() ”和“
”和“![]() ”代表两种不同的单质分子,它们在一定条件下能发生化学反应,反应前后的微观示意图如下所示,下列说法正确的是
”代表两种不同的单质分子,它们在一定条件下能发生化学反应,反应前后的微观示意图如下所示,下列说法正确的是
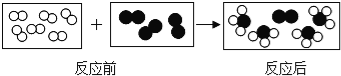
A. 该反应是化合反应
B. 该反应有2种生成物
C. 每个生成物分子由3个原子构成
D. 参加反应的“![]() ”和“
”和“![]() ”分子的个数比是2:1
”分子的个数比是2:1
查看答案和解析>>
科目: 来源: 题型:
【题目】纳米材料具有特殊的性质和功能.纳米二氧化钛![]() 参与的光催化反应可使吸附在其表面的甲醛等物质被氧化,降低空气中有害物质的浓度.正钛酸
参与的光催化反应可使吸附在其表面的甲醛等物质被氧化,降低空气中有害物质的浓度.正钛酸![]() 在一定条件下分解失水可制得纳米
在一定条件下分解失水可制得纳米![]() .下列说法不正确的是
.下列说法不正确的是
A. 甲醛对人体健康有害
B. 纳米![]() 添加到墙面涂料中,可消除甲醛
添加到墙面涂料中,可消除甲醛
C. 纳米![]() 与普通的
与普通的![]() 的性质、功能完全相同
的性质、功能完全相同
D. 制备纳米![]() 的反应:
的反应:![]()
查看答案和解析>>
科目: 来源: 题型:
【题目】我国药学家屠呦呦因发现了治疗疟疾的特效药青蒿素(挽救了全球数百万人的生命)于2015年10月获得诺贝尔医学奖。她在研究过程中曾关键性地用乙醚提取青蒿素。乙醚的化学式为C4H10O。请回答:
(1)每个乙醚分子中有_____个原子,乙醚的相对分子质量为_____;
(2)乙醚(C4H10O)中碳、氧元素质量比为_____;
(3)乙醚(C4H10O)中碳元素的质量分数是_____(精确到0.1%)。
查看答案和解析>>
科目: 来源: 题型:
【题目】电子工业常用30%的FeCl3溶液腐蚀覆盖有一薄层铜的绝缘板,制成印刷电路板。人们为了从废腐蚀液(含有CuCl2、FeCl2和FeCl3)中回收铜,并重新得到FeCl3溶液,设计如下实验流程。
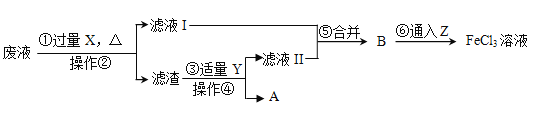
已知:2FeCl3+Fe=3FeCl2
(1)操作②、④的名称是_____;
(2)上述流程中,X的化学式为_____,加入过量的原因是_____,步骤③中有关反应的化学方程式为_____;
(3)Z为Cl2,第⑥步发生的反应为化合反应,此反应的化学方程式为_____。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com