
科目: 来源: 题型:
【题目】甲、乙、丙、丁4种初中化学常见的物质,由氢、碳、氧、钠中的1~3种元素组成。 用如图所示装置和试剂做了以下3个连续实验。

已知:酚酞溶液遇Na2CO3溶液、NaHCO3溶液均呈红色。
(1)打开K,将胶头滴管中的水挤入集气瓶中,振荡集气瓶,观察到烧杯中的导管口有气泡冒出,触摸集气瓶壁,感觉到微热。
① 已知甲为白色固体,有强烈的腐蚀性,易潮解,则甲的化学式为_____。
② 烧杯中导管口有气泡冒出的原因是_____。
(2)关闭K,打开集气瓶塞,将少量黑色固体乙点燃后,立即伸入瓶中,塞紧瓶塞,观察到乙在丙中剧烈燃烧,发出白光。燃烧产物丁分子的微观示意图为![]() ,则丙分子的微观示意图为_____。
,则丙分子的微观示意图为_____。
(3)待乙充分燃烧至熄灭后,冷却至室温,振荡集气瓶后,打开K,观察到烧杯中的溶液沿导管进入集气瓶,瓶中产生大量气泡。
①烧杯中的溶液进入集气瓶后产生气泡的原因_____(用化学方程式解释)。
② 充分反应后,集气瓶内溶液为无色,则溶液中的溶质除酚酞、NaCl外,还可能有_____。
查看答案和解析>>
科目: 来源: 题型:
【题目】某小组同学选择白磷和红磷作为可燃物,用下图装置探究可燃物的燃烧条件。实验过程中,瓶1、瓶2充入氧气,瓶3中充满80 ℃的热水,水槽中盛放80 ℃热水。
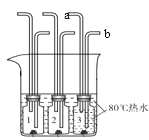
已知:白磷的着火点为40 ℃,红磷的着火点为240 ℃。
(1)磷燃烧的化学方程式为_____。
(2) 瓶1中加入少量白磷,瓶2、瓶3中分别加入_____,则可同时证明可燃物燃烧的两个条件。
(3)若仅利用瓶3证明“与氧气接触”是可燃物燃烧的条件之一,则相应的实验方案是_____。
查看答案和解析>>
科目: 来源: 题型:
【题目】实验室制备二氧化碳并除去其中的杂质。
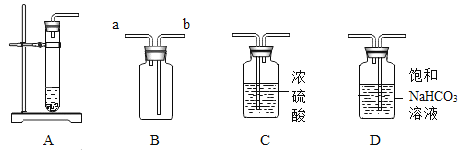
(1)利用装置A、B制取并收集二氧化碳。
① 制备二氧化碳的化学方程式为_____。
② 检验二氧化碳是否集满的操作是在a处放置_____。
(2)制得的二氧化碳中含有水蒸气、氯化氢等杂质气体。
① C中浓硫酸的作用是_____。
② D装置的作用是_____(用化学方程式表示)。
查看答案和解析>>
科目: 来源: 题型:
【题目】某同学用如图所示装置进行实验。
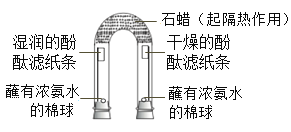
已知:浓氨水易释放出氨气。
(1)该实验能说明分子具有的性质是_____。
(2)若该实验能说明“氨气能与水发生化学反应”,则相应的实验现象是_____。
查看答案和解析>>
科目: 来源: 题型:
【题目】如图为家庭制氧机内桶构造示意图,桶上设有制氧剂投药口和出气口.已知:
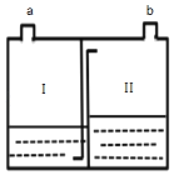
i.制氧剂的主要成分是过碳酸钠和催化剂
ii.本产品用于人体保健吸氧,产生的氧气需通入水中净化.
(1)制氧时,从投药口中投入药品后,立即将其关闭.
①过碳酸钠加入水中后,分解产生过氧化氢;过氧化氢再在催化剂的作用下产生氧气.过氧化氢发生反应的化学方程式为_____.
②氧气的出口为_____(填“a”或“b”).
(2)若在装置的Ⅰ、Ⅱ中放入其它试剂,可进行以下实验.
①检验碳酸盐:实验过程中,从a或b处加入试剂后,需将产生气体的一侧(a或b)密闭.其中,Ⅰ中盛放的试剂是_____.
②研究金属性质:I中加入铁屑和过量稀盐酸,II中只加入锌粒,关闭a口.一段时间后,II中可以观察到的现象有_____.
查看答案和解析>>
科目: 来源: 题型:
【题目】小丽欲在家配制100 g溶质的质量分数为10%的葡萄糖口服液。
(1)需要称取的葡萄糖的质量是_____g。
(2)在配制过程中,需要使用的器具包括_____(填字母序号)。
A  电子天平 B
电子天平 B ![]() 100 mL量杯 C
100 mL量杯 C  勺子 D
勺子 D  玻璃碗
玻璃碗
查看答案和解析>>
科目: 来源: 题型:
【题目】C60可用作吸氢材料,其原理是C60与H2在一定条件下反应生成氢化物;该氢化物在80 ~ 215 ℃时,会分解放出H2。
(1)C60属于_____(填字母序号)。
A 单质 B 化合物 C 混合物
(2)求算C60的相对分子质量的计算式为_____。
(3)C60可用作吸氢材料是利用了其_____(填“物理”或“化学”)性质。
查看答案和解析>>
科目: 来源: 题型:
【题目】元素周期律的发现对于寻找新材料、制备农药等具有重要作用。
(1)发现了元素周期律、制作出世界上第一张元素周期表的化学家是_____(填字母序号)。
A  门捷列夫 B
门捷列夫 B  达尔文 C
达尔文 C  牛顿
牛顿
(2)硅是重要的半导体材料。如图是元素周期表中硅元素的信息,由图可推知,硅原子的核外电子数为_____。

查看答案和解析>>
科目: 来源: 题型:
【题目】向一定质量的甲中加入乙,反应过程中,溶液的总质量与加入乙质量的关系能用下图曲线表示的是
甲 | 乙 | |
A | 稀盐酸 | 碳酸钙 |
B | CuSO4溶液 | 铁粉 |
C | NaOH溶液 | 稀盐酸 |
D | Ca(OH)2溶液 | CO2 |
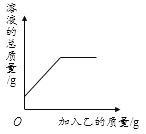
A.AB.BC.CD.D
查看答案和解析>>
科目: 来源: 题型:
【题目】M、N两种物质的溶解度曲线如图所示。t2℃时,分别将50 g的M、N固体加入到100 g水中,搅拌。下列说法不正确的是( )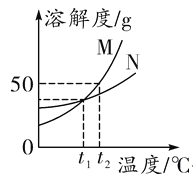
A. t2 ℃时,N固体不能完全溶解
B. t2 ℃时,M的饱和溶液中溶质的质量分数为50%
C. M的溶解度受温度变化的影响大于N
D. 分别将上述t2 ℃时 M、N的溶液降温到t1 ℃,得到M、N溶液的质量一定相等
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com