
科目: 来源: 题型:
【题目】常见的食品脱氧剂多为无机铁系脱氧剂,其主要成分为活性铁粉。果果自制脱氧剂(2g铁粉、0.5g活性炭、0.5g食盐),进行如下实验:
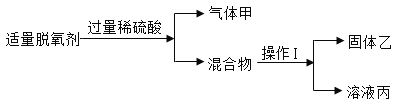
请回答:
(1)操作Ⅰ的名称是______,乙在水的净化的作用是______;
(2)写出生成气体甲的化学方程式为_________。溶液丙中含有的溶质是____(写化学式)。
查看答案和解析>>
科目: 来源: 题型:
【题目】为了探究某脱氧剂的成分(由两种单质组成),进行了如下实验:
(实验观察)脱氧剂为灰黑色粉末,若在空气中放置一段时间,有红棕色固体生成。
(实验猜想)根据颜色变化,猜想该脱氧剂中含有_____________(填化学式)。
(验证猜想)为验证该种成分,进行的具体操作方法为______________。
(实验探究)新取一定量的脱氧剂,将已验证的成分分离。取剩余固体与少量CuO混合,置于如图所示装置中加热。一会儿观察到黑色固体变红色,同时澄清石灰水变浑浊。

(实验结论)该脱氧剂中还含有___________(填化学式)。写出澄清石灰水变浑浊的化学方程式为__________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】阳光牌小包装“脱氧剂”成分为Fe粉、活性炭及少量NaCl、水。使用一段时间后,其中的Fe粉会转变成Fe2O3而变质。某化学兴趣小组欲探究使用过的阳光牌“脱氧剂”的变质程度(已变质的Fe粉占变质前Fe粉的质量分数),设计并进行如下探究过程。
步骤(1)取食品包装袋中的阳光牌“脱氧剂”一袋,将里面的固体溶于水,过滤、洗涤、干燥滤渣。
步骤(2)取步骤(1)中的滤渣8.0g,加入足量的稀H2SO4与滤渣充分反应,过滤、洗涤、干燥得固体1.2g。
步骤(3)取步骤(2)中的滤液,加入足量的NaOH溶液,得到的固体经洗涤后转移到坩埚中,充分加热、冷却、称量,得到8.0gFe2O3(注:滤液中的Fe元素已全部转化为Fe2O3)。
求(1)![]() 滤渣中Fe和Fe2O3两种物质的总质量____。
滤渣中Fe和Fe2O3两种物质的总质量____。
(2)该“脱氧剂”在未变质时,Fe粉和活性炭的质量之比____。
(3)该“脱氧剂”的变质程度____。
查看答案和解析>>
科目: 来源: 题型:
【题目】高铁酸钠(Na2FeO4)是一种高效多功能水处理剂,工业上常采用次氯酸钠(NaClO)氧化法生产,反应原理用化学方程式表示为3NaClO+2Fe(NO3)3+10NaOH=2Na2FeO4↓+3NaCl+6NaNO3+5H2O。(NaClO的相对分子质量为74.5;Na2FeO4的相对分子质量为166)。
(1)在Fe(NO3)3中,铁元素和氮元素的质量比为______(填最简比)。
(2)现称取44.7g次氯酸钠,最多能制得高铁酸钠的质量是多少?(列式计算)______
查看答案和解析>>
科目: 来源: 题型:
【题目】自来水厂净水过程示意图如图。请回答下列问题:
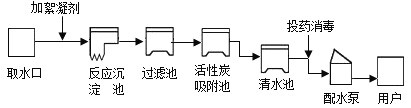
(1)除去水中固态杂质的设备是______(填序号)
A过滤池 B吸附池 C清水池
(2)吸附池中利用了活性炭所具有的很强的_____性,该过程属于____(填“物理”或“化学”)变化。
(3)生活中可以用________区别硬水和软水,常采用_________的方法降低水的硬度。
(4)通常向清水池投放高铁酸钠(化学式为Na2FeO4)杀菌消毒,高铁酸钠中铁元素的化合价为______;高铁酸钠(Na2FeO4)被广泛应用于自来水净化消毒,其原理为:4Na2FeO4+10____=4Fe(OH)3(胶体)+3____+8NaOH(请将化学方程式补充完整)。
(5)我国有关部门规定,经上述流程净化后进入用户的饮用水含铁<0.3mgL-1,含铜<1.0mgL-1,….其中的“铁、铜”指的是______(填序号)
A原子 B分子 C元素
查看答案和解析>>
科目: 来源: 题型:
【题目】高铁酸钠(Na2FeO4)是水处理过程中的一种新型净水剂,它的氧化性比高锰酸钾更强,本身在反应中被还原成三价铁离子达到净水的目的。它是由硝酸铁、氢氧化钠和氯气在一定条件下制得的,同时还生成硝酸钠和氯化钠等。
(1)写出制取高铁酸钠的化学方程式:______;
(2)在制取高铁酸钠的反应中______元素被氧化;
(3)高铁酸钠之所以有净水作用,除杀菌外,另一个原因是______。
查看答案和解析>>
科目: 来源: 题型:
【题目】高铁酸钠(Na2FeO4)是一种高效多功能水处理剂,工业上常采用次氯酸钠(NaClO)氧化法生产,反应原理用化学方程式表示为:3NaClO+2Fe(NO3) 3+10NaOH=2Na2FeO4↓+3NaCl+6NaNO3+5H2O
(1)次氯酸钠(NaClO) 中Cl元素的化合价为_____;
(2)高铁酸钠(Na2FeO4)中铁元素和氧元素的质量比为_____ (填最简比);
(3)现要制得830kg含杂质20%的高铁酸钠,至少需要次氯酸钠的质量是多少_________?(列式计算)
查看答案和解析>>
科目: 来源: 题型:
【题目】近年来,市场上木糖醇口香糖正逐渐取代蔗糖口香糖。请根据资料回答问题:
资料1:木糖醇是一种甜度相当于蔗糖、易溶于水的白色固体(木糖醇在某些温度下的溶解度分别为:30℃时70g、50℃时84g、60℃时90g)。
资料2:人体口腔中唾液正常的pH在6.6~7.1范围内,其酸性的增强不利于牙齿的健康。
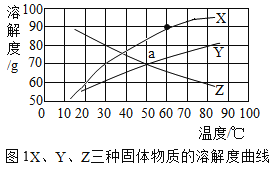
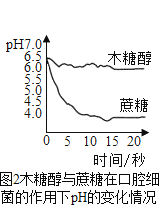
根据以上信息,回答下列问题:
(1)木糖醇具有的物理性质有_____(任写一点)。
(2)据图1判断:表示木糖醇溶解度曲线的是_____(选填“X”、“Y”、或“Z”),图中a 点表示的含义是_____。
(3)据图2 可知:在口腔细菌的作用下,木糖醇分解产物的酸性比蔗糖分解产物的酸性更_____(填“强”或“弱”),所以咀嚼木糖醇口香糖比蔗糖口香糖更有利于牙齿的健康。
查看答案和解析>>
科目: 来源: 题型:
【题目】近几年木糖醇(C5H12O5)作为新型甜味剂正在悄悄地代替蔗糖进入我们的生活。如图是木糖醇和蔗糖的溶解度曲线:

(1)通过比较木糖醇和蔗糖的溶解度曲线,在溶解度方面的一个共同点为_____。
(2)木糖醇入口后往往伴有微微的清凉感,这是因为它易溶于水,并在溶解时会_____(填“吸热”或“放热”)。
(3)有60℃的木糖醇和蔗糖的两种饱和溶液,欲使它们的溶质的质量分数相等,且仍为饱和溶液,可采取的一种方法是_____。
(4)木糖醇具有可燃性,它在足量的氧气中燃烧的化学方程式是_____。
查看答案和解析>>
科目: 来源: 题型:
【题目】近年来,市场上木糖醇口香糖正逐渐取代蔗糖口香糖,新型甜味剂木糖醇(C5H12O5)是一种甜度相当于蔗糖、易溶于水的白色粉末状固体。则回答:
(1)木糖醇的相对分子质量为_____;木糖醇_____(填“属于”或“不属于”)氧化物。
(2)现有15.2g木糖醇中碳元素质量与_____g葡萄糖(C6H12O6)中碳元素的质量相等。
(3)人们食用含糖较高的物质在口腔中细菌的作用下产生酸性物质,腐蚀牙齿,形成龋齿。则食用_____(填“蔗糖”或“木糖醇”)能有效的防止龋齿。
(4)合理开发利用木糖醇将具有十分看好的发展前景。若从化学角度来认识,你还想知道哪些信息呢?(只要一点即可)_____。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com