
【题目】已知:25 ℃时某些弱酸的电离平衡常数如表。
CH3COOH | HClO | H2CO3 |
Ka=1.75×10-5 | Ka=3.0×10-8 | Ka1=4.4×10-7 Ka2=4.7×10-11 |
下面图像表示常温下,稀释CH3COOH、HClO两种酸的稀溶液时,溶液pH随加水量的变化。
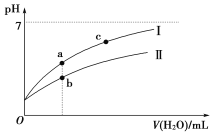
(1)相同浓度CH3COONa和NaClO的混合液中,各离子浓度的大小关系是____________________。
(2)向NaClO溶液中通入少量二氧化碳的离子方程式为______________。
(3)图像中a、c两点处的溶液中![]() ________(HR代表CH3COOH或HClO,填“相等”或“不相等”)。
________(HR代表CH3COOH或HClO,填“相等”或“不相等”)。
(4)图像中a点酸的总浓度________(填“大于”“小于”或“等于”)b点酸的总浓度。
【答案】(1)c(Na+)>c(CH3COO-)>c(ClO-)>c(OH-)>c(H+)(3分)
(2)ClO-+CO2+H2O===HClO+![]() (2分) (3)相等(2分) (4)小于(2分)
(2分) (3)相等(2分) (4)小于(2分)
【解析】根据表中电离平衡常数可知:酸性由强至弱的顺序为CH3COOH>H2CO3>HClO>![]() ,结合质子的能力由大到小的顺序为
,结合质子的能力由大到小的顺序为![]() >ClO->
>ClO->![]() >CH3COO-。
>CH3COO-。
(1)ClO-的水解程度大于CH3COO-的水解程度,同浓度CH3COONa和NaClO的混合液中,各离子浓度的大小关系应是c(Na+)>c(CH3COO-)>c(ClO-)>c(OH-)>c(H+)。
(2)由H2CO3的Ka1=4.4×10-7,Ka2=4.7×10-11,HClO的Ka=3.0×10-8,可知ClO-结合质子的能力大于HCO小于![]() ,离子方程式应为ClO-+CO2+H2O===HClO+
,离子方程式应为ClO-+CO2+H2O===HClO+![]() 。
。
(3)![]() 变形为
变形为![]() ,该式即为K电离/Kw,温度相同,则该式的值相等。
,该式即为K电离/Kw,温度相同,则该式的值相等。
(4)相同pH的CH3COOH和HClO,HClO的浓度大于CH3COOH的浓度,稀释到相同体积时,HClO(Ⅱ)浓度大于CH3COOH(Ⅰ)浓度。即a点酸(CH3COOH)的总浓度小于b点酸(HClO)的总浓度。


 阅读快车系列答案
阅读快车系列答案科目:高中地理 来源: 题型:
【题目】小华在实验室进行以下实验:将四个完全相同的空心薄铁皮球分别放入四个盛有密度为ρ(g/cm3)的食盐水的烧杯中,铁球所处的位置如图所示。然后,他将水、密度均为ρ(g/cm3)的三种溶液(CuSO4、AgNO3、稀硫酸)分别加入上述四个烧杯中。回答下列问题:
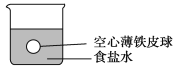
(1)加入水时,看到的现象是____________________________________________。
(2)加入稀硫酸时看到的现象是(假定整个反应过程中铁皮球壁完整)_____________________,发生反应的离子方程式是____________________________________________。
(3)加入CuSO4溶液时看到的现象是___________________________________________________,
发生反应的离子方程式是______________________________________________。
(4)加入AgNO3溶液时看到的现象是_________________________________,发生反应的离子方程式是_____________________________________________________。
查看答案和解析>>
科目:高中地理 来源: 题型:
【题目】氮的氧化物和硫的氧化物是导致酸雨的物质。
(1)形成酸雨的原理之一可简单表示如下:
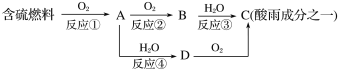
回答下列问题:
①酸雨的pH________(填“>”、“<”或“=”)5.6。
②D物质的化学式为____________。
③反应②的化学方程式为_________________________________________。
(2)在一定条件下氨气亦可用来将氮氧化物转化为无污染的物质。写出氨气和二氧化氮在一定条件下反应的化学方程式:__________________,反应中氧化剂是____________,还原剂是_______________。
(3)用氢氧化钠溶液可以吸收废气中的氮氧化物,反应的化学方程式如下:
NO2+NO+2NaOH===2NaNO2+H2O,2NO2+2NaOH===NaNO2+NaNO3+H2O
现有V L某NaOH溶液能完全吸收n mol NO2和m mol NO组成的大气污染物。
①所用烧碱溶液的物质的量浓度至少为________ mol·L1。
②若所得溶液中c(![]() )∶c(
)∶c(![]() )=1∶9,则原混合气体中NO2和NO的物质的量之比n∶m=______。
)=1∶9,则原混合气体中NO2和NO的物质的量之比n∶m=______。
③用含n和m的代数式表示所得溶液中![]() 和
和![]() 浓度的比值c(
浓度的比值c(![]() )∶c(
)∶c(![]() )=________。
)=________。
查看答案和解析>>
科目:高中地理 来源: 题型:
【题目】和下列离子反应方程式相对应的化学方程式正确的是
A.Cu2++2OH===Cu(OH)2——CuCO3+2NaOH===Cu(OH)2↓+Na2CO3
B.Ba2++![]() ===BaSO4↓——Ba(OH)2+H2SO4===BaSO4↓+2H2O
===BaSO4↓——Ba(OH)2+H2SO4===BaSO4↓+2H2O
C.Ag++Cl===AgCl↓——AgNO3+NaCl===AgCl↓+NaNO3
D.Cu+2Ag+===Cu2++2Ag↓——Cu+2AgCl===2Ag+CuCl2
查看答案和解析>>
科目:高中地理 来源: 题型:
【题目】为了制取纯净干燥的气体A,可用如图所示装置,生成A的速度可通过滴入液体B的速度控制,已知A是一种无色、无味、不能使酸碱指示剂变色、也不会在空气中燃烧的气体,但能使带火星的木条复燃。
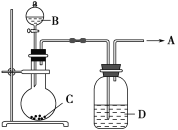
(1)A是________。
(2)若C是一种淡黄色固体,则烧瓶中发生反应的化学方程式是_____________________。
(3)若C是一种黑色粉末,则B物质是________,C物质的作用是_____________________。
(4)洗气瓶(广口瓶)中装的试剂D是________,其作用是______________________。所制得的气体用________法收集。
查看答案和解析>>
科目:高中地理 来源: 题型:
【题目】下表所示是几种弱电解质的电离平衡常数和某难溶电解质的溶度积Ksp(25 ℃)。
电解质 | 平衡方程式 | 电离平衡常数 | Ksp |
CH3COOH | CH3COOH | 1.76×105 | |
H2CO3 | H2CO3 HC | Ka1=4.31×107 Ka2=5.61×1011 | |
C6H5OH | C6H5OH | 1.1×1010 | |
H3PO4 | H3PO4
| Ka1=7.52×103 Ka2=6.23×108 Ka3=2.20×1013 | |
NH3·H2O | NH3·H2O | 1.76×105 | |
BaSO4 | BaSO4(s) | 1.07×1010 |
回答下列问题:
(1)由上表分析,若①CH3COOH,②![]() ,③C6H5OH,④
,③C6H5OH,④![]() 均可看成酸,则它们的酸性由强到弱的顺序为 (填编号)。
均可看成酸,则它们的酸性由强到弱的顺序为 (填编号)。
(2)25 ℃时,将等体积、等浓度的CH3COOH溶液和氨水混合,混合液中:c(CH3COO) (填“>”“=”或“<”)c(![]() )。
)。
(3)25 ℃时,向10 mL 0.01 mol·L1苯酚溶液中滴加V mL 0.01 mol·L1氨水,下列说法正确的是 (填序号)。
A.若混合液pH>7,则V≥10
B.若混合液pH<7,则c(![]() )>c(C6H5O)>c(H+)>c(OH)
)>c(C6H5O)>c(H+)>c(OH)
C.V=10时,混合液中水的电离程度小于10 mL 0.01 mol·L1苯酚溶液中水的电离程度
D.V=5时,2c(NH3·H2O)+2c(![]() )=c(C6H5O)+c(C6H5OH)
)=c(C6H5O)+c(C6H5OH)
(4)如图所示为某温度时BaSO4的沉淀溶解平衡曲线,下列说法不正确的是 (填序号)。
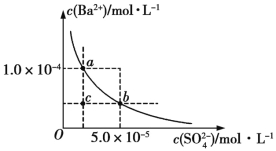
A.加入Na2SO4可使溶液由a点变为b点
B.在曲线上方区域(不含曲线)任意一点时,均有BaSO4沉淀生成
C.蒸发溶剂可能使溶液由c点变为曲线上a、b之间的某一点(不含a、b)
D.升高温度,可使溶液由b点变为c点
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com