
【题目】如图是部分短周期主族元素原子半径与原子序数的关系图,下列说法正确的是( )

A.M、N的氧化物都能与Z、R的最高价氧化物对应水化物反应
B.Y的单质能从含R简单离子的水溶液中置换出R单质
C.某物质焰色反应呈黄色,该物质一定是含Z元素的盐
D.X、M两种元素组成的化合物熔点很高
【答案】D
【解析】
同周期,自左而右,原子半径减小;同主族,自上而下,原子半径增大,故前7种元素处于第二周期,后7种元素处于第三周期,由原子序数可知,X为O元素,Y为F元素,Z为Na元素,M为Al元素,N为Si元素,R为Cl元素,据此分析解答。
根据上述分析可知:X为O元素,Y为F元素,Z为Na元素,M为Al元素,N为Si元素,R为Cl元素。
A.M、N的氧化物分别为氧化铝和二氧化硅,Z、R的最高价氧化物对应水化物分别为NaOH和高氯酸,氧化铝为两性氧化物,能够与氢氧化铝、高氯酸反应,但二氧化硅能够与氢氧化钠溶液反应,不能与高氯酸反应,故A错误;
B.Y的单质F2与水反应,无法从含有氯离子的溶液中置换出氯气,故B错误;
C.焰色反应是某些金属元素受热时发生电子跃迁而产生的现象,只要含有这种元素的任何物质都会产生同样的现象,所以焰色反应呈黄色的物质不一定是含Na的盐,也可能是含Na的碱、化合物、单质等,故C错误;
D.X、M两种元素组成的化合物为氧化铝,氧化铝为离子化合物,具有较高的熔点,故D正确;
故选D。


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
【题目】已知热化学方程式:C(金刚石,s)+O2(g)=CO2(g) △H1 ;
C(石墨,s)+O2(g)=CO2(g) △H2;
C(石墨,s)=C(金刚石,s)△H3=+1.9kJ/mol 下列说法正确的是
A. 金刚石比石墨稳定 B. △H1 > △H2
C. △H3=△H1 -△H2 D. 石墨转化成金刚石的反应是吸热反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)实验室用金属铜和稀硝酸制取NO的离子方程式为______________________。
(2)NO是有毒气体,某学生为防止污染,用分液漏斗和烧杯装配了一套简易的、能随开随用、随关随停的NO气体发生装置,如图甲所示。

①实验室若没有铜丝,而只有小铜粒,在使用上述装置进行实验时,可用丝状材料包裹铜粒以代替铜丝进行实验,这种丝状材料的成分可以是________(填序号)。
A.铁 B.铝 C.铂 D.玻璃
②打开分液漏斗的活塞使反应进行,在分液漏斗中实际看到的气体是红棕色的,原因是__________(填化学方程式)。
(3)为证明铜丝与稀硝酸反应生成的确实是NO,某学生另设计了一套如图乙所示的装置制取NO。反应开始后,可以在U形管右端观察到无色的NO气体。
①长玻璃管的作用是______________________________________________________。
②让反应停止的操作方法及原因是__________________________________________。
(4)以下收集NO气体的装置,合理的是________(填序号)。
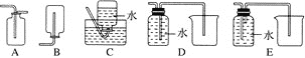
(5)将32.64 g铜与140 mL一定浓度的硝酸反应,铜完全溶解产生的NO和NO2混合气体在标准状况下的体积为11.2 L。请回答:
①NO的体积为________ L,NO2的体积为________ L。
②待产生的气体全部释放后,向溶液中加入VmLamol·L-1的NaOH溶液,恰好使溶液中的Cu2+全部转化成沉淀,则原硝酸溶液的浓度为________ mol·L-1。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】无水AlCl3(183℃升华)遇潮湿空气即变质,同时产生大量白雾,实验室可用下列装置制备。

(1)反应前,装置A中盛放浓盐酸的仪器名称是_____。
(2)反应时,装置A中发生反应的化学方程式是_____。
(3)装置B中盛放的是饱和NaCl溶液,作用是_____。
(4)装置F中试剂的作用是_____。
(5)装置G用于吸收多余Cl2,反应的离子方程式是_____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】碱式碳酸铜在烟火、农药、颜料、杀菌剂等方面应用广泛。一种以辉铜矿(Cu2S,含有SiO2和少量Fe2O3等杂质)为原料制备碱式碳酸铜的流程如图所示:

已知:①有关金属离子形成氢氧化物沉淀的pH范围如下:

②[Cu(NH3)4]SO4常温稳定,在热水中会分解生成NH3;
③Ksp[Fe(OH)3]=4.0×10-38。
回答下列问题:
(1)加快“浸取”速率,除将辉铜矿粉碎外,还可采取的措施有___(任写一种)。
(2)滤渣I经CS2提取后可获得一种淡黄色副产品,则滤渣I中的主要成分是___(填化学式)。回收淡黄色副产品过程中温度控制在50~60℃之间,不宜过高或过低的原因是___。
(3)常温下“除铁”时加入的试剂A可用CuO,调节pH的范围为___,若加A后将溶液的pH调为5,则溶液中Fe3+的浓度为___ mol/L。
(4)写出“沉锰”(除Mn2+)过程中反应的离子方程式:___。
(5)“赶氨”时,最适宜的操作方法是___。
(6)测定副产品MnSO4·H2O样品的纯度:准确称取样品14.00g,加蒸馏水配成100mL溶液,取出25.00mL用标准的BaCl2溶液测定,完全反应后得到了4.66g沉淀,则此样品的纯度为___(保留到小数点后两位)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关化学平衡常数的描述中正确的是( )
A. 化学平衡常数的大小取决于化学反应本身,与其他外界条件无关
B. 相同温度下,反应A+BC与反应CA+B的化学平衡常数相同
C. 反应2SO2(g)+O2(g)2SO3(g) ΔH<0的化学平衡常数随温度升高而增大
D. 反应A(g)+B(g)2C(g)的平衡常数表达式为K=![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据下列实验操作、现象所得出的结论正确的是( )
实验操作 | 现象 | 结论 | |
A | 向氯水中滴加硝酸酸化的AgNO3溶液 | 产生白色沉淀 | 氯水中含有Cl﹣ |
B | 向某溶液中滴加盐酸 | 有无色气体产生 | 溶液中一定有CO32﹣ |
C | 向某溶液中加入烧碱溶液后加热,用湿润的红色石蕊试纸检验 | 石蕊试纸变蓝 | 溶液中有NH4+ |
D | 将SO2通入到酸性KMnO4溶液中 | 溶液紫红色褪去 | SO2具有漂白性 |
A.AB.BC.CD.D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某温度下,在固定容积的容器中,可逆反应A(g)+3B(g)![]() 2C(g)达到平衡,此时测得n(A)∶n(B)∶n(C)=2∶2∶1。若保持温度不变,以n(A)∶n(B)∶n(C)=2∶2∶1的比例向该容器中再充入A、B和C,下列叙述正确的是
2C(g)达到平衡,此时测得n(A)∶n(B)∶n(C)=2∶2∶1。若保持温度不变,以n(A)∶n(B)∶n(C)=2∶2∶1的比例向该容器中再充入A、B和C,下列叙述正确的是
A. 刚充入时反应速率υ正减少,υ逆增大
B. 平衡不发生移动
C. 平衡向逆反应方向移动
D. 物质C的质量分数增大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】完成下列电化学习题:
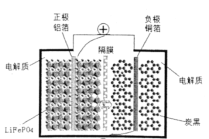
(1)某电池工作时的总反应可简化为:![]() ,电池中的固体电解质可传导Li+,则放电时,正极的电极反应式为________。充电时,Li+迁移方向为____(填“由左向右”或“由右向左”),图中聚合物隔膜应为____(填“阳”或“阴”)离子交换膜。
,电池中的固体电解质可传导Li+,则放电时,正极的电极反应式为________。充电时,Li+迁移方向为____(填“由左向右”或“由右向左”),图中聚合物隔膜应为____(填“阳”或“阴”)离子交换膜。
(2)使用间接电解法可处理燃煤烟气中的NO,装置如下图左。已知电解池的阴极室中溶液在pH在4~7(酸性)之间,试写出阴极的电极反应式______;用离子方程式表示吸收塔中除去NO的原理________。

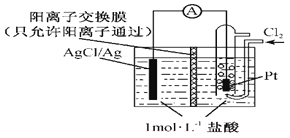
(3)某原电池装置如图所示,电池总反应为2Ag+Cl2=2AgCl。则负极反应为_______,放电时交换膜右侧溶液中酸性____(填“增强”、“减弱”或“不变”),若用KCl溶液代替盐酸,则电池总反应______(填“改变”或“不变”)。
(4)在生产和生活中采取了多种防止金属腐蚀的措施,利用原电池原理保护金属的方法是_______。
(5)纯锌与酸反应,为什么加入少许硫酸铜后会加速反应_________
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com