
【题目】无水AlCl3(183℃升华)遇潮湿空气即变质,同时产生大量白雾,实验室可用下列装置制备。

(1)反应前,装置A中盛放浓盐酸的仪器名称是_____。
(2)反应时,装置A中发生反应的化学方程式是_____。
(3)装置B中盛放的是饱和NaCl溶液,作用是_____。
(4)装置F中试剂的作用是_____。
(5)装置G用于吸收多余Cl2,反应的离子方程式是_____。
【答案】分液漏斗 MnO2+4HCl(浓)![]() MnCl2+Cl2↑+2H2O 除去氯气中氯化氢 防止空气中水进入装置E Cl2+2OH﹣=Cl﹣+ClO﹣+H2O
MnCl2+Cl2↑+2H2O 除去氯气中氯化氢 防止空气中水进入装置E Cl2+2OH﹣=Cl﹣+ClO﹣+H2O
【解析】
二氧化锰和浓盐酸反应制取氯气,氯气中含有氯化氢和水,装置B为饱和食盐水除去氯化氢,装置C中浓硫酸吸收水,装置D为制取无水氯化铝,装置E收集无水氯化铝,装置F的浓硫酸的作用是防止水进入装置E,以获得洁净的无水氯化铝,装置G是用强碱氢氧化钠吸收多余的氯气,据此分析。
(1)A中盛放浓盐酸的仪器名称是分液漏斗,故答案为:分液漏斗;
(2)反应时,装置A中发生反应的化学方程式是MnO2+4HCl(浓)![]() MnCl2+Cl2↑+2H2O,
MnCl2+Cl2↑+2H2O,
故答案为:MnO2+4HCl(浓)![]() MnCl2+Cl2↑+2H2O;
MnCl2+Cl2↑+2H2O;
(3)装置B中盛放的是饱和NaCl溶液,作用是除去氯气中氯化氢,故答案为:除去氯气中氯化氢;
(4)装置F中的浓硫酸的作用是防止空气中水进入装置E,故答案为:防止空气中水进入装置E;
(5)装置G是用强碱NaOH吸收多余的Cl2,防止污染大气,反应的离子方程式是Cl2+2OH﹣=Cl﹣+ClO﹣+H2O,
故答案为:Cl2+2OH﹣=Cl﹣+ClO﹣+H2O。


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
【题目】物质的量是高中化学计算的核心:
(1)相同物质的量的NH3和H2S的质量比___,分子个数比为___,同温同压下的体积比__,所含氢原子的个数比为____.
(2)现有m g某气体,它的一个分子由四原子构成,它的摩尔质量为M g/mol.设阿伏伽德罗常数为NA,则:
①该气体的物质的量为____mol.
②该气体中所含的原子总数为____个.
③该气体在标准状况下的体积为___L.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知在一定条件下2SO2(g)+O2(g)![]() 2SO3(g) ΔH=-QkJ·mol-1。向一密闭容器中加入2molSO2和1molO2,达平衡时SO2的转化率为90%,放出的热量为Q1;向另一相同容器中加入2molSO3,在相同条件下,达平衡时吸收的热量为Q2,则下列关系中正确的是( )
2SO3(g) ΔH=-QkJ·mol-1。向一密闭容器中加入2molSO2和1molO2,达平衡时SO2的转化率为90%,放出的热量为Q1;向另一相同容器中加入2molSO3,在相同条件下,达平衡时吸收的热量为Q2,则下列关系中正确的是( )
A. Q>Q1>Q2B. Q2>Q>Q1C. Q1>Q>Q2D. Q>Q1=Q2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B是两种有刺激气味的气体。试根据下列实验事实填空。
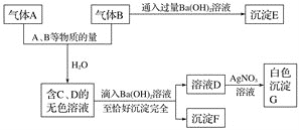
(1)写出A~F各物质的化学式:
A__________、B__________、C__________、D__________、E__________、F__________。
(2)写出A、B跟水反应的离子方程式:______________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】短周期主族元素 X、Y、Z、W 原子序数依次增大,X 是地壳中含量最多的元素,Y 原子的最外层只有一个电子,Z 位于元素周期表ⅢA族,W 与X属于同一主族。下列说法正确的是
A. 原子半径:r(W) > r(Z) > r(Y)
B. 由X、Y 组成的化合物中均不含共价键
C. Y 的最高价氧化物的水化物的碱性比Z的弱
D. X 的简单气态氢化物的热稳定性比W的强
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】水中溶解氧的测定方法如下:向一定量水样中加入适量MnSO4和碱性KI溶液,生成MnO(OH)2沉淀,密封静置;加入适量稀H2SO4,待MnO(OH)2与I完全反应生成Mn2+和I2后,以淀粉作指示剂,用Na2S2O3标准溶液滴定至终点,测定过程中物质的转化关系如下:
![]()
①写出O2将Mn2+氧化成MnO(OH)2的离子方程式:__________。
②取加过一定量CaO2·8H2O的池塘水样100.00 mL,按上述方法测定水中溶解氧量,消耗0.01000 mol·L1 Na2S2O3标准溶液13.50 mL。(已知反应:I2+2S2O32-=2I-+S4O62-)计算该水样中的溶解氧(以mg·L1表示),写出计算过程__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图是部分短周期主族元素原子半径与原子序数的关系图,下列说法正确的是( )

A.M、N的氧化物都能与Z、R的最高价氧化物对应水化物反应
B.Y的单质能从含R简单离子的水溶液中置换出R单质
C.某物质焰色反应呈黄色,该物质一定是含Z元素的盐
D.X、M两种元素组成的化合物熔点很高
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列不能用勒沙特列原理解释的是( )
A. Fe(SCN)3溶液中加入固体KSCN后颜色变深
B. 棕红色NO2加压后颜色先变深后变浅
C. SO2催化氧化成SO3的反应,往往需要使用催化剂
D. 高压比常压有利于NH3的合成
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图所示,将铁棒和石墨棒插入1 L 1 mol/L食盐水中。下列说法正确的是( )
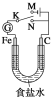
A. 若电键K与N连接,铁被保护不会腐蚀
B. 若电键K与N连接,正极反应式是4OH--4e-===2H2O+O2↑
C. 若电键K与M连接,将石墨棒换成铜棒,可实现铁棒上镀铜
D. 若电键K与M连接,当两极共产生28 L(标准状况)气体时,生成了1 mol NaOH
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com