
����Ŀ��Ϊ��֤��Ԫ�ر���Ԫ�طǽ�����ǿ��ij��ѧʵ��С���������ʵ�飬��ش��������⣺

(1)A��ҩƷ�����������Ļ�ѧ��Ӧ����ʽ____��������2.24 L Cl2(���)ʱ����������Ũ��������ʵ���Ϊ____��
(2)B���Լ�Ϊ_______����װ�õ�������_______��
(3)C��ʢ������Һ����װ�õ�������______��
(4)��D��KI��Һ����������_____��ͨ���۲쵽________��������֤����Ԫ�صķǽ����Դ��ڵ�Ԫ�ء�ָ������ʵ����ƵIJ���֮��_____��
(5)���Ķ�������Ϣ��
�������ˮ��Һ���Ա��Ȼ������ ��S2Cl2��������Ԫ����-1�� ��ͭ�������ڼ��������·�Ӧ�����Ȼ�ͭ��ͭ�����ڼ��������·�Ӧ��������ͭ �ܷе㣺���>���� �ݸ���������Դ�������
��֤����Ԫ�صķǽ����Ա���Ԫ��ǿ����______(�����)
���𰸡�MnO2+4HCl(Ũ)![]() MnCl2+Cl2��+2H2O 0.2mol �����Ȼ�����Һ ��ȥCl2��HCl ��������ɫ���� ���� ��Һ���� û��β������Cl2װ�� �ڢۢ�
MnCl2+Cl2��+2H2O 0.2mol �����Ȼ�����Һ ��ȥCl2��HCl ��������ɫ���� ���� ��Һ���� û��β������Cl2װ�� �ڢۢ�
��������
��1��Aװ��������ȡ����������������Ũ����Ͷ������̷�Ӧ�����Ȼ��̡�������ˮ�����Է�Һ©����ʢ�ŵ���Ũ���ᡢ��ƿ�м������MnO2����ѧ����ʽΪ MnO2+4HCl(Ũ) ![]() MnCl2+Cl2��+2H2O�����ݻ�ѧ����ʽ��֪������1molCl2����2molHCl��������������
MnCl2+Cl2��+2H2O�����ݻ�ѧ����ʽ��֪������1molCl2����2molHCl��������������![]() =0.1molCl2����������HClΪ0.2mol����ΪMnO2+4HCl(Ũ)
=0.1molCl2����������HClΪ0.2mol����ΪMnO2+4HCl(Ũ) ![]() MnCl2+Cl2��+2H2O��0.2mol��
MnCl2+Cl2��+2H2O��0.2mol��
��2��Ũ������лӷ��ԣ��������ɵ������к���HCl������ʳ��ˮ���ܽ�HCl���������������ܽ⣬�����ñ���ʳ��ˮ��ȥ�����е�HCl�����Թ��ƿ��ʢ�ŵ��DZ���ʳ��ˮ���������dz�ȥ�����е�HCl����Ϊ����ʳ��ˮ����ȥ�����е�HCl��
��3��Ҫ֤����Ԫ�صķǽ����Ա�SԪ��ǿ��������������������������S��ʵ�֣����ӷ���ʽΪCl2+S2-=S��+2Cl-�����������ɵ���ɫ����S����Ϊ�е���ɫ�������ɡ�
��4������I2�����۱���ɫ������I2���ʵ����ɣ������D��KI��Һ�������������ۣ�����Cl2+2KI=2KCl+I2��I2�����۱���ɫ������֤��Cl2�û�����I2��֤����Ԫ�صķǽ����Դ��ڵ�Ԫ�أ���ΪCl2���ж����壬���������ŷŵ������У�����ʵ��װ������һ��ʢ���ռ���Һװ�ã�Ŀ�������շ�Ӧ��ʣ������壬��ֹ��Ⱦ������
��Ϊ���ۣ�����ɫ��û��β������Cl2��װ�á�
��5������̬�⻯����Һ������ǿ����ǽ�����ǿ���ж��أ�Ӧ�ñȽ����ȶ��ԣ��ʢٴ���
��S2Cl2��������Ԫ����-1�ۣ�����Ԫ����+1�ۣ�˵���γɵĹ��õ��Ӷ�ƫ����Ԫ�أ�ƫ����Ԫ�أ�˵���������Ӷ�Cl>S������˵����Ԫ�صķǽ����Ա���Ԫ�صķǽ����������ʢ���ȷ��
��������ͭԪ�����������̬������+2�ۣ�����ֻ������ͭԪ������+1�ۣ�˵�������������Ը�ǿ��˵����Ԫ�صķǽ����Ա���Ԫ�صķǽ����������ʢ���ȷ��
����Ϊ��Ǻ�������Ϊ���Ӿ��壬�е㣺���>����, ֻ˵����Ƿ��Ӽ������������������Ӽ�����������ǽ�����ǿ���ж��أ��ʢܴ���
������������Ӧˮ���������ǿ˵���ǽ�����ǿ������������Դ������ᣬ˵����Ԫ�صķǽ����Ա���Ԫ�صķǽ����������ʢ���ȷ����Ϊ�ڢۢݡ�


 ��У����ϵ�д�
��У����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����з����У���������ʵ������ȡ������
A. �����Թ��е��Ȼ�粒���
B. ����ƿ�н���ʯ�Һ��Ȼ�炙�ϣ���ˮ������״�����
C. ����Һ©���е�Ũ��ˮ����װ����ʯ�ҵ���ƿ��
D. ����ƿ�е�Ũ��ˮ����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��25����101 kPa�£�2g����ȼ������Һ̬ˮ���ų�285.8kJ��������ʾ�÷�Ӧ���Ȼ�ѧ����ʽ��ȷ���ǣ� ��
A. 2H2(g)+O2(g) == 2H2O(1) ��H�� �D285.8kJ��mol![]()
B. 2H2(g)+ O2(g) == 2H2O(1) ��H�� +571.6 kJ��mol
C. 2H2(g)+O2(g) == 2H2O(g) ��H�� �D571.6 kJ��mol
D. H2(g)+1/2O2(g) == H2O(1) ��H�� �D285.8kJ��mol
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��һ������ȼ�ϵ�صĽṹʾ��ͼ������ʾ�����ڸõ�ص�������ȷ����(����)
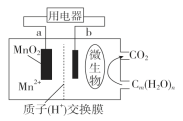
A. ��ع���ʱ��������a����b
B. �������ڵ缫���ŵ�ʱ������ԭ��Ӧ
C. �ŵ�����У�H����������������
D. ������ӦʽΪ��MnO2��4H����2e��===Mn2����2H2O
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��N2��H2�ϳ�NH3�������仯��ͼ��ʾ���÷�Ӧ���Ȼ�ѧ����ʽ�ǣ� ��
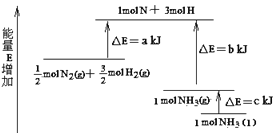
A.N2(g)��3H2(g)��2NH3(l) ��H��2(a-b-c)kJ/mol
B.N2(g)��3H2(g)��2NH3(g) ��H��2(b-a)kJ/mol
C.1/2 N2(g)��3/2H2(g)��NH3(l) ��H��(b��c-a)kJ/mol
D.1/2 N2(g)��3/2H2(g)��NH3(g) ��H��(a��b)kJ/mol
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������йظ����ж�����������ȷ���ǣ� ��
A.1mol H2ȼ�շų�������ΪH2��ȼ����
B.Na2SO3��H2O2�ķ�ӦΪ������ԭ��Ӧ
C.![]() ��
��![]() ��Ϊͬϵ��
��Ϊͬϵ��
D.BaSO4��ˮ��Һ�����磬��BaSO4���������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������Ϊ��ɫҺ�壬��ԭ��ǿ���ױ��������м��ԣ����ᷴӦ�����Ρ�������������H2�Ʊ���
![]() ��3H2
��3H2![]()
![]() ��2H2O��
��2H2O��
�䲿��װ�ü��й��������£�
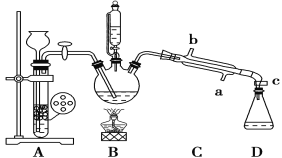
��Ŀ | �е�/�� | �ܶ�(g/mL) | �ܽ��� |
������ | 210.9 | 1.20 | ������ˮ���������Ҵ������� |
���� | 184.4 | 1.02 | ����ˮ���������Ҵ������� |
���� | 34.6 | 0.71 | ������ˮ�������������������� |
ʵ�鲽�裺
�ټ��װ�õ������ԣ����Ӻ�C������װ�õ���ˮ��
������������ƿ�м����ʯ������������ȡ�º�ѹ��Һ©���������¶ȼơ�
�۴�װ��A��B�������ͨ��H2һ��ʱ�䡣
�ܵ�ȼB���ľƾ��ƣ����ȣ�ʹ�¶�ά����140����з�Ӧ��
�ݷ�Ӧ�����ر�װ��A��B�������������ʯ�ҡ�
�������¶ȼƵ�λ�ã��������ȣ��ռ�182��186 ����֣��õ��ϴ�������
�ش��������⣺
��1����������¶ȼ�ˮ�����λ����________��
��2�����й���ʵ��������У��������________��
A�������ܵ���ˮӦ�ô�b����a��
B��ʵ�鿪ʼʱ���¶ȼ�ˮ����Ӧ���뷴ӦҺ�У����ڿ��Ʒ�ӦҺ���¶�
C��װ��A��Ӧʹ��п�ۣ������ڼӿ�����H2������
D�������ʯ��Ŀ���Ƿ�ֹ����
��3����ʵ���в���ۺܵ͢�˳��ߵ�����ʵ���п��ܲ����ĺ����_______��
��4������ǰ��������м�����ʯ�ҵ�������_______��
��5����ѧ�����ɷ�Ӧ��ɺ�ֱ������õ������Ĵ��Ȳ��ߣ�����������̣�
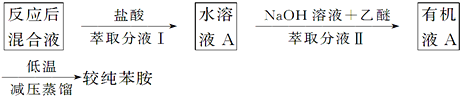
�����������������������ᱽ����ˮ��ȡ���ڼ�����Һ���ֱ����л��ܼ�����ȡ��������ȡ��������ȡ����Ʒ��͡�ʵ���з��͵�������___���ڷ�Һ©���н�����ȡ��Һʱ��Ӧע�ⲻʱ��������Ŀ����____��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij�������ֻ������Ե����̼�������缫���ϣ�������ZnSO4��Һ���л��߾�������̬����ʣ������ܷ�ӦΪMnO2+![]() Zn��(1+
Zn��(1+![]() )H2O��
)H2O��![]() ZnSO4
ZnSO4![]() MnOOH��
MnOOH��![]() ZnSO4[Zn(OH)2]3��xH2O.���ؽṹ��ͼ1��ʾ��ͼ2���л��߾���ĽṹƬ�Ρ�����˵���в���ȷ����
ZnSO4[Zn(OH)2]3��xH2O.���ؽṹ��ͼ1��ʾ��ͼ2���л��߾���ĽṹƬ�Ρ�����˵���в���ȷ����
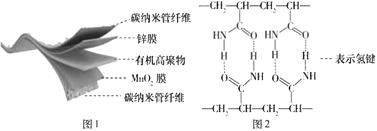
A.̼���ܾ��е����ԣ��������缫����
B.�ŵ�ʱ����ص�������ӦΪMnO2-e-+H+=MnOOH
C.���ʱ��Zn2+����ZnĤ
D.�ϳ��л��߾���ĵ�����![]()
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��SO2��NO�Ǵ�����Ⱦ�����SO2��NO�����Na2S2O4��NH4NO3��Ʒ������ͼ���£�CeΪ��Ԫ�أ���
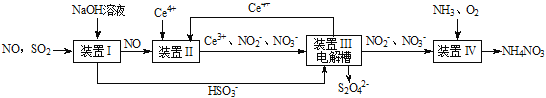
��1��װ�â�������HSO3-�����ӷ���ʽΪ_____ ��
��2�����������H2SO3��HSO3-��SO32-��������SO2��NaOH��Һ��Ӧ�����Һ�У����ǵ����ʵ�������X(i)����ҺpH�Ĺ�ϵ��ͼ��ʾ��
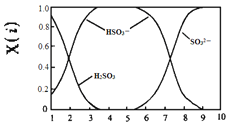
������˵����ȷ����_____������ĸ��ţ���
A.pH=8ʱ����Һ��c(HSO3-) <c(SO32-)
B.pH=7ʱ����Һ��c(Na+)=c(HSO3-)+c(SO32-)
C.Ϊ��þ����ܴ���NaHSO3���ɽ���Һ��pH������4��5����
����pH=5��NaHSO3��Һ�еμ�һ��Ũ�ȵ�CaCl2��Һ����Һ�г��ֻ��ǣ�pH��Ϊ2���û�ѧƽ���ƶ�ԭ��������ҺpH���͵�ԭ��_____��
��3��װ�â��У����������£�NO��Ce4+�����IJ�����Ҫ��NO3-��NO2-��д������NO3-�����ӷ���ʽ____��
��4��װ�â������֮һ������Ce4+����ԭ����ͼ��ʾ��

������Ce4+�ĵ缫��ӦʽΪ_________��
������Ce4+�ӵ��۵�_____������ĸ��ţ���������
��5����֪����װ�â�����Һ�У�NO2-��Ũ��Ϊa g/L��Ҫʹ1m3����Һ�е�NO2-��ȫת��ΪNH4NO3����������װ�â���ͨ���״���µ�O2___L�����ú�a����ʽ��ʾ������������������
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com