
【题目】两种一元碱MOH和ROH的溶液分别加水稀释,溶液pH的变化如图所示,下列叙述正确的是

A. MOH是一种弱碱
B. 在x点,((M+)=c(R+)
C. 稀释前,c(MOH)=l0c(ROH)
D. 稀释前MOH溶液和ROH溶液中由水电离出的c(OH-)前者是后者的10倍
【答案】B
【解析】A、根据图示,溶液稀释100倍,ROH溶液的pH减小了1,MOH溶液pH减小了2,所以MOH是强碱,ROH是弱碱,故A错误;B、在x点,两溶液中pH相等,氢氧根离子浓度等于c(M+)、c(R+),所以c(M+)=c(R+),故B正确;C、由于MOH是强碱,ROH是弱碱,稀释前,MOH等于0.1mol/L,ROH大于0.01mol/L,所以稀释前,c(MOH)<10 c(ROH),故C错误;D、稀释前,MOH溶液中c(OH-)=0.1mol/L,ROH溶液中的c(OH-)=0.01mol/L,由水电离出的c(OH-)分别为10-13 mol/L、10-12 mol/L,因此MOH溶液中水电离的c(OH-)是ROH溶液中由水电离出的氢氧根离子浓度的![]() 倍,故D错误;故选B。
倍,故D错误;故选B。


科目:高中化学 来源: 题型:
【题目】将11.2g铁投入200mL某浓度的盐酸中,铁和盐酸恰好完全反应。求:
(1)11.2g铁的物质的量
(2)所用盐酸中HCl的物质的量浓度
(3)反应中生成的H2在标准状况下的体积
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】全钒液流电池装置如图,电解液在电解质储罐和电池间不断循环。下列说法错误的是
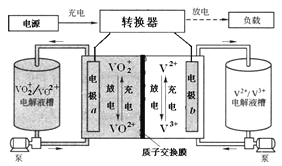
A. 充电时,氢离子通过交换膜移向右侧
B. 充电时,电源负极连接a电极
C. 放电时装置发生的总反应为:VO2++V2++2H+=VO2++V3++H2O
D. 质子交换膜可阻止VO2+与V2+直接发生反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】图用分类法表示了一些物质或概念之间的从属或包含关系,不正确的是( )
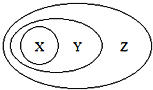
X | Y | Z | |
A | NaAlO2 | 盐 | 纯净物 |
B | 胶体 | 分散系 | 混合物 |
C | Al2O3 | 两性氧化物 | 氧化物 |
D | 单质参与反应 | 置换反应 | 氧化还原反应 |
A. A B. B C. C D. D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定条件下,通过下列反应可实现燃煤烟气中硫的回收:SO2(g)+2CO(g)![]() 2CO2(g)+S(l) ΔH<0,若反应在恒容的密闭容器中进行,下列有关说法正确的是( )
2CO2(g)+S(l) ΔH<0,若反应在恒容的密闭容器中进行,下列有关说法正确的是( )
A. 平衡前,随着反应的进行,容器内压强始终不变
B. 平衡时,其他条件不变,分离出硫,正反应速率加快
C. 平衡时,其他条件不变,升高温度可提高SO2的转化率
D. 其他条件不变,使用不同催化剂,该反应的平衡常数不变
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铁、钴(Co)是同族元素,都是较活泼的金属,它们的化合物在工业上有重要的应用。
(1)草酸钴(CoC2O4)是一种难溶于水的浅粉红色粉末,通常用CoSO4溶液和(NH4)2C2O4溶液反应制得,写出该反应的离子方程式:______________
(2)现将含0.5mol FeCl3的溶液和含1.5mol KSCN的溶液混合,混合后溶液体积为1L,已知溶液存在平衡:Fe3++ 3SCN-=Fe(SCN)3(忽略其它过程)。平衡浓度 c[Fe(SCN)3]与温度T的关系如图1所示:则该反应△H____0(填“>”或“<”),温度为T1时,反应在5秒钟时达到平衡,则达到平衡时的平均反应速率v(SCN-)=____,该温度下的Fe3+的平衡转化率为____。
(3)工业上用电解浓NaOH溶液制备Na2FeO4,其工作原理如图2所示,则Cu电极连接电源的 ___极,阳极的电极反应式为________________

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】X、Y、Z、M、R为五种短周期元素,其原子半径和最外层电子数之间的关系如下图所示。

下列说法不正确的是
A. 简单阳离子半径:X< R
B. 最高价含氧酸的酸性:Z < Y
C. M的氢化物常温常压下为气体
D. X与Y可以形成正四面体结构的分子
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氨气及含氮化合物在化工生产和国防工业中具有广泛应用。请回答:
(1)已知:(i)氢气的燃烧热为286.0 kJ·mol-1
(ii)4NH3(g)+3O2(g)![]() 2N2(g)+6H2O (l) ΔH=- 1530.6 kJ·mol-1。
2N2(g)+6H2O (l) ΔH=- 1530.6 kJ·mol-1。
合成氨反应的热化学方程式为_____________________________。
(2)恒温恒容条件下,起始按物质的量之比为1∶1向密闭容器中充入N2(g)和H2(g),发生合成氨的反应。达平衡后,N2(g)的体积分数为_______________;然后只降低温度,N2(g)的体积分数会_________(填选项字母)。
A.增大 B.减小 C.不变 D.不能判断
(3)T℃时,CO2(g)和NH3(g)合成尿素的原理为2NH3(g)+CO2(g)![]() CO(NH2)2(s)+H2O(1)。在2 L恒容密闭容器中,通入1.2 mol NH3(g)和0.6 mol CO2(g),2 min时反应恰好达到平衡,测得c(NH3)=0.2 mol·L-1。
CO(NH2)2(s)+H2O(1)。在2 L恒容密闭容器中,通入1.2 mol NH3(g)和0.6 mol CO2(g),2 min时反应恰好达到平衡,测得c(NH3)=0.2 mol·L-1。
①0~2min内,用NH3表示的反应速率υ(NH3)=___________;反应的平衡常数K=____________。
②若其他条件不变,2 min时将容器体积迅速压缩到1L,在3 min时重新达到平衡,请在图1中画出2~3 min内c(NH3)随时间(t)变化的曲线关系图。

(4)碱性氨气燃料电池的装置如图2 所示,写出负极的电极反应式____________________。当电路中每通过3.6 mol e-,则需要标况下空气的体积________________L。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】I.已知硝酸铵在不同温度下分解会有不同的产物,反应方程式如下,
![]()
![]()
![]() ①
①
![]()
![]()
![]() ②
②
![]()
![]()
![]() ③
③
![]()
![]()
![]() ④
④
请回答下列问题
(1)若反应②生成标准状况下的33.6LN2O,则转移电子数为______ 。
(2)反应③中物质X的化学式是 _______________。
(3)反应④中氧化产物是 ___________。(填化学式)
II.某同学写出以下三个化学方程式(未配平):
①NO+HNO2→N2O3+H2O ②NH3+NO→HNO2+H2O
③N2O4+H2O→HNO3+HNO2 其中你认为有可能实现的是_________________。
III.下列三个氧化还原反应中,氧化剂氧化性由强到弱的顺序是_________________。
①2FeCl3+2KI=2FeCl2+2KCl+I2
②2FeCl2+Cl2=2FeCl3
③2KMnO4+16HCl(浓)=2KCl+2MnCl2+5Cl2↑+8H2O
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com