
【题目】全钒液流电池装置如图,电解液在电解质储罐和电池间不断循环。下列说法错误的是
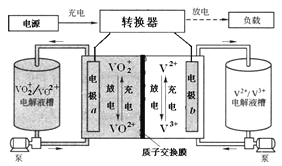
A. 充电时,氢离子通过交换膜移向右侧
B. 充电时,电源负极连接a电极
C. 放电时装置发生的总反应为:VO2++V2++2H+=VO2++V3++H2O
D. 质子交换膜可阻止VO2+与V2+直接发生反应
【答案】B
【解析】分析:本题是一道比较常规的考查电化学知识的试题。解题时应该从图示入手,按照放电的箭头,判断原电池正负极,再按照四个选项的叙述,进行分析。
详解:根据图示的放电箭头,a电极上的反应是VO2+中的+5价V得电子转化为VO2+中的+4价V,所以a为正极,b为负极。
A.充电(电解)时,阳离子应该向阴极(负极)移动,所以氢离子应该通过交换膜移向右侧,选项A正确。
B.电池充电时,正极转化为充电的阳极,负极转化为充电的阴极,所以电源负极应该连接b电极,选项B错误。
C.根据放电的箭头得到,放电时的反应物有:VO2+和V2+,生成物为:VO2+和V3+,所以放电时装置发生的总反应为:VO2++V2++2H+=VO2++V3++H2O(中间是质子交换膜,所以可以在反应物中补充氢离子),选项 C正确。
D.质子交换膜只能允许H+通过,所以可阻止VO2+与V2+直接发生反应,选项D正确。


科目:高中化学 来源: 题型:
【题目】现有金属单质A、B、C和气体甲、乙、丙以及物质D、E、F、G、H,它们之间的相互转化关系如下图所示(图中有些反应的生成物和反应的条件没有标出)。
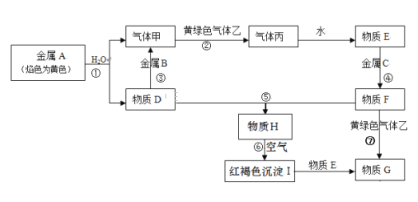
(1)写出下列物质的化学式:B__________,丙__________,乙__________,H__________
(2)根据要求回答:
①D溶液和F溶液在空气中混合的现象__________;
②)反应③离子方程式__________;
③反应⑦离子方程式__________;
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,0.1 mol/L某一元酸(HA)溶液中![]() =1×10-8,下列叙述正确的是
=1×10-8,下列叙述正确的是
A. 溶液中水电离出的c(H+)=10-10 mol/L
B. 溶液中c(H+)+c(A-)=0.1 mol/L
C. 溶液中加入一定量CH3COONa晶体或加水稀释,溶液的c(OH-)均增大
D. 与0.05mol/LNaOH溶液等体积混合后所得溶液中离子浓度大小关系为c(A-)>c(Na+)>c(OH-)>c(H+)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】部分弱酸的电离平衡常数如表:
(1)室温下①0.1 mol·L-1 HCOONa,②0.1 mol·L-1 NaClO,③0.1 mol·L-1 Na2CO3,④0.1 mol·L-1
NaHCO3溶液的pH由大到小的关系为_____________________________________。
(2)浓度均为0.1 mol·L-1的Na2SO3和Na2CO3的混合溶液中,SO![]() 、CO
、CO![]() 、HSO
、HSO![]() 、HCO
、HCO![]() 浓度由大到小的顺序为___________________________________。
浓度由大到小的顺序为___________________________________。
(3)下列离子方程式正确的是________(填字母)。
a.2ClO-+H2O+CO2===2HClO+CO![]() b.2HCOOH+CO
b.2HCOOH+CO![]() ===2HCOO-+H2O+CO2↑
===2HCOO-+H2O+CO2↑
c.H2SO3+2HCOO-===2HCOOH+SO![]() d.Cl2+H2O+2CO
d.Cl2+H2O+2CO![]() ===2HCO
===2HCO![]() +Cl-+ClO-
+Cl-+ClO-
(4)某温度(T ℃)下的溶液中,c(H+)=10-xmol·L-1,c(OH-)=10-y mol·L-1,x与y的关系如图所示.

① 此温度下,0.01mol/L的NaOH溶液中水电离出的OH-浓度为_____。
②在此温度下,0.1 mol·L-1的NaHSO4溶液与0.1 mol·L-1的Ba(OH)2溶液按下表中甲、乙、丙、丁不同方式混合:
甲 | 乙 | 丙 | 丁 | |
0.1 mol·L-1Ba(OH)2溶液体积/mL | 10 | 10 | 10 | 10 |
0.1 mol·L-1NaHSO4溶液体积/mL | 5 | 10 | 15 | 20 |
按丁方式混合后,所得溶液显________(填“酸”“碱”或“中”)性.写出按乙方式混合后,反应的离子方程式:__________________________。按甲方式混合后,所得溶液的pH为________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Ⅰ、下表是元素周期表的一部分。表中所列的字母分别代表一种化学元素。

(1)写出基态时Q元素原子的电子排布式__________,J元素原子的外围电子排布图________________。
(2)下列对比正确的是__________。
a.原子半径H>G>B>A b.第一电离能E>D>C>B
c.电负性A>H>G>Q d.最高价氧化物的水化物酸性B>A>H>G
(3)关于元素在元素周期表中的位置以及元素原子的外围电子排布特点的有关叙述不正确的是______。
a.L位于元素周期表第五周期ⅠA族,属于s区元素
b.O位于元素周期表第七周期Ⅷ族,属于ds区元素
c.M的外围电子排布式为6s1,属于ds区元素
d.H所在族的外围电子排布式为ns2np2,属于p区元素
Ⅱ、已知A、B、C、D、E、F、G都是元素周期表中短周期主族元素,它们的原子序数依次增大。A是元素周期表中原子半径最小的元素,D3B中阴、阳离子具有相同的电子层结构,B、C均可分别与A形成10电子分子,B、C属同一周期,两者可以形成许多种共价化合物,C、F属同一主族,B原子最外电子层的p能级上的电子处于半满状态,C的最外层电子数是内层电子数的3倍,E最外层电子数比最内层多1。请用具体的元素回答下列问题:
(4)F、G元素对应的最高价含氧酸中酸性较强的化学式为__________。
(5)第一电离能:B__________C,电负性:C__________F。(填“<”、“>”或“=”)
(6)A、C形成的一种绿色氧化剂X有广泛应用,X分子中A、C原子个数比为1∶1,X的电子式为____________,试写出Cu、稀硫酸与X反应制备硫酸铜的离子方程式__________。
(7)写出E与D的最高价氧化物对应的水化物反应的化学方程式______________________ 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图所示实验装置,下列说法不正确的是
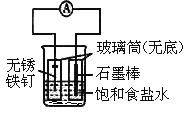
A. 装置为铁的吸氧腐蚀实验
B. 一段时间后,向插入石墨棒的玻璃筒内滴入石蕊试液,可观察到石墨附近的溶液变红
C. 一段时间后,向插入铁钉的玻璃筒内滴入NaOH溶液,即可观察到铁钉附近的溶液有沉淀出现
D. 若将装置中饱和食盐水换成稀硫酸,装置为析氢腐蚀
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铂(Pt)及其化合物用途广泛。
(1)在元素周期表中,Pt与Fe相隔一个纵行、一个横行,但与铁元素同处_____族。基态铂原子有2个未成对电子,且在能量不同的原子轨道上运动,其价电子排布式为____________。
(2)二氯二吡啶合铂是由Pt2+、Cl-和吡啶结合形成的铂配合物,有顺式和反式两种同分异构体。科学研究表明,顺式分子具有抗癌活性。
①吡啶分子是大体积平面配体,其结构简式如图所示。每个吡啶分子中含有的σ键数目为________。
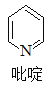
②二氯二吡啶合铂中存在的微粒间作用力有________(填序号)。
a.离子键 b.氢键 c.范德华力 d.金属键 e.非极性键
③反式二氯二吡啶合铂分子是非极性分子,画出其结构式:_____。
(3)某研究小组将平面型的铂配合物分子进行层状堆砌,使每个分子中的铂原子在某一方向上排列成行,构成能导电的“分子金属”,其结构如图所示。
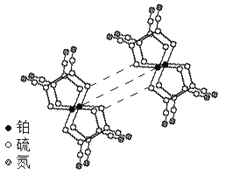
① 硫和氮中,第一电离能较大的是______。
②“分子金属”可以导电,是因为______能沿着其中的金属原子链流动。
③“分子金属”中,铂原子是否以sp3的方式杂化?简述理由:______。
(4)金属铂晶体中,铂原子的配位数为12,其立方晶胞沿x、y或z轴的投影图如图所示。若金属铂的密度为d g·cm-3,则晶胞参数a=_________________nm(列计算式)。

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】两种一元碱MOH和ROH的溶液分别加水稀释,溶液pH的变化如图所示,下列叙述正确的是

A. MOH是一种弱碱
B. 在x点,((M+)=c(R+)
C. 稀释前,c(MOH)=l0c(ROH)
D. 稀释前MOH溶液和ROH溶液中由水电离出的c(OH-)前者是后者的10倍
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】C60具有完美的球形结构。之后Si60、N60等球形分子被不断制备出来。回答下列问题:
(1)Si 的核外电子排布式为____________,C和N元素中第一电离能较大的是________________。
(2)富勒烯衍生物具有良好的光电性能,富勒烯(C60)的结构如图所示,C60属于________晶体;C60中C原子的杂化类型为__________________。

(3)N60的晶体中存在的作用力有____________(填字母)。
A.共价键 B.离子键 C.氢键 D.范德华力 E.配位键 F.金属键
(4)立方氮化硼(BN)可做磨料,其结构与金刚石相似,二者具有相似性结构的原因是______________________________________________。
(5)金属M(相对原子质量为m)与N60形成的化合物晶体结构如图所示(其中白球代表N60,黑球代表金属M),其晶胞边长为k pm,NA代表阿伏加德罗常数的值,则其密度为_______g·cm-3,该化合物中N60的配位数为__________________。

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com