
| A、分液时,分液漏斗中下层液体从下口放出,上层液体从上口倒出 |
| B、蒸馏时,应使温度计水银球靠近蒸馏烧瓶支管口 |
| C、滴定时,左手控制滴定管活塞,右手握持锥形瓶,边滴边振荡,眼睛注视滴定管中的液面 |
| D、称量时,称量物放在称量纸上,置于托盘天平的左盘,砝码放在托盘天平的右盘中(放有等质量的纸) |


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
| A | |||
| B | C | D |
| 催化剂 |
| 选项 | a | b | c | d |
| x | 温度 | 温度 | 加入H2的物质的量 | 加入甲的物质的量 |
| y | 甲的物质的量 | 平衡常数K | 甲的转化率 | 生成物物质的量总和 |
查看答案和解析>>
科目:高中化学 来源: 题型:
 Ⅰ.25℃时,在20ml Ba(OH)2溶液中逐滴加入0.2mol/L醋酸溶液,曲线如图所示,试回答以下问题:
Ⅰ.25℃时,在20ml Ba(OH)2溶液中逐滴加入0.2mol/L醋酸溶液,曲线如图所示,试回答以下问题:查看答案和解析>>
科目:高中化学 来源: 题型:
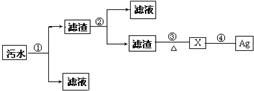
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、向水中滴加FeCl3的稀溶液,以制备Fe(OH)3胶体 |
| B、用盐酸滴定氢氧化钠,用酚酞作指示剂,当锥形瓶中溶液由无色变成红色时即达到滴定终点 |
| C、室温下,用pH试纸测定浓度为0.1 mol?L-1 NaClO溶液和0.1 mol?L-1 CH3COONa溶液的pH,比较HClO和CH3COOH的酸性强弱 |
| D、室温下,向Mg(OH)2中加入饱和氯化铵溶液能使Mg(OH)2溶解 |
查看答案和解析>>
科目:高中化学 来源: 题型:
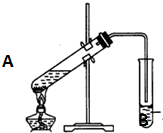 实验室用一定比例的乙醇、乙酸和浓硫酸的混合液制备乙酸乙酯,装置如图所示:
实验室用一定比例的乙醇、乙酸和浓硫酸的混合液制备乙酸乙酯,装置如图所示:查看答案和解析>>
科目:高中化学 来源: 题型:
| A、①②③ | B、②⑥⑦ |
| C、③④⑤ | D、④⑤⑦ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A | B | C | D | |
| A | ↑ | ↓ | - | |
| B | ↑ | ↓ | ↑ | |
| C | ↓ | ↓ | - | |
| D | - | ↑ | - |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、空气、天然气、苛性钾、石灰石 |
| B、液态氯化氢、稀硫酸、硫酸钠晶体、二氧化硫 |
| C、盐酸、水煤气、醋酸、干冰 |
| D、纯碱、铝合金、冰水混合物、乙醇 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com