
| A | |||
| B | C | D |
| 催化剂 |
| 选项 | a | b | c | d |
| x | 温度 | 温度 | 加入H2的物质的量 | 加入甲的物质的量 |
| y | 甲的物质的量 | 平衡常数K | 甲的转化率 | 生成物物质的量总和 |
| 27g/mol×2mol |
| 13.5g |
| 催化剂 |
| c(NH4+)?c(OH-) |
| c(NH3?H2O) |
| 0.02×10-7 |
| a-0.02 |
| 2 |
| a-0.02 |
| 2 |
| a-0.02 |


 课堂全解字词句段篇章系列答案
课堂全解字词句段篇章系列答案科目:高中化学 来源: 题型:
| A、厕所清洁剂 醋 肥皂 厨房清洁剂 |
| B、醋 厕所清洁剂 肥皂 厨房清洁剂 |
| C、厕所清洁剂 厨房清洁剂 醋 肥皂 |
| D、厨房清洁剂 醋 肥皂 厕所清洁剂 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、X、M两种元素形成的化合物只能存在离子键 |
| B、元素Y、Z、W的单质晶体属于同种类型的晶体 |
| C、由于W、Z、M元素的氢化物相对分子质量依次减小,所以其沸点依次降低 |
| D、元素W和M的某些单质可作为水处理中的消毒剂 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
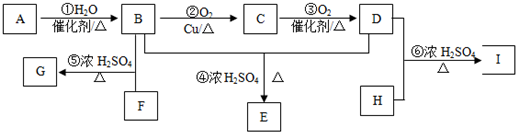
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、分液时,分液漏斗中下层液体从下口放出,上层液体从上口倒出 |
| B、蒸馏时,应使温度计水银球靠近蒸馏烧瓶支管口 |
| C、滴定时,左手控制滴定管活塞,右手握持锥形瓶,边滴边振荡,眼睛注视滴定管中的液面 |
| D、称量时,称量物放在称量纸上,置于托盘天平的左盘,砝码放在托盘天平的右盘中(放有等质量的纸) |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com