
【题目】已知K2Cr2O7溶液中存在如下平衡:Cr2O72-(橙色)+ H2O![]() 2H++ 2CrO42-(黄色)①向2 mL 0.1 mol·L-1 K2Cr2O7溶液中滴入3滴6 mol·L-1 NaOH溶液,溶液由橙色变为黄色;向所得溶液中再滴入5滴浓H2SO4,溶液由黄色变为橙色。②向2 mL 0.1 mol·L-1 酸化的K2Cr2O7溶液中滴入适量(NH4)2Fe(SO4)2溶液,溶液由橙色变为绿色,发生反应:Cr2O72- + 14H++ 6Fe2+=2Cr3+(绿色) + 6Fe3+ + 7H2O。
2H++ 2CrO42-(黄色)①向2 mL 0.1 mol·L-1 K2Cr2O7溶液中滴入3滴6 mol·L-1 NaOH溶液,溶液由橙色变为黄色;向所得溶液中再滴入5滴浓H2SO4,溶液由黄色变为橙色。②向2 mL 0.1 mol·L-1 酸化的K2Cr2O7溶液中滴入适量(NH4)2Fe(SO4)2溶液,溶液由橙色变为绿色,发生反应:Cr2O72- + 14H++ 6Fe2+=2Cr3+(绿色) + 6Fe3+ + 7H2O。
下列分析正确的是
A.实验①和②均能证明K2Cr2O7溶液中存在上述平衡
B.实验②能说明氧化性:Cr2O72-> Fe3+
C.CrO42-和Fe2+在酸性溶液中可以大量共存
D.稀释K2Cr2O7溶液时,溶液中各离子浓度均减小
 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
【题目】在4 L密闭容器中充入6 mol A气体和5 mol B气体,在一定条件下发生反应:3A(g)+B(g) ![]() 2C(g)+xD(g),达到平衡时,生成了2 mol C,经测定,D的浓度为0.5 mol·L-1,下列判断正确的是( )。
2C(g)+xD(g),达到平衡时,生成了2 mol C,经测定,D的浓度为0.5 mol·L-1,下列判断正确的是( )。
A.x=1
B.B的转化率为20%
C.平衡时A的浓度为1.50 mol·L-1
D.达到平衡时,在相同温度下容器内混合气体的压强是反应前的85%
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是
A. 正丁烷和异丁烷均有两种一氯取代物
B. 乙烯和苯都能与H2发生加成反应,说明二者的分子中均含碳碳双键
C. 乙醇与金属钠能反应,且在相同条件下比水与金属钠的反应更剧烈
D. 乙醛能被还原成乙醇,但不能被氧化成乙酸
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,下列各组离子在指定溶液中一定能大量共存的是( )
A. ![]() 的溶液中:Na+、K+、AlO2-、NO3-
的溶液中:Na+、K+、AlO2-、NO3-
B. 含有大量Fe3+的溶液中:NH4+、I-、Cl-、K+
C. pH=7的溶液中:NH4+、Al3+、SO42-、NO3-
D. 0.1mol·L-1Na2SO3的溶液中:H+、Ca2+、Fe2+、Cl-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)氯化铝水溶液呈 性,原因是: (用离子方程式表示);把AlCl3溶液蒸干,灼烧,最后得到的主要固体产物是 。
(2)硫化钠溶于水时发生水解,其水解的离子方程式为 (只写第一步),在配制硫化钠 溶液时可以加入少量的 以抑制其水解。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】I、现有含CaO杂质的CaC2试样。设计以下实验,测定CaC2试样的纯度。(反应方程式为:CaC2+2H2O→Ca(OH)2+C2H2↑),请从下图中选用适当的装置,完成该实验。
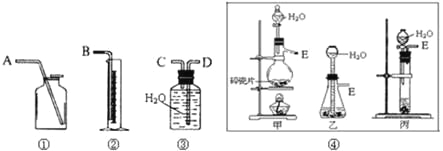
(1)制取C2H2最好选④中的 装置(填“甲”“乙”或“丙”),所选用装置的连接顺序是 (填各接口A~E的顺序)。
(2)若实验时称取的试样为1.4g,产生的乙炔在标准状况下的体积为448mL,此试样中CaC2的质量分数为 。(保留3为有效数字)

II、某同学在实验室从如图标签的试剂瓶中取少许钠进行燃烧实验,实验后 发现还有少许黑色固体生成。从反应物及实验操作猜测:
该黑色物质可能为碳与另一种氧化物组成的混合物。
根据题意和图示回答下面问题:
(1)装置图⑤中A的名称 。
(2)此氧化物可能是 或 (写化学式)。
(3)对黑色固体物质的组成作如图⑥所示研究
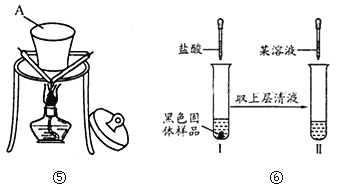
①实验I中加入盐酸溶液的目的是 。
②仅通过实验II,用最简步骤能快速确定黑色氧化物的组成,请完善该设计。(限选试剂:稀盐酸、KSCN溶液、10%H2O2溶液)
实验操作 | 预期现象与结论 | 相关离子方程式 |
取少量实验I中的澄清溶液,加入试剂 |
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知:C(s)+ 1/2O2(g)CO(g) ΔH1 =—110.5 kJ/mol
CO(g)+ 1/2O2(g)CO2(g) ΔH2 = —283.0 kJ/mol
则反应C(s)+O2(g)CO2(g)的反应热为
A. 172.5 kJ/mol B. —172.5 kJ/mol C. 393.5 kJ/mol D. —393.5 kJ/mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】水煤气(CO 和H2)是合成甲醇的重要原料,它可用水蒸气通过炽热的炭层制得:C(s)+H2O(g)![]() CO(g)+H2(g) △H=+131.3kJ/mol
CO(g)+H2(g) △H=+131.3kJ/mol
⑴该反应的平衡常数的表达式为:_________________;升高温度,K值将 ;容器中气体的平均相对分子质量将 。(填“增大”、“减小”或“不变”)。
⑵上述反应达到平衡后,将体系中的C(s)部分移走,平衡将 (填序号)。
A.向左移 B.向右移 C.不移动
⑶下列事实能说明该反应在一定条件下已达到平衡状态的有 (填序号)。
A.单位体积内每消耗1molCO的同时生成1molH2
B.混合气体总物质的量保持不变
C.生成H2O(g)的速率与消耗CO的速率相等
D.H2O(g)、CO、H2的浓度相等
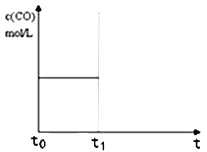
⑷上述反应在t0时刻达到平衡(如图),若在t1时刻改变某一条件,请在图中继续画出t1时刻后c(CO)随时间的变化曲线:
①缩小容器体积(用实线表示)。
②降低温度(用虚线表示)。
⑸某温度下,将4.0mol H2O(g)和足量的炭充入2L的密闭容器中,发生如下反应,C(s)+H2O(g)![]() CO(g)+H2(g),达到平衡时测得K=1,则此温度下H2O(g)的转化率为 。
CO(g)+H2(g),达到平衡时测得K=1,则此温度下H2O(g)的转化率为 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com