
【题目】下列物质中,能够导电的电解质是( )
A. 铜丝 B. 熔融的MgCl2 C. NaCl溶液 D. SO3
科目:高中化学 来源: 题型:
【题目】在2L容积不变的密闭容器内,800℃时反应2NO(g)+O2(g)![]() 2NO2(g)体系中,n(NO)随时间的变化如下表:
2NO2(g)体系中,n(NO)随时间的变化如下表:

(1)用O2的反应速率表示0~2s内该反应的平均反应速率v=_______________。若上述反应在850℃下进行,反应2s时n(NO)=0.009mol,并且不再随时间而改变,则该反应是__________热反应。
(2)图中表示NO2浓度变化的曲线是__________(填字母)。
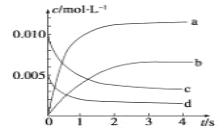
(3)能说明该反应已达到平衡状态的是________(填序号)。
A.v(NO2)=2v(O2) B.容器内的压强保持不变
C.v逆(NO)=2v正(O2) D.容器内气体密度保持不变
(4)能使该反应的反应速率增大,且平衡向正反应方向移动的是________(填序号)。
A.及时分离出NO2 B.适当升高温度
C.增大O2的浓度 D.选择高效催化剂
查看答案和解析>>
科目:高中化学 来源: 题型:
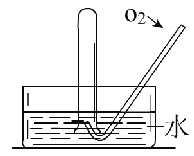
【题目】如图所示,将一瓶充满NO2气体的试管倒扣在水槽中,气体颜色由____逐渐变为____色,试管内的液面会逐渐_____________;当反应停止后向试管中缓慢通入氧气,气体颜色又由______色逐渐变为______色,之后又变为______色,试管内的液面会____________。用化学方程式表示试管中发生的化学反应_____________,____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列实验对应的现象及结论均正确,且两者具有因果关系的是
选项 | 实验 | 现象 | 结论 |
A | 向稀硝酸与过量铜粉反应后的溶液中滴加稀硫酸 | 有气泡生成 | 常温下,铜与稀硫酸反应生成SO2 |
B | 在酒精灯上加热铝箔 | 铝熔化,但熔化的铝不滴落 | Al2O3的熔点比Al高 |
C | 向Fe(SCN)3溶液中滴加稀NaOH溶液 | 溶液有红色变为红褐色 | 减小反应物浓度、平衡向逆反应方向移动 |
D | 选用酚酞作试剂,用NaOH溶液滴定醋酸溶液 | 溶液变为粉红色 | NaOH溶液过量 |
A. A B. B C. C D. D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在容积为1 L的密闭容器中,加入1.0 mol A和2.2 mol B进行如下反应:A(g) + 2B(g) ![]() C(g) + D(g),在800℃时,D的物质的量n(D)和时间t的关系如图。
C(g) + D(g),在800℃时,D的物质的量n(D)和时间t的关系如图。
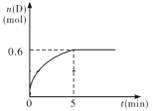
(1)800℃时,0~5 min内,以B表示的平均反应速率为____________。
(2)利用图中数据计算在800 ℃时的平衡常数的数值为___________。
(3)若700℃,反应达平衡时,A的浓度为0.55mol/L,则该反应为_________反应(填“吸热”或“放热”)。
(4)800 ℃时,某时刻测得体系中物质的量浓度如下:c(A)=0.06 mol·L-1,c(B)=0.50 mol·L-1,c(C)=0.20 mol·L-1,c(D)=0.018 mol·L-1,则此时该反应______________(填“向正方向进行”、“向逆方向进行”或“处于平衡状态”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定质量的Na、K分别投入足量的同浓度、同体积的稀盐酸中,在相同条件下产生氢气的体积随时间变化的曲线如图中a、b所示,则下列说法中不正确的是

A. 曲线a对应的反应使用了催化剂
B. 投入的Na、K物质的量相等
C. 曲线a代表K的反应,曲线b代表Na的反应
D. 两反应中反应速率不同的主要原因是反应物自身的性质不同
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】电解原理在化学工业中有广泛应用。如图表示一个电解池,装有电解液a,X、Y是两块电极板,通过导线与直流电源相连。请回答以下问题:
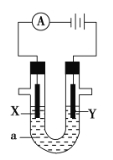
(1)若X、Y都是惰性电极,a是AgNO3溶液,实验开始时,同时在两边各滴入几滴石蕊试液,则
①电解池中Y电极上的电极反应式为 。在Y电极附近观察到的实验现象是 ;检验该电极反应产物的方法是 。
②X电极上的电极反应式为 。
(2)如要用电解方法精炼粗镍,电解液a选用Ni(NO3)2溶液,则:
①X电极的材料是 ,电极反应式为 ;
②Y极的材料是 ,电极反应式为 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知K2Cr2O7溶液中存在如下平衡:Cr2O72-(橙色)+ H2O![]() 2H++ 2CrO42-(黄色)①向2 mL 0.1 mol·L-1 K2Cr2O7溶液中滴入3滴6 mol·L-1 NaOH溶液,溶液由橙色变为黄色;向所得溶液中再滴入5滴浓H2SO4,溶液由黄色变为橙色。②向2 mL 0.1 mol·L-1 酸化的K2Cr2O7溶液中滴入适量(NH4)2Fe(SO4)2溶液,溶液由橙色变为绿色,发生反应:Cr2O72- + 14H++ 6Fe2+=2Cr3+(绿色) + 6Fe3+ + 7H2O。
2H++ 2CrO42-(黄色)①向2 mL 0.1 mol·L-1 K2Cr2O7溶液中滴入3滴6 mol·L-1 NaOH溶液,溶液由橙色变为黄色;向所得溶液中再滴入5滴浓H2SO4,溶液由黄色变为橙色。②向2 mL 0.1 mol·L-1 酸化的K2Cr2O7溶液中滴入适量(NH4)2Fe(SO4)2溶液,溶液由橙色变为绿色,发生反应:Cr2O72- + 14H++ 6Fe2+=2Cr3+(绿色) + 6Fe3+ + 7H2O。
下列分析正确的是
A.实验①和②均能证明K2Cr2O7溶液中存在上述平衡
B.实验②能说明氧化性:Cr2O72-> Fe3+
C.CrO42-和Fe2+在酸性溶液中可以大量共存
D.稀释K2Cr2O7溶液时,溶液中各离子浓度均减小
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在实验室中手不慎被玻璃划破,可用FeCl3溶液应急止血,其主要原因可能是( )。
A.FeCl3溶液有杀菌消毒作用
B.FeCl3溶液能使血液胶体发生聚沉
C.FeCl3溶液能产生Fe(OH)3沉淀堵住伤口
D.FeCl3能使血液发生化学反应
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com